Анемия — симптомы и лечение
Что такое анемия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Голышевой Екатерины Николаевны, терапевта со стажем в 10 лет.
Над статьей доктора Голышевой Екатерины Николаевны работали литературный редактор Юлия Липовская , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Анемия, или малокровие (Anemia) — это уменьшение количества эритроцитов и снижение уровня гемоглобина.
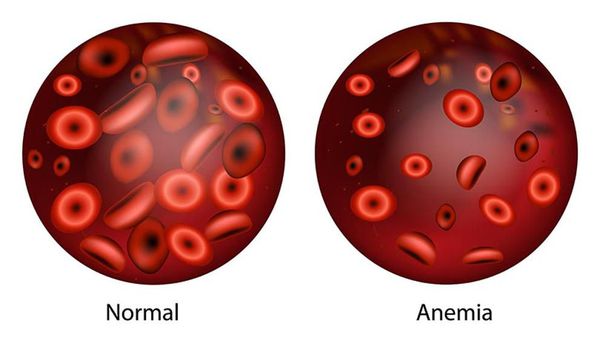
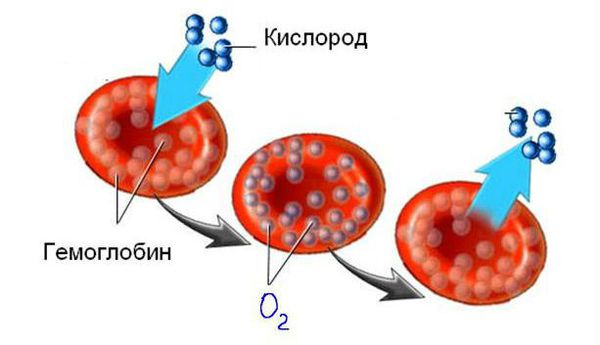
Эритроциты — это красные кровяные тельца, в них нет клеточного ядра, зато они содержат в себе особый железосодержащий белок — гемоглобин (Hb), который выполняет в организме важнейшую функцию газообмена (переносит кислород из лёгких в ткани и уносит от них углекислый газ). Следовательно, уменьшение количества эритроцитов в крови ведёт в снижению уровня гемоглобина. Есть ещё одно важное понятие — гематокрит (Hct) — это процентное соотношение эритроцитов к плазме крови.
У мужчин анемию определяют при следующий показателях:
Для детей показатели нормы с возрастом меняются, поэтому нужно использовать специальные возрастные таблицы [4] .
Выделяют наследственные типы анемий:
- При нарушении строения мембраны эритроцитов:
- анемия Минковского — Шоффара (микросфероцитарная гемолитическая анемия, или наследственный сфероцитоз) — заболевание, в основе которого лежит дефект белков мембраны эритроцитов;
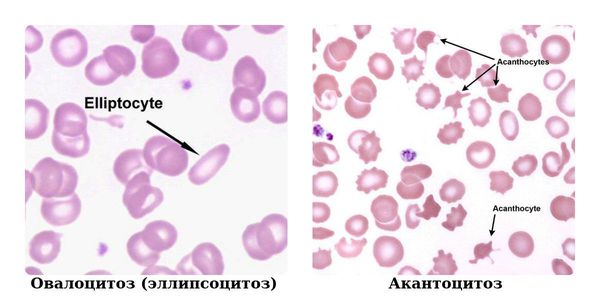
- овалоцитоз (эллипсоцитоз) — заболевание, при котором эритроциты имеют овальную или эллиптическую форму;
- акантоцитоз — наличие в периферической крови эритроцитов с различными выростами цитоплазмы.
- При дефиците энзимов (белков, ускоряющих биохимические реакции) в эритроцитах.
- При нарушении образования гемоглобина (талассемия, серповидноклеточная анемия, гемоглобинозы).
В ряде случаев причинами анемии являются недостаток определённых витаминов и микроэлементов (В12, фолиевая кислота, железо), либо проблема с их усвояемостью.
Вторичные причины развития анемии
По своей сущности анемия является симптомом многих состояний: онкологических заболеваний или заболеваний, сопровождающихся хроническим кровотечением (язвенная или эрозивная болезнь органов пищеварения, геморрой). Но ввиду важности этого симптома и значительного его распространения анемия фактически приравнивается к нозологической самостоятельности, то есть к отдельной группе диагнозов [1] .
К причинам развития железодефицитной анемии (ЖДА) относятся:
- хронические кровопотери;
- нарушение всасывания микроэлементов и витаминов в кишечнике;
- повышенная потребность в железе (например, в период беременности);
- нарушение его транспорта (доставки органам и тканям);
- недостаточное поступление в организм с продуктами питания.
Например, высокая потребность в железе является главной причиной ЖДА у беременных и матерей, кормящих грудью. У женщин репродуктивного возраста в большинстве случаев железодефицитная анемия возникает вследствие обильных менструаций, а у детей — из-за недостаточного потребления с пищей. ЖДА может являться следствием несбалансированного питания при вегетерианской диете, так как железо из растительных продуктов усваивается хуже. В продуктах растительного происхождения содержится фитиновая кислота, которая образует с железом нерастворимые комплексы и ухудшает всасывание железа из этих продуктов. Лучше всего железо усваивается из продуктов животного происхождения, в мясе присутствует белок миоглобин, который улучшает всасывание железа в кишечнике.
Главное место среди причин анемий занимают острые и хронические кровопотери, нарушение кроветворения, ряд хронических и инфекционных заболеваний. Хронические кровопотери определяются малым объёмом теряемой крови, небольшой продолжительностью, очень часто протекают скрыто для самих больных и не всегда воспринимаются как первопричина анемии лечащими врачами разных специальностей. Такие кровопотери могут происходить, например, в случае обильных менструальных кровотечений у женщин, которые привыкают к этому и считают нормой. В этом случае неправильно и не до конца собранный гинекологический анамнез зачастую остаётся на «заднем» плане при диагностическом поиске причин анемии. При подозрении на скрытый дефицит железа, либо на любую другую анемию необходимо уточнять длительность менструального цикла, объём и продолжительность менструальных выделений. Прямо спрашивать о количестве расходуемых прокладок в сутки, необходимости замены ночью, что уже является признаком избыточной потери крови и требует консультации гинеколога для определения тактики ведения.
При острых кровотечениях с большим объёмом теряемой крови анемия развивается из-за резкого снижения эритроцитарной массы и зависит от степени кровопотери, а также от компенсаторной активации кроветворения. Длительно текущие хронические кровопотери неизбежно вызывают истощение депо (запасов) железа с развитием анемии. Условно в 1 мл крови содержится 0,5 мг железа, если у больного, допустим, кровоточащий геморрой, то потеря 2-3 чайных ложек крови каждый день (10 мл = 5 мг железа) будет выше суточного поступления железа. Вследствие этого сильно снижаются его запасы, что уже является фактором риска развития железодефицитной анемии, либо скрытого дефицита железа [2] .
Анемия у детей
Анемия у детей проявляется такими же симптомами, как и анемия у взрослых: слабостью, быстрой утомляемостью, сонливостью, сухостю кожи, «заедами» в углах рта, выпадением волос, частыми головными болями, головокружениями, обмороками, шумом в ушах, снижением памяти и концентрации внимания, частыми простудными заболевания. У детей к анемии может присоединиться ночное недержание мочи (энурез). Также у детей с анемией страдает нервная система: ребёнок становится вялым, плаксивым, беспокойным, у него поверхностный сон, он плохо кушает и не набирает вес. Дети с тяжёлой анемией в возрасте до одного года могут отставать в развитии от сверстников.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы анемии
У анемий нет чётких специфичных симптомов, поэтому дифференциальная диагностика по одной лишь клинической картине невозможна. Признаки анемии появляются только тогда, когда уровень гемоглобина сильно снижается относительно индивидуального исходного показателя пациента. Симптомы в основном более выражены у больных с другими хроническими неинфекционными заболеваниями, к примеру эрозивными или язвенными болезнями желудочно-кишечного тракта, воспалительными заболеваниями тонкого кишечника (целиакия, болезнь Крона) или при стремительном развитии анемии.
При развитии анемии появляются бледность кожных покровов, общая слабость, тошнота, головокружение, загрудинные боли, тахикардия, одышка, в тяжёлых случаях бывают синкопы (потеря сознания). К ряду возможных симптомов анемии относятся: головная боль, головокружение, шум в ушах, отсутствие менструаций и расстройства пищеварения. При тяжёлой анемии развивается гипоксия тканей или гиповолемия, в этом случае возрастает вероятность наступления сердечно-сосудистой недостаточности или шока.
Симптомы, определяющие происхождение анемии
Симптомы анемии, развивающейся вследствие острой или хронической кровопотери: мелена (кал чёрного цвета, свидетельствующий о внутреннем кровотечении из верхних отделов желудочно-кишечного тракта), носовое кровотечение, обильные менструальные выделения, кровотечение из геморроидальных узлов.
Пожелтение кожных покровов и склер, моча тёмного цвета при отсутствии заболеваний печени указывают на разрушение эритроцитов с выделением гемоглобина (гемолиз).
Стремительная потеря веса без объективных причин может являться следствием онкологического процесса в организме.
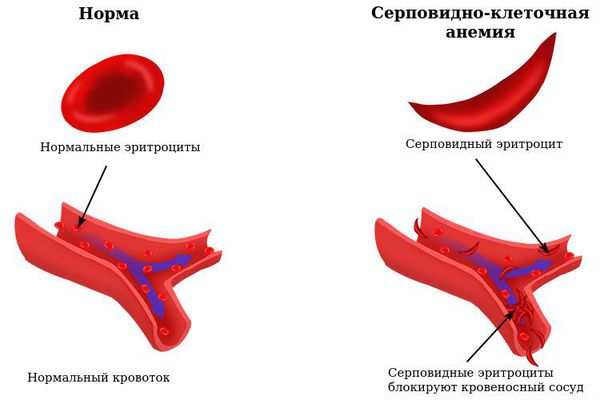
Интенсивная боль в грудной клетке или костях может указывать на серповидно-клеточную анемию (наследственное заболевание крови, в основе которого нарушение структуры белка гемоглобина), а ощущение жжения, покалывания, ползания мурашек по всей поверхности кистей — на B12-дефицитную анемию [4] .
Патогенез анемии
У каждой разновидности анемии имеется своя причина, но их патогенез очень схож, поэтому рассмотрим механизм развития часто встречающихся анемий.
Патогенез железодефицитной анемии складывается из двух механизмов:
- Встречается при всех анемиях: гипоксические изменения (нарушение функции тканевого дыхания) в тканях и органах, возникающие в результате снижения количества гемоглобина в организме. Клинические проявления гипоксических изменений представлены общей слабостью, сонливостью, снижением умственной работоспособности и физической выносливости, шумом в ушах, головокружениями, обморочными состояниями, одышкой при нагрузке, сердцебиением, бледностью.
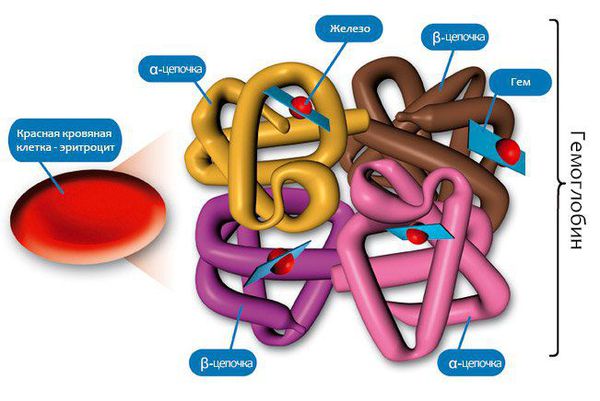
- Присущ исключительно железодефицитной анемии: замедление активности ферментов, содержащих железо, участвующих в тканевом дыхании клеток. Основой формирования железодефицитной анемии является дефицит железа в организме. Железо является каркасом для образования молекул гемоглобина, а именно его железосодержащей части — гема.
Дефицит железа, как и другие анемии в организме, проходит три стадии:
- Прелатентная — скрытая форма, так как эта стадия не имеет клинических проявлений.
- Латентная — нарушается тканевое дыхание и ферментативная активность.
- Анемия — снижение общего количества гемоглобина или гематокрита, уменьшение количества эритроцитов [1] .
Патогенез В12-дефицитной анемии
Сущность В12 дефицитной анемии заключается в нарушении процесса созревания красных кровяных клеток вследствие дефицита витамина В12 или В9 (фолиевой кислоты).
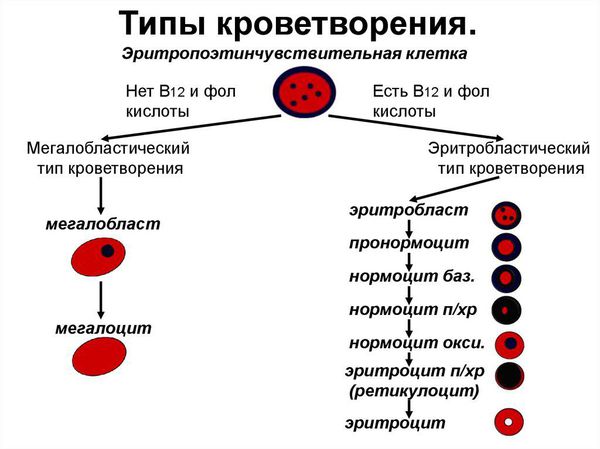
При дефиците витамина В12 прежде всего страдают: костный мозг, головной мозг и эпителий желудочно-кишечного тракта. В красном ростке кроветворения появляется мегалобластный тип кроветворения: возникает дефект синтеза ДНК, в результате чего формируются очень крупные клетки — мегалобласты, а из них мегалоциты; нарушается синхронность созревания ядра и цитоплазмы эритроцитов; красные кроветворные клетки гибнут рано. В это же время снижается гранулоцитопоэз (образование гранулоцитов, которые представляют собой самую многочисленную группу лейкоцитов) и тромбоцитопоэз (образование тромбоцитов).
При недостатке витамина В12 нарушается обмен жирных кислот и накапливаются нейротоксичные метилмалоновая и пропионовая кислоты. Синтез миелина (вещества, образующего миелиновую оболочку нервных волокон) нарушается. Повреждаются задние и боковые спинномозговые столбы [3] .
Классификация и стадии развития анемии
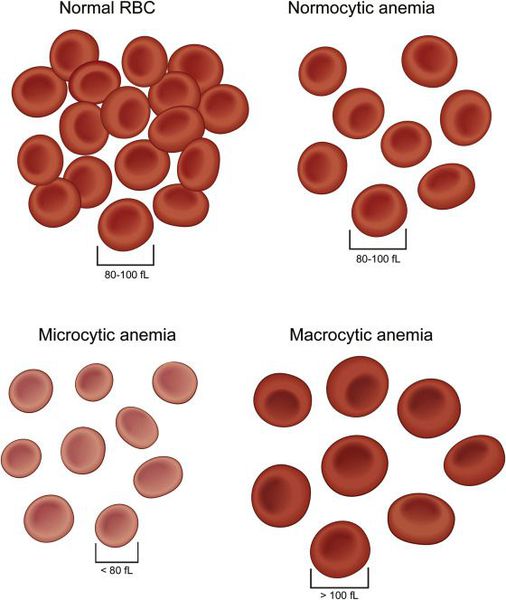
I. Классификация анемий по морфологии (размеру) эритроцитов
- Макроцитарная — тип анемии, при которой образуются эритроциты крупных размеров (макроциты):
- дефицит витамина В12 и фолиевой кислоты;
- эритролейкоз — это редкая форма острого миелоидного лейкоза (рака кроветворной системы), характеризующаяся наличием в крови большого количества ядерных эритроцитов;
- миелодисплазия — врождённое заболевание, характеризующееся патологическими изменениями в позвоночном столбе и спинном мозге и нарушениями миелоидного кроветворения (образования эритроцитов, гранулоцитов, тромбоцитов и моноцитов). Как правило, доброкачественные опухоли при миелодисплазии представлены кистами, реже встречаются другие формы новообразований.
- Анемия микроцитарная — разновидность анемий, которые характеризуются уменьшением размеров эритроцитов. К этому типу относятся:
- талассемия (анемия Кули) — заболевание, при котором нарушается синтез жизненно важного белка гемоглобина, входящего в состав эритроцитов.
- микросфероцитоз — это гемолитическая анемия, обусловленная генетическим дефектом мембран эритроцитов и характеризующаяся постоянным гемолизом — разрушением эритроцитов с выделением в окружающую среду гемоглобина;
- железодефицитная анемия.
- Нормоцитарная анемия — это тип анемии, при котором эритроциты имеют нормальный размер.
- гипопластическая — патология, характеризующаяся угнетением кроветворной функции костного мозга;
- гемолитические анемии — патология эритроцитов, в основе которой ускоренное разрушение красных кровяных телец;
- анемии вследствие хронических заболеваний;
- анемия при меилодиспластическом синдроме — заболевание системы крови, при которых нарушается нормальное кроветворение вследствие диспластических изменений костного мозга.
II. Классификация по цветовому показателю (ЦП)
- Гипохромная анемия (ЦП менее 0,8): железодефицитная анемия, железоперераспределительная анемия, талассемия и др.
- Нормохромная анемия (ЦП от 0.86 до 1.06 ): апластическая анемия, анемия при меилодиспластическом синдроме и др.
- Гиперхромная (ЦП выше 1,05): В12-дефицитная анемия, дефицит фолиевой кислоты и др.

III. Классификация анемий патогенетическая
Анемии вследствие кровопотери:
- Постгеморрагическая анемия острая.
- Постгеморрагическая анемия хроническая.
Анемии, вызванные нарушением образования гемоглобина и эритроцитов:
- Железодефицитная анемия.
- Анемия вследствие неправильного перераспределения железа.
- Железонасыщенная анемия из-за нарушения синтеза гема.
- Мегалобластные анемии при нарушении синтеза ДНК.
- В12-дефицит и дефицит фолиевой кислоты.
- Мегалобластные анемии при дефиците ферментов, принимающих участие в синтезе пуриновых оснований (аденина, гуанина), которые участвуют в построении нуклеотидов, нуклеиновых кислот и др. биологически активных соединений, и пиримидиновых оснований (урацила, цитозина, тимина), входящих в состав нуклеиновых кислот, нуклеозидов, нуклеотидов.
- В12 (фолиево)-ахрестическая анемия. Возникает вследствие того, что костный мозг не в состоянии использовать имеющиеся в организме антианемические субстанции (витамин B12, фолиевую кислоту).
- Анемии гипопролиферативные.
- Анемии вследствие недостаточности костного мозга.
- Апластическая анемия — патология кроветворной системы, которая подавляет кроветворную функцию костного мозга и проявляется низким образованием эритроцитов, лейкоцитов и тромбоцитов или только одних эритроцитов.
- Рефрактивная анемия при миелодиспластическом синдроме.
- Анемии метапластические
- Анемия вследствие гемобластозов (новообразований, развивающихся в кроветворной и лимфатической системе).
- Анемия вследствие метастазирования рака в костный мозг.
- Анемии из-за нарушения эритропоэза.
Анемии при усиленном кроверазрушении.
- Наследственные.
- При нарушении строения мембраны эритроцитов (анемия Минковского — Шоффара микросфероцитарная, овалоцитоз, акантоцитоз).
- При дефиците энзимов в эритроцитах.
- При нарушении образования гемоглобина (талассемия, серповидноклеточная анемия, гемоглобинозы).
- Приобретённые.
- Аутоиммунные.
- Периодическая ночная гемоглобинурия (попадание гемоглобина в мочу в результате повреждения сосудов). Причиной пароксизмальной ночной гемоглобинурии является соматическая мутация в стволовых клетках костного мозга, которая приводит к нарушению регулирования системы комплемента (части иммунной системы, которая осуществляет защиту от бактерий и других возбудителей болезней), разрушению эритроцитов, тромбозам вен и артерий, недостаточности костного мозга. Мутация находится в Х-сцепленном гене фосфатидилинозитолгликана класса А (PIG-A).
- Лекарственные.
- После травм и вследствие микроангиопатий.
- При отравлении гемолитическими ядами и токсинами бактерий.
IV. Анемии по степеням тяжести EORTC (Европейское общество диагностики и лечения рака)
Степень тяжести анемии и количество гемоглобина:
- 0 степень > 120 г/л;
- 1 степень — 120-100 г/л;
- 2 степень — 100-80 г/л;
- 3 степень — 80-65 г/л;
- 4 степень — менее 65 г/л [3] .
Осложнения анемии
Больные анемией отмечают влияние ряда симптомов на их повседневную активность.
Хроническая усталость. Последствием анемии может быть постоянная общая слабость, сонливость, упадок сил, рассеянность, невозможность полноценно и регулярно заниматься спортом.
Иммунная система. По результатам исследований доказано, что анемия влияет на иммунитет, делая человека более восприимчивым к хроническим и инфекционным болезням.
Тяжёлая анемия увеличивает риск развития осложнений, направленных на сердечно-сосудистую систему или дыхательную. Могут появиться тахикардия (учащённое сердцебиение) и сердечная недостаточность (недостаточная эффективность кровоснабжения организма).
Беременность. Тяжёлые анемии у беременных женщин увеличивают риск ухудшения внутриутробного питания плода, осложнений во время родов и послеродовом периоде. Также такие пациентки более подвержены послеродовой депрессии. Ряд исследований показал, что дети, рождённые от женщин с анемией во время беременности, с высокой вероятностью:
- рождены недоношенными (до 37 недели беременности);
- при рождении имеют массу тела ниже нормы;
- имеют сниженный уровень железа в организме;
- медленнее развиваются и имеют сниженные умственные способности.
Синдром беспокойных ног. Появление синдрома беспокойных ног на фоне анемии называется вторичным синдромом беспокойных ног. Синдром беспокойных ног очень распространён, поражает нервную систему и вызывает непреодолимое желание постоянно шевелить ногами. Появляются неприятные ощущения в бёдрах, икрах и ступнях. Синдром беспокойных ног, причиной которого является анемия, лечится железосодержащими препаратами до нормализации запасов железа в организме [6] .
Диагностика анемии
К какому врачу обратиться
При подозрении на анемию следует обратиться к врачу-терапевту. При необходимости может потребоваться консультация врача-гематолога и врача-гастроэнтеролога.
Лабораторная диагностика анемий
Общими критериями лабораторной диагностики всех анемий в общем анализе крови при подсчёте «ручным» методом являются один или сразу несколько показателей:
- снижение концентрации гемоглобина (Нb менее 110 г/л);
- снижение количества эритроцитов (менее 3,8 х10*12 клеток/л );
- снижение цветового показателя (менее 0,85);
- сниженное или нормальное количество ретикулоцитов — предшественников эритроцитов (норма 10-20 %) в общем анализе крови.
Также могут быть морфологические изменения эритроцитов (изменение формы) — анизоцитоз (изменение размеров эритроцитов или лейкоцитов) и пойкилоцитоз (деформация формы красных кровяных телец). В общем анализе крови необходимо обратить внимание на появление незрелых гранулоцитов, что может говорить о всевозможных воспалительных, аллергических процессах, аутоиммунных заболеваниях, инфекциях, вызванных вирусами или бактериями.
При выполнении общего анализа крови на автоматическом гематологическом анализаторе изменяются нормы указанных выше показателей и ряд эритроцитарных индексов. Также в общем анализе крови выявляется:
- снижение среднего объёма эритроцита (MCV): менее 80 фл;
- снижение среднего содержания Нb в эритроците (МСН): менее 26 пг;
- снижение средней концентрации Нb в эритроците (MCHC): менее 320 г/л;
- повышение степени анизоцитоза эритроцитов (RDW): больше 14 %.
Изменения в биохимическом анализе крови определяются патогенезом анемии и могут включать:
- снижение концентрации сывороточного железа (менее 12,5 мкмоль/л);
- увеличение общей железосвязывающей способности сыворотки (более 69 мкмоль/л);
- снижение коэффициента насыщения трансферрина железом (менее 17 %);
- снижение концентрации ферритина в сыворотке крови (менее 30 нг/мл или мкг/л);
- снижение витамина В12 и фолиевой кислоты при В12-дефицитной анемии.
В дополнение появилась возможность определения растворимых трансферриновых рецепторов (рТФР), концентрация которых при дефиците железа повышается (более 2,9 мкг/мл).
Дифференциальный диагноз ЖДА
- Дефицитные анемии: фолиево-дефицитная анемия (D52), В12-дефицитная анемия (D51) (мегалобластные анемии);
- Анемии вследствие хронических неинфекционных заболеваний (D63.8). Мегалобластные анемии по лабораторным признакам:
- макроцитарная (MCV более 100 фл);
- развитие вторичных изменений из-за вовлечения в процесс других ростков кроветворения в виде лейкопении (снижения количества лейкоцитов), нейтропении (снижения количества нейтрофилов) и тромбоцитопении (снижения количества тромбоцитов);
- гиперсегментация ядер нейтрофилов;
- мегалобластный тип кроветворения, наличие в костном мозге крупных эритроидных клеток;
- снижение витамина В12 в сыворотке крови (норма 100-700 пг/мл) при В12-дефицитной анемии;
- уменьшение концентрации в сыворотке крови (норма 3-20 нг/мл) или содержания в эритроцитах фолиевой кислоты (норма 166-640 нг/мл) при фолиеводефицитной анемии [5] .
Лечение анемии
Лечение в первую очередь должно быть направлено на выявление и устранение первопричины, поэтому терапия анемий длится долго, зачастую сопровождается несколькими врачами-специалистами.
Показание к лечению
Показание для медикаментозного лечения — это снижение уровня гемоглобина менее 120 г/л у женщин и ниже 130 г/л у мужчин.
В основном лечение подразумевает восстановление запасов гемоглобина, увеличение количества эритроцитов, нормализацию гематокрита. Основным эффективным методом лечения железодефицитных анемий является применение препаратов железа внутрь или парентерально (внутривенно или внутримышечно).
Чтобы восстановить уровень гемоглобина у больного железодефицитной анемией нужно, чтобы доза двухвалентного железа в сутки (эффективно всасывается только оно) составляла 100-300 мг, учитывая истощённые запасы железа (около 1,5 г).
Эффективнее назначать препараты с более высоким содержанием двухвалентного железа, их нужно принимать перорально (через рот) 1-2 раза в сутки. Для больных это самый удобный подход, следовательно, увеличивается их приверженность к терапии. В состав многих лекарственных форм железа входит аскорбиновая и янтарная кислоты, фруктоза, цистеин и др., они помогают наилучшему всасыванию железа в желудочно-кишечном тракте. Препараты железа лучше всего переносятся, если принимать их с пищей.
Лечение железодефицитной анемии парентеральными формами препаратов железа
Существуют чёткие показания для такой терапии:
- при нарушенном всасывании из кишечника (синдром недостаточности всасывания, резекция тонкой кишки, энтериты и др.);
- обострение хронических заболеваний желудочно-кишечного тракта, таких как язвенная болезнь желудка или двенадцатиперстной кишки, болезнь Крона, неспецифический язвенный колит;
- плохая переносимость железосодержащих препаратов при приёме внутрь;
- при необходимости быстрого восполнения запасов железа в организме.
С целью парентерального введения используют препараты железа, такие как «Феринжект» (вутривенно) «Эктофер» (внутримышечно), «Фербитол» (внутримышечно), «Феррум Лек» (внутримышечно, внутривенно), «Ферковен»(внутривенно) [2] .
Относительно лечения послеродовой анемии нет чётких выводов о методах. Согласно исследованиям, пероральный приём железа не имеет существенного преимущества по сравнению с внутривенным введением железа или плацебо. Однако пероральное употребление железа не приводит к развитию опасных для жизни аллергических реакций, как внутривенное введение железа. Клиническое значение переливания крови остаётся неопределённым, в частности из-за имеющихся рисков. Этот метод можно использовать при лечении послеродовой анемии в случае острого или сильного кровотечения во время родов. Однако он не рекомендуется после небольших и умеренных кровотечений у стабильных пациентов с лёгкой или бессимптомной анемией. В любом случае необходимо оценить степень тяжести анемии и рассмотреть применение диеты, богатой железом, в качестве метода профилактики и дополнения к лечению [7] .
Железодефицитная анемия — самый распространённый тип анемии. Однако лечение других типов малокровия отличается от лечения ЖДА. При других разновидностях анемии для нормализации показателей крови необходимо, например, восполнять запасы витамина В12, фолиевой кислоты, контролировать сопутствующие хронические заболевания и другие факторы, которые явились первопричиной анемии. Для этого необходимо своевременное обращение к врачу, который займётся диагностикой и определением тактики ведения.
Как улучшить лечение. Диета
В пищевой рацион при всех видах анемий следует добавить употребление продуктов с высоким содержанием железа: свиная и говяжья печень, телятина, говядина, гречневая крупа, зеленые яблоки, гранаты, грибы, капуста, фасоль и другие бобовые, горький шоколад и др.

Питаться нужно 4-6 раз в день. Для нормального переваривания еда должна быть комнатной температуры, слишком холодная или слишком горячая пища раздражают слизистую желудка, что препятствуют всасыванию полезных элементов. Количество выпитой воды в день — 30 мл на 1 кг веса, включая чай, сок, суп и т. д. Категорически запрещёно принимать алкоголь и курить. Алкоголь не только негативно сказывается на здоровье ЖКТ, но и вымывает полезные компоненты с мочой, что вредно даже для здоровых людей. Курение повышает кислотность желудка, что может спровоцировать развитие гастрита или язвы. В этом случае нарушится всасывание полезных микроэлементов.
При железодефицитной анемии необходимо включить ферментированные продукты питания (кефир, квас, квашеная капуста и др.). Кислота, содержащаяся в таких продуктах, легко вступает в контакт с железом и не даёт образоваться плохо всасывающимся фитатам железа, вследствие чего улучшается проникновение железа в энтероциты (клетки, выстилающие внутреннюю поверхность кишечника). Образование фитатов железа также уменьшается, если растительные продукты измельчить или подвергнуть термической обработке [10] .
Ежедневные курсовые добавки железа у менструирующих женщин являются эффективной клинической стратегией здравоохранения для облегчения анемии и устранения дефицита железа, а также для увеличения запасов гемоглобина и железа. Ежедневное добавление железа также улучшает физическую работоспособность у женщин. Кроме того, имеются данные о том, что добавление железа снижает усталость [8] .
Беременным женщинам рекомендуются ежедневные пероральные добавки железа и фолиевой кислоты: 30-60 мг элементарного железа и 400 мкг (0,4 мг) фолиевой кислоты для предотвращения малокровия, послеродового сепсиса, преждевременных родов и низкого веса ребёнка при рождении [9] .
Противопоказания при анемии
При анемии противопоказаны жёсткие диеты, рацион питания должен включать продукты с высоким содержанием железа, витамина В12 и фолиевой кислоты. Также развитие анемии возможно на фоне приёма некоторых лекарств (противоопухолевые, ряд антибактериальных, противопротозойных, противовирусных, противовоспалительных, противоревматических, противоэпилептических и антипсихотических препаратов). Поэтому приём данной группы лекарств при анемии должен проходить под контролем специалиста.
Можно ли лечить анемию народными средствами
На сегодняшний день эффективных народных средств лечения анемии не существует, потому что коррекция дефицита железа не может быть достигнута только изменением питания или использованием каких-либо трав, отваров и соков. Причина этого состоит в том, что усвоение железа из пищи ограничено (не более 3-5 % из растительной пищи), а в лекарственных препаратах оно содержится в большей концентрации.
Прогноз. Профилактика
Прогноз
Для прогноза играет важную роль причина анемии. Ранняя диагностика и быстрое определение тактики ведения постгеморрагической анемии напрямую связано с хорошим прогнозом.
Если анемия связана с дефицитом железа, витамина В12 или фолиевой кислоты, нужно дополнение диеты продуктами питания, богатыми данными микроэлементами и витаминами. Более плохой прогноз касается анемий, которые появились вследствие онкологических заболеваний, в том числе кроветворных органов, либо генетических нарушений, так как они плохо поддаются лечению.
Профилактика
Профилактика анемии включает в себя регулярные осмотры у терапевта со сдачей анализов, своевременное выявление и лечение хронических заболеваний, в том числе выявление и лечение источника хронической кровопотери (язвенные заболевания внутренних органов, геморрой и т. д.).
Для профилактики анемии, как и для лечения, важно наличие в рационе продуктов с высоким содержанием железа, витамина В12 и фолиевой кислоты.
Анемия (малокровие)
Информация, представленная на странице, не должна быть использована для самолечения или самодиагностики. При подозрении на наличие заболевания, необходимо обратиться за помощью к квалифицированному специалисту. Провести диагностику и назначить лечение может только ваш лечащий врач.
Содержание статьи:

Что такое анемия (малокровие)?
Нередко можно встретить не совсем корректное определение того, что анемия – это малокровие. Хотя сам термин именно таким образом переводится с латыни, но если быть точными, то при анемии страдает количество эритроцитов и(ли) гемоглобина, а не всей крови в целом. Только при острых кровопотерях в результате массивного кровотечения с развитием постгеморрагической анемии на небольшой временной промежуток общий объем крови может снижаться, но он быстро восполняется плазмой.
Что такое анемия
Согласно современным представлениям анемией называют патологическое состояние, при котором происходит снижение уровня эритроцитов (красных клеток крови) и гемоглобина. В результате страдает доставка в ткани кислорода, из-за чего развивается тканевая гипоксия. Анемия обычно возникает как результат различных патологий, считается одним из проявлений различных заболеваний. Анемией у мужчин считают снижение гемоглобина менее 120г/л, у женщин менее 110 г/л.
Причины возникновения
Развитие анемии связано с нарушением образования новых эритроцитов, усилением разрушения красных клеток или повышенных потерь эритроцитов при кровотечениях. По данным статистики среди ведущих причин анемии выделяют потери крови. Они могут быть как острыми, при одномоментной потере крови более 500-800 мл, так и хроническими, если кровь теряется ежедневно небольшими порциями.
Острые кровопотери провоцируются ранениями, носовым, маточным, пищеводным кровотечением, потерей крови, которая вытекает из стенки кишечника, сосудов в грудной и брюшной полости.
Хронические потери крови возможны при язвенном поражении желудка и кишечника, геморрое, после гемодиализа, при патологиях репродуктивной сферы с обильными менструациями. Постоянные кровопотери истощают запасы железа в организме, его поступает меньше, чем расходуется. Как результат страдает синтез гемоглобина, его уровень снижается.
Железодефицит может возникнуть при проблемах всасывания, если есть воспалительные патологии кишечника, удалена его часть, выявлены опухоли. Анемия возможна при уменьшении в крови белков, которые переносят железо в костный мозг – это патологии почек, проблемы печени, голодание, нарушение всасывания белка. У детей раннего возраста анемия возможна в силу того, что их организм не смог накопить достаточно железа, поскольку не получал его из тела матери. В этом случае проблема возникает в первые месяцы после рождения.
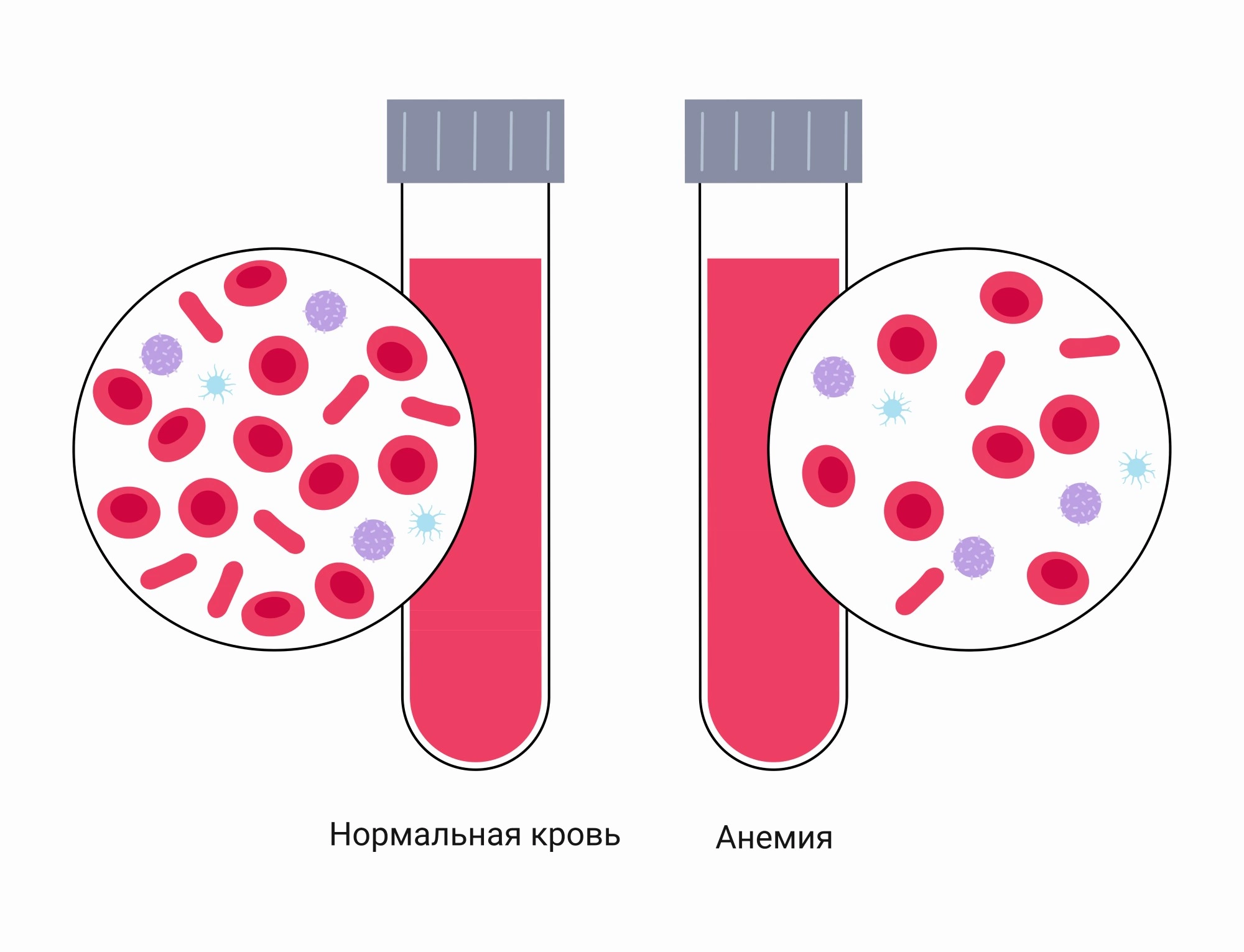
Возможно развитие анемии из-за нарушения процесса кроветворения – образования новых клеток костным мозгом. Это бывает не только при дефиците железа, но и соединений, которые участвуют в процессе образования эритроцитов. Среди основных можно выделить нехватку витаминов В6 и В12, фолиевой кислоты, меди.
Уменьшение выработки эритроцитов возможно при повреждении костного мозга. Чаще всего стволовые клетки, из которых образуются эритроциты, повреждаются различными токсическими соединениям, облучением, в костном мозге образуются метастазы, повреждающие костный мозг и приводящие к нарушению кроветворения. Проблемы с образованием гемоглобина и эритроцитов возможны, если страдает синтез белка глобина, снижается синтез гормонов – эритропоэтинов, которые стимулируют активность костного мозга.
Анемии, которые возникают в силу усиленного разрушения эритроцитов – гемолитические возможны в результате наследования дефектов мембран клеток, воздействия различных гемолитических ядов или иммунных реакций. Наследственные гемолитические анемии связаны с нарушением работы особых ферментов, отвечающих за стабильность оболочки эритроцита, изменениями в структуре гемоглобина, расстройством процесса его синтеза, дефектами в самих мембранах.
Приобретенный гемолиз возможен при отравлениях химическими и биологическими ядами, дефиците витаминов, механических повреждениях оболочек, реакциях – «антиген-антитело» при переливании крови или аллергии.
Классификация

Симптоматика любых анемий в первую очередь обусловлена кислородным голоданием тканей. Поэтому независимо от причин малокровия, признаки разных видов анемии будут схожими, а их интенсивность – варьироваться в зависимости от степени тяжести болезни.
Лучше понимать, что это за болезнь, помогает классификация, основанная на целом ряде факторов. По происхождению анемии можно разделить на:
- гемолитические – возникают в результате активного массированного разрушения мембран эритроцитов;
- постгеморрагические – возникают в результате потери крови при различных видах кровотечений;
- апластические – связаны с подавлением активности костного мозга по созданию новых клеток крови;
- дефицитные – возникают из-за нехватки железа, витаминов, микроэлементов, белков.
В зависимости от уровня гемоглобина выделяют анемии трех степеней тяжести. Это разделение важно для планирования лечения и тактики оказания первой помощи:
- легкая анемия – снижение гемоглобина в пределах 110-90 г/л;
- средней тяжести – показатели уменьшены до 90-70 г/л;
- тяжелая анемия – менее 70 г/л.
По размеру эритроцитов, который определяют при изучении их морфологии, выделяются:
- микроцитарные анемии (клетки меньше, чем обычно, могут иметь обычную или измененную форму);
- нормоцитарные состояния – размеры эритроцитов не изменяются, страдает их общее количество, уровень гемоглобина.
- макроцитарные (вплоть до мегалоцитов) – размеры красных клеток увеличены, они могут иметь неправильную форму.
По цветовому показателю (он отражает насыщение эритроцитов гемоглобином) можно выделить:
- гипохромную анемию, когда цветовой показатель снижен менее 0,8 единиц;
- нормохромную с ЦП в пределах от 0,8 до 1,05;
- гиперхромную анемию с превышением ЦП более 1,06.
По течению процесса можно выделить острую анемию и хроническую. Это разделение характерно для постгеморрагических видов болезни.
Симптомы
Среди всех вариантов преобладает железодефицитная анемия, хотя проявления и признаки ее похожи на многие другие формы (за исключением некоторых специфических признаков, типичных для каждой отдельной формы). Среди общих проявлений можно выделить:
- бледность кожи, при выраженных формах болезни приобретающая восковой или серо-землистый оттенок;
- слабость, которая возникает с самого утра, не зависит от тяжести нагрузок, почти не проходит;
- повышенную утомляемость от привычных дел, постоянную сонливость;
- головокружения и приступы обмороков, частое потемнение в глазах;
- шум, зуммер, писк в ушах, постоянно мелькающие мушки перед глазами;
- сердцебиение при малейших нагрузках, одышку, учащение пульса.
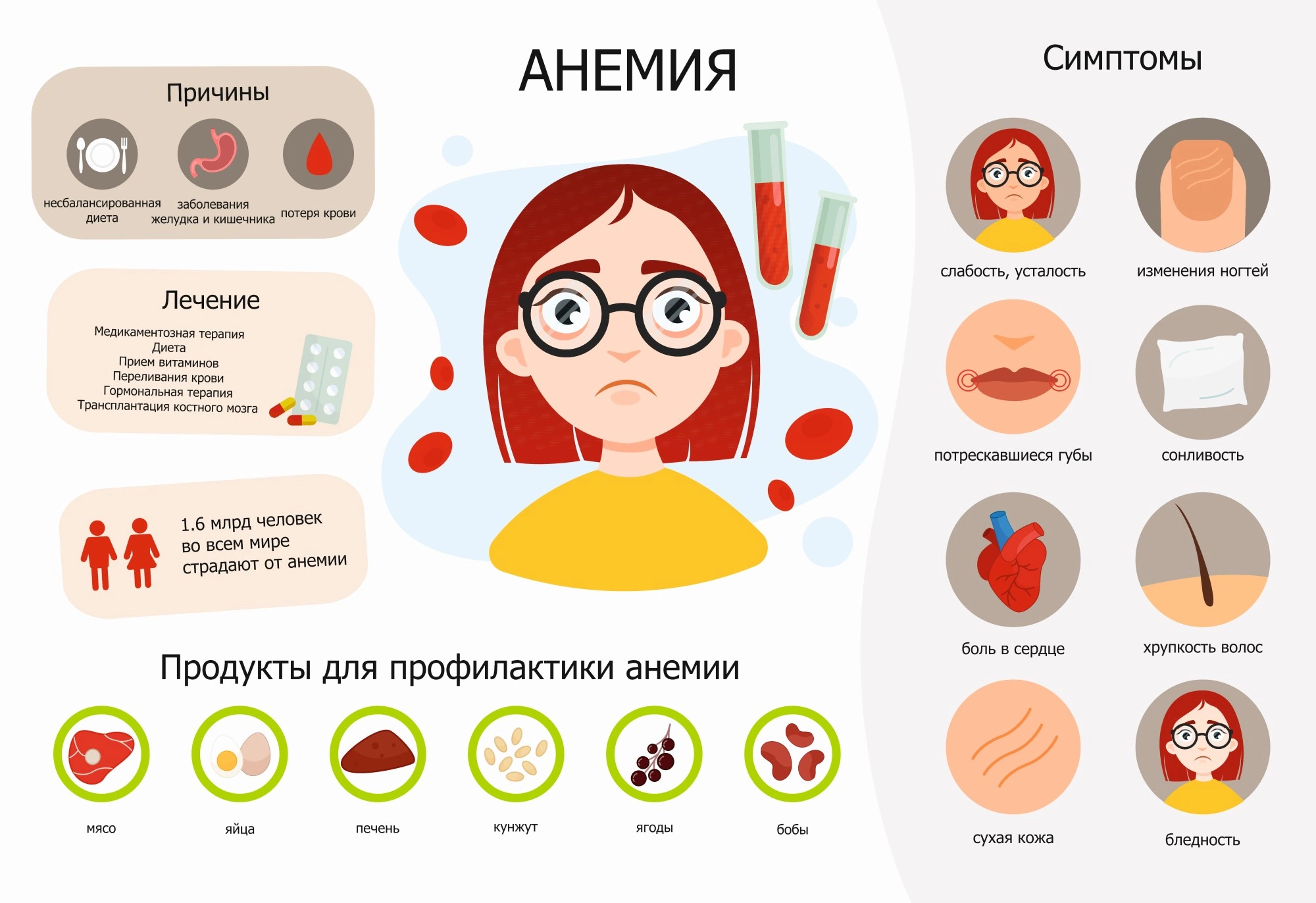
При легких анемиях эти признаки выражены слабо или совсем не определяются, при медленном развитии анемии тело адаптируется к снижению гемоглобина, симптомы могут быть смазанными. В зависимости от конкретной причины анемии, есть и ряд специфических проявлений у каждого вида болезни.
На ранней стадии железодефицитной анемии, в период скрытого дефицита железа и сидеропении, никаких жалоб может не быть. Проблемы определяет только лабораторное тестирование. По мере развития дефицитного состояния могут возникать:
- сильная сухость кожных покровов, мелкие повреждения кожи, растрескивание,
- ломкость ногтей, проблемы волос (сухость, ломкость, тусклость);
- заеды в углах рта;
- слабость мышц;
- ощущение жжения в языке, нарушение вкуса (желание есть землю, мел, сырые крупы или мясо);
- пристрастие к резким сильным запахам.
Кроме того, при анемии с дефицитом железа возможны поражения пищеварительного тракта, развитие гастритов.
При анемии, которая возникает при нехватке витамина В12, возможны серьезные поражения пищеварительной системы в форме атрофического гастрита и неврологические проявления. Обычно это парестезии, нарушения чувствительности в ногах или руках, онемение в конечностях. При выраженной анемии могут возникать расстройства психики – галлюцинации, бред, слабоумие. На фоне дефицита витамина В9 (фолиевой кислоты) симптомы похожи на предыдущую форму, но практически нет неврологической симптоматики, редко бывает глоссит. Нехватка фолатов формирует обострение шизофрении, частые приступы эпилепсии.
При гемолитической анемии возможна желтизна кожи и слизистых оболочек, размер селезенки увеличивается, могут образовываться камни в желчном пузыре. Если возникает сильный гемолиз эритроцитов (разрушение), помимо анемии, развития желтухи и нарушения общего состояния возникает тошнота с рвотой, проблемы с сознанием, судороги, острая почечная недостаточность, проблемы с сосудами.
Апластическая анемия возникает на фоне подавления работы костного мозга, возникают кровоизлияния. Они обычно появляются в области голеней и живота, бедер, в областях введения лекарств. Часто возникают пневмонии или бронхиты.
Чем опасна анемия: ключевые осложнения
В зависимости от вида анемии последствия могут существенно различаться. Среди основных проблем различают хроническую усталость с общей слабостью, сонливостью, упадком сил и рассеянностью, трудностями при выполнении повседневных дел и занятий спортом.
Нарушения иммунной системы связаны с влиянием гипоксии на иммунную систему. Это делает людей более восприимчивыми к хроническим инфекциям.
Тяжелые анемии повышают риск осложнений со стороны сердца, сосудов и респираторного тракта, могут возникать аритмии и недостаточность сердца.
Анемия может серьезно ухудшить состояние при беременности: возможно нарушение внутриутробного развития плода, проблемы в родах и после них. Также возможна послеродовая депрессия, могут быть недоношенность, сниженная масса тела и анемии младенцев.
На фоне анемии возможно развитие синдрома беспокойных ног – это связано с поражением нервной системы, что ведет к тому, что нужно постоянно шевелить ногами. Проблема лечится приемом препаратов железа.
Диагностика разных форм анемии
Первым этапом диагностики является общий анализ крови. В нем определяют уровень эритроцитов, гемоглобина, цветовой показатель и гематокрит. Помимо них, современные анализаторы определяют размеры эритроцитов, распределяя их в процентном соотношении. Кроме того, определяют уровень ретикулоцитов, оценивают лейкоцитарную формулу и уровень СОЭ, количество тромбоцитов.
Дополнительно сдают еще ряд анализов — оценить количество железа в сыворотке, биохимические показатели, количество витаминов в плазме, уровень билирубина, коагулограмму. Для полной картины нужно провести УЗИ брюшной полости и щитовидки, рентген грудной клетки, ЭКГ. Если есть подозрения на апластическую анемию, проводится пункция костного мозга.
Лечение
Согласно клиническим рекомендациям определяется тактика ведения пациента, и подбираются препараты для коррекции анемии. В зависимости от вида анемии врачи определяют, как лечить, составлять диету и подбирать продукты.
Назначают препараты железа через рот, курс рассчитывается по уровню гемоглобина. Эффективность терапии оценивается по результатам контрольных анализов крови. При неэффективности или непереносимости пероральных препаратов назначают введение препаратов железа внутривенно. В некоторых случаях дополняют лечение инъекциями витамина В12, поливитаминами, стимуляторами эритропоэза.
Одна диета не может вылечить анемию, но продукты, богатые железом и аскорбиновой кислотой, правильно составленный рацион улучшают усвоение, усиливают всасывание железа. Полезны мясные продукты, салаты из овощей, свежие фрукты.
Профилактика
Для предотвращения анемии необходимо регулярно посещать врача, сдавать анализы крови, своевременно лечить все хронические заболевания, сопровождающиеся потерей крови. В рацион важно включать красное мясо, субпродукты, свежие овощи.
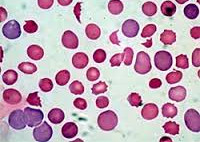
Гемолитическая анемия
Гемолитическая анемия – патология эритроцитов, отличительным признаком которой является ускоренное разрушение красных кровяных телец с высвобождением повышенного количества непрямого билирубина. Для данной группы заболеваний типично сочетание анемического синдрома, желтухи и увеличения размеров селезенки. В процессе диагностики исследуется общий анализ крови, уровень билирубина, анализ кала и мочи, УЗИ органов брюшной полости; проводится биопсия костного мозга, иммунологические исследования. В качестве методов лечения используется медикаментозная, гемотрансфузионная терапия; при гиперспленизме показана спленэктомия.
МКБ-10


Общие сведения
Гемолитическая анемия (ГА) — малокровие, обусловленное нарушением жизненного цикла эритроцитов, а именно преобладанием процессов их разрушения (эритроцитолиза) над образованием и созреванием (эритропоэзом). Данная группа анемий очень обширна. Их распространенность неодинакова в различных географических широтах и возрастных когортах; в среднем патология встречается у 1% населения. Среди прочих видов анемий на долю гемолитических приходится 11%. Патология характеризуется укорочением жизненного цикла эритроцитов и их распадом (гемолизом) раньше времени (через 14-21 день вместо 100-120 суток в норме). При этом разрушение эритроцитов может происходить непосредственно в сосудистом русле (внутрисосудистый гемолиз) или в селезенке, печени, костном мозге (внесосудистый гемолиз).

Причины
Этиопатогенетическую основу наследственных гемолитических синдромов составляют генетические дефекты мембран эритроцитов, их ферментных систем либо структуры гемоглобина. Данные предпосылки обусловливают морфофункциональную неполноценность эритроцитов и их повышенное разрушение. Гемолиз эритроцитов при приобретенных анемиях наступает под влиянием внутренних факторов или факторов окружающей среды, среди которых:
- Аутоиммунные процессы. Образование антител, агглютинирующих эритроциты, возможно при гемобластозах (остром лейкозе, хроническом лимфолейкозе, лимфогранулематозе), аутоиммунной патологии (СКВ, неспецифическом язвенном колите), инфекционных заболеваниях (инфекционном мононуклеозе, токсоплазмозе, сифилисе, вирусной пневмонии). Развитию иммунных гемолитических анемий могут способствовать посттрансфузионные реакции, профилактическая вакцинация, гемолитическая болезнь плода.
- Токсическое действие на эритроциты. В ряде случаев острому внутрисосудистому гемолизу предшествует отравление мышьяковистыми соединениями, тяжелыми металлами, уксусной кислотой, грибными ядами, алкоголем и др. Вызывать разрушение клеток крови может прием определенных лекарств (противомалярийных препаратов, сульфаниламидов, производных нитрофуранового ряда, анальгетиков).
- Механическое повреждение эритроцитов. Гемолиз эритроцитов может наблюдаться при тяжелых физических нагрузках (длительной ходьбе, беге, лыжном переходе), при ДВС-синдроме, малярии, злокачественной артериальной гипертензии, протезировании клапанов сердца и сосудов, проведении гипербарической оксигенации, сепсисе, обширных ожогах. В этих случаях под действием тех или иных факторов происходит травматизация и разрыв мембран изначально полноценных эритроцитов.

Патогенез
Центральным звеном патогенеза ГА является повышенное разрушение эритроцитов в органах ретикулоэндотелиальной системы (селезенке, печени, костном мозге, лимфатических узлах) или непосредственно в сосудистом русле. При аутоиммунном механизме анемии происходит образование антиэритроцитарных АТ (тепловых, холодовых), которые вызывают ферментативный лизис мембраны эритроцитов. Токсические вещества, являясь сильнейшими окислителями, разрушают эритроцит за счет развития метаболических, функциональных и морфологических изменений оболочки и стромы красных кровяных телец. Механические факторы оказывают прямое воздействие на клеточную мембрану. Под влиянием этих механизмов из эритроцитов выходят ионы калия и фосфора, а внутрь поступают ионы натрия. Клетка разбухает, при критическом увеличении ее объема наступает гемолиз. Распад эритроцитов сопровождаются развитием анемического и желтушного синдромов (так называемой «бледной желтухой»). Возможно интенсивное окрашивание кала и мочи, увеличение селезенки и печени.
Классификация
В гематологии гемолитические анемии подразделяются на две большие группы: врожденные (наследственные) и приобретенные. Наследственные ГА включают следующие формы:
- эритроцитарные мембранопатии (микросфероцитоз – болезнь Минковского-Шоффара, овалоцитоз, акантоцитоз) – анемии, обусловлены структурными аномалиями мембран эритроцитов
- ферментопении (энзимопении) – анемии, вызванные дефицитом тех или иных ферментов (глюкозо-6-фосфатдегидрогеназы, пируваткиназы и др.)
- гемоглобинопатии— анемии, связанные с качественными нарушениями структуры гемоглобина или изменением соотношения его нормальных форм (талассемия, серповидно-клеточная анемия).
Приобретенные ГА подразделяются на:
- мембранопатии приобретенные (пароксизмальная ночная гемоглобинурия – б-нь Маркиафавы-Микели, шпороклеточная анемия)
- иммунные (ауто- и изоиммунные) – обусловлены воздействием антител
- токсические – анемии, обусловленные воздействием химических веществ, биологических ядов, бактериальных токсинов
- механические — анемии, вызванные механическим повреждением структуры эритроцитов (тромбоцитопеническая пурпура, маршевая гемоглобинурия)
Симптомы
Наследственные мембранопатии, ферментопении и гемоглобинопатии
Наиболее распространенной формой данной группы анемий является микросфероцитоз, или болезнь Минковского-Шоффара. Наследуется по аутосомно-доминантному типу; обычно прослеживается у нескольких представителей семьи. Дефектность эритроцитов обусловлена дефицитом в мембране актомиозиноподобного белка и липидов, что приводит к изменению формы и диаметра эритроцитов, их массивному и преждевременному гемолизу в селезенке. Манифестация микросфероцитарной ГА возможна в любом возрасте (в младенчестве, юношестве, старости), однако обычно проявления возникают у детей старшего возраста и подростков. Тяжесть заболевания варьирует от субклинического течения до тяжелых форм, характеризующихся часто повторяющимися гемолитическими кризами. В момент криза нарастает температура тела, головокружение, слабость; возникают боли в животе и рвота.
Основным признаком микросфероцитарной гемолитической анемии служит желтуха различной степени интенсивности. Вследствие высокого содержания стеркобилина кал становится интенсивно окрашенным в темно-коричневый цвет. У пациентов с болезнь Минковского-Шоффара наблюдается склонность к образованию камней в желчном пузыре, поэтому часто развиваются признаки обострения калькулезного холецистита, возникают приступы желчной колики, а при закупорке холедоха конкрементом — обтурационная желтуха. При микросфероцитозе во всех случаях увеличена селезенка, а у половины пациентов – еще и печень. Кроме наследственной микросфероцитарной анемии, у детей часто встречаются другие врожденные дисплазии: башенный череп, косоглазие, седловидная деформация носа, аномалии прикуса, готическое нёбо, полидактилия или брадидактилия и пр. Пациенты среднего и пожилого возраста страдают трофическими язвами голени, которые возникают в результате гемолиза эритроцитов в капиллярах конечностей и плохо поддаются лечению.
Энзимопенические анемии связаны с недостатком определенных ферментов эритроцитов (чаще — Г-6-ФД, глутатион-зависимых ферментов, пируваткиназы и др). Гемолитическая анемия может впервые заявлять о себе после перенесенного интеркуррентного заболевания или приема медикаментов (салицилатов, сульфаниламидов, нитрофуранов). Обычно заболевание имеет ровное течение; типична «бледная желтуха», умеренная гепатоспленомегалия, сердечные шумы. В тяжелых случаях развивается ярко выраженная картина гемолитического криза (слабость, рвота, одышка, сердцебиение, коллаптоидное состояние). В связи с внутрисосудистым гемолизом эритроцитов и выделением гемосидерина с мочой последняя приобретает темный (иногда черный) цвет. Особенностям клинического течения гемоглобинопатий — талассемии и серповидно-клеточной анемии посвящены самостоятельные обзоры.
Приобретенные гемолитические анемии
Среди различных приобретенных вариантов чаще других встречаются аутоиммунные анемии. Для них общим пусковым фактором выступает образование антител к антигенам собственных эритроцитов. Гемолиз эритроцитов может носить как внутрисосудистый, так и внутриклеточный характер. Гемолитический криз при аутоиммунной анемии развивается остро и внезапно. Он протекает с лихорадкой, резкой слабостью, головокружением, сердцебиением, одышкой, болями в эпигастрии и пояснице. Иногда острым проявлениям предшествуют предвестники в виде субфебрилитета и артралгий. В период криза стремительно нарастает желтуха, не сопровождающаяся кожным зудом, увеличивается печень и селезенка. При некоторых формах аутоиммунных анемий больные плохо переносят холод; в условиях низких температур у них может развиваться синдром Рейно, крапивница, гемоглобинурия. Вследствие недостаточности кровообращения в мелких сосудах возможны осложнения в виде гангрены пальцев ног и рук.
Токсические анемии протекают с прогрессирующей слабостью, болями в правом подреберье и поясничной области, рвотой, гемоглобинурией, высокой температурой тела. Со 2-3 суток присоединяется желтуха и билирубинемия; на 3-5 сутки возникает печеночная и почечная недостаточность, признаками которых служат гепатомегалия, ферментемия, азотемия, анурия. Отдельные виды приобретенных гемолитических анемий рассмотрены в соответствующих статьях: «Гемоглобинурия» и «Тромбоцитопеническая пурпура», «Гемолитическая болезнь плода».
Осложнения
Каждый вид ГА имеет свои специфические осложнения: например, ЖКБ – при микросфероцитозе, печеночная недостаточность – при токсических формах и т.д. К числу общих осложнений относятся гемолитические кризы, которые могут провоцироваться инфекциями, стрессами, родами у женщин. При остром массивном гемолизе возможно развитие гемолитической комы, характеризующейся коллапсом, спутанным сознанием, олигурией, усилением желтухи. Угрозу жизни больного несут ДВС-синдром, инфаркт селезенки или спонтанный разрыв органа. Неотложной медицинской помощи требуют острая сердечно-сосудистая и почечная недостаточность.
Диагностика
Определение формы ГА на основе анализа причин, симптоматики и объективных данных относится к компетенции гематолога. При первичной беседе выясняется семейный анамнез, частота и тяжесть протекания гемолитических кризов. В процессе осмотра оценивается окраска кожных покровов, склер и видимых слизистых, производится пальпация живота для оценки величины печени и селезенки. Сплено- и гепатомегалия подтверждается при проведении УЗИ печени и селезенки. Лабораторный диагностический комплекс включает:
- Исследование крови. Изменения в гемограмме характеризуются нормо- или гипохромной анемией, лейкопенией, тромбоцитопенией, ретикулоцитозом, ускорением СОЭ. В биохимических пробах крови определяется гипербилирубинемия (увеличение фракции непрямого билирубина), увеличение активности лактатдегидрогеназы. При аутоиммунных анемиях большое диагностическое значение имеет положительная проба Кумбса.
- Анализы мочи и кала. Исследование мочи выявляет протеинурию, уробилинурию, гемосидеринурию, гемоглобинурию. В копрограмме повышено содержание стеркобилина.
- Миелограмму. Для цитологического подтверждения выполняется стернальная пункция. Исследование пунктата костного мозга обнаруживает гиперплазию эритроидного ростка.
В процессе дифференциальной диагностики исключаются гепатиты, цирроз печени, портальная гипертензия, гепатолиенальный синдром, порфирии, гемобластозы. Пациента консультируют гастроэнтеролог, клинический фармаколог, инфекционист и другие специалисты.

Лечение
Различные формы ГА имеют свои особенности и подходы к лечению. При всех вариантах приобретенной гемолитической анемии необходимо позаботиться об устранении влияния гемолизирующих факторов. Во время гемолитических кризов больным необходимы инфузии растворов, плазмы крови; витаминотерапия, по необходимости – гормоно- и антибиотикотерапия. При микросфероцитозе единственно эффективным методом, приводящим к 100 % прекращению гемолиза, является спленэктомия.
При аутоиммунной анемии показана терапия глюкокортикоидными гормонами (преднизолоном), сокращающая или прекращающая гемолиз. В некоторых случаях требуемый эффект достигается назначением иммунодепрессантов (азатиоприна, 6-меркаптопурина, хлорамбуцила), противомалярийных препаратов (хлорохина). При резистентных к медикаментозной терапии формах аутоиммунной анемии выполняется спленэктомия. Лечение гемоглобинурии предполагает переливание отмытых эритроцитов, плазмозаменителей, назначение антикоагулянтов и антиагрегантов. Развитие токсической гемолитической анемии диктует необходимость проведения интенсивной терапии: дезинтоксикации, форсированного диуреза, гемодиализа, по показаниям – введение антидотов.
Прогноз и профилактика
Течение и исход зависят от вида анемии, тяжести протекания кризов, полноты патогенетической терапии. При многих приобретенных вариантах устранение причин и полноценное лечение приводит к полному выздоровлению. Излечения врожденных анемий добиться нельзя, однако возможно достижение длительной ремиссии. При развитии почечной недостаточности и других фатальных осложнений прогноз неблагоприятен. Предупредить развитие ГА позволяет профилактика острых инфекционных заболеваний, интоксикаций, отравлений. Запрещается бесконтрольное самостоятельное использование лекарственных препаратов. Необходимо тщательная подготовка пациентов к гемотрансфузиям, вакцинации с проведением всего комплекса необходимых обследований.
4. Клинические рекомендации по диагностике и лечению аутоиммунных гемолитический анемий/ Цветаева Н.В., Никулина О.Ф. — 2014.
Источник https://probolezny.ru/anemiya/
Источник https://www.smclinic-spb.ru/doctor/gematolog/zabolevania/1439-anemiya-malokrovie
Источник https://www.krasotaimedicina.ru/diseases/hematologic/hemolytic-anemia