Лечение хронического эндометрита в прегравидарной подготовке женщин с невынашиванием беременности
Сайт издательства «Медиа Сфера»
содержит материалы, предназначенные исключительно для работников здравоохранения. Закрывая это сообщение, Вы подтверждаете, что являетесь дипломированным медицинским работником или студентом медицинского образовательного учреждения.
- Издательство «Медиа Сфера»
- (бесплатный номер по вопросам подписки)
пн-пт с 10 до 18
- Издательство «Медиа Сфера»
а/я 54, Москва, Россия, 127238
- Издательство
- «Медиа Сфера»
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Оптимизация ведения пациенток с привычным невынашиванием беременности и хроническим эндометритом на этапе прегравидарнойподготовки
Журнал: Российский вестник акушера-гинеколога. 2017;17(5): 29‑34
Аршакян А.К., Зароченцева Н.В., Титченко Ю.П., Меньшикова Н.С. Оптимизация ведения пациенток с привычным невынашиванием беременности и хроническим эндометритом на этапе прегравидарнойподготовки. Российский вестник акушера-гинеколога. 2017;17(5):29‑34.
Arshakian AK, Zarochentseva NV, Titchenko IuP, Men’shikova NS. Optimization of the management of patients with recurrent miscarriage and chronic endometritis at the stage of pregravid preparation. Russian Bulletin of Obstetrician-Gynecologist. 2017;17(5):29‑34. (In Russ.)
https://doi.org/10.17116/rosakush201717529-34
Цель исследования — определение вирусных агентов в эндометрии у пациенток с привычным невынашиванием беременности и хроническим эндометритом и возможности улучшения репродуктивного прогноза у данных пациенток на фоне применения противовирусной иммуномодулирующей терапии. Материал и методы. Под наблюдением находились 50 пациенток с привычным невынашиванием беременности и хроническим эндометритом в возрасте от 21 года до 39 лет. Всем пациенткам проведены клинико-диагностическое обследование, бактериологическое исследование микрофлоры влагалища, цервикального канала и полости матки, диагностика урогенитальных инфекций методом полимеразной цепной реакции, ультразвуковое исследование с допплеровским картированием, гистологическое исследование биоптатов эндометрия. Результаты. Выявлена высокая частота инфекций, передаваемых половым путем, и вирусных инфекций (герпетическая, цитомегаловирусная и папилломавирусная). Бактериологический контроль в подгруппе пациенток, получавших наряду с антибиотикотерапией иммуномодулирующий препарат на основе аллоферона-альфа, выявил 100% эрадикацию бактериальной микрофлоры и снижение вирусной нагрузки до клинически незначимых уровней. Заключение. Применение противовирусного иммуномодулирующего препарата на основе аллоферона-альфа в комплексе с антибактериальной терапией у пациенток с хроническим эндометритом и привычным невынашиванием беременности достоверно в большем проценте наблюдений ведет к благоприятному исходу лечения.
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Хроническое воспаление эндометрия (хронический эндометрит — ХЭ) — одно из часто встречающихся, но не всегда верно и вовремя диагностируемых заболеваний репродуктивной системы. При этом частота невынашивания беременности, которое нередко бывает как причиной, так и его следствием, стабильно высокая и составляет 15—25% исходов всех беременностей, по данным ВОЗ. Несмотря на полиэтиологичность, одним из основных факторов привычного невынашивания беременности являются персистирующая вирусная и бактериальная инфекции [1—5]. Недооценка роли микробного агента, как одного из ведущих причин ХЭ, вводит в заблуждение клиницистов и не способствует эффективному лечению [6—8]. Циркулируя в эндометрии, микробные агенты вызывают аутоиммунное воспаление эндометрия. Согласно отечественным исследованиям [3, 9, 10], распространенность ХЭ у пациенток с бесплодием и невынашиванием беременности колеблется от 1 до 70%. Такой разброс обусловлен как отсутствием единой концепции построения морфологического диагноза, так и несостоятельностью существующих диагностических тест-систем. Проведенное итальянскими учеными в марте 2008 г. исследование с участием 2190 женщин с различной патологией репродуктивной системы, включая бесплодие, внематочную беременность, аномальные маточные кровотечения, выявило ХЭ у 438 (20%) пациенток [11].
Современные ученые склоняются к мнению, что основным «виновником» любого воспаления является такая белковая единица, как инфламмасома. Инфламмасомы возбуждаются при увеличении капсазы-1, вызывают образование провоспалительных цитокинов и тем самым обеспечивают воспалительный ответ [12].
В развитии нарушений генеративной функции немаловажную роль играют иммунологические изменения в организме на фоне хронического воспаления, такие как увеличение количества макрофагов в эндометрии, медиаторный и клеточный дисбаланс в эндометрии. Поэтому применение противовирусных иммуномодулирующих препаратов при лечении данных больных является доказанной необходимостью.
Цель исследования — определение вирусных агентов в эндометрии у пациенток с привычным невынашиванием беременности и ХЭ и возможности улучшения репродуктивного прогноза у данных пациенток на фоне противовирусной иммуномодулирующей терапии.
Материал и методы
Всем 50 пациенткам с привычным невынашиванием беременности и ХЭ (основная группа) в возрасте от 21 года до 39 лет проведено полное клинико-диагностическое обследование для уточнения генеза невынашивания беременности и подбора восстановительного лечения перед последующей беременностью. Наряду с общеклиническими исследованиями проводились бактериологические: исследование качественного и количественного состава микрофлоры влагалища, цервикального канала и полости матки; диагностика урогенитальных инфекций методом полимеразной цепной реакции в режиме реального времени с использованием тест-систем производства ФГУН «ЦНИИЭ» Роспотребнадзора (Москва), включающих определение хламидий, микоплазм, уреаплазм, вируса простого герпеса (ВПГ) 1-го и 2-го типов, цитомегаловируса (ЦМВ) и вируса Эпштейна—Барр (ВЭБ), вируса папилломы человека (ВПЧ) высокого канцерогенного риска (ВКР); ультразвуковое исследование с допплеровским картированием до лечения и после него на 5—7-й и 22—24-й дни цикла; пайпель-биопсия эндометрия на 7—11-й день менструального цикла до лечения и после него; гистологическое исследование биоптатов эндометрия, взятых на 7—11-й день менструального цикла до лечения и после него.
На этапе лечения больные были разделены на две подгруппы по 25 пациенток в каждой. Пациенткам 1-й подгруппы с 1-го дня менструации через день наряду с антибиотикотерапией назначался противовирусный препарат на основе аллоферона-альфа.
Пациенткам 2-й подгруппы проводилась антибактериальная и противовирусная иммунокорригирующая терапия с учетом результатов посевов из полости матки и цервикального канала.
Для статистической обработки полученных результатов использовали систему Statistica.
Результаты и обсуждение
Среди обследованных пациенток нарушение менструальной функции имелось у 44%: олигоменорея — у 10%, перименструальные кровянистые выделения — у 26%, аномальные маточные кровотечения — у 8%.
Следует отметить, что клинических проявлений ХЭ у большинства пациенток не отмечалось, что соответствует сложившемуся мнению о латентном, первично-хроническом течении воспалительного процесса в эндометрии.
Пациентки с привычным невынашиванием беременности на фоне ХЭ соматически были отягощены хроническими заболеваниями мочевыделительной системы, желудочно-кишечного тракта, дыхательной системы, что свидетельствует о низком индексе здоровья и иммунодепрессии как факторах, способствующих возникновению инфекционно-воспалительных заболеваний половых органов (персистенция бактериальных и вирусных инфекций приводит к снижению специфической и неспецифической сопротивляемости организма, развитию аутоиммунных процессов). Кроме того, неблагоприятным фактором для формирования репродуктивной функции у данных пациенток явилось проведение большого количества общехирургических полостных операций в препубертатном периоде, в том числе аппендэктомий.
В ходе исследования у обследованных пациенток выявлена высокая частота хронических воспалительных заболеваний шейки матки (100%), хронического воспаления придатков матки (14%), которые также могли явиться провоцирующими факторами для прерывания беременности. Однако при лабораторном обследовании не у всех пациенток с ХЭ удалось выявить инфекционный агент в эндометрии, что, вероятно, связано с инфицированием нижележащей стромы.
При диагностике отделяемого из цервикального канала и полости матки при ХЭ был выявлен почти весь спектр инфекций, передаваемых половым путем (ИППП).
В посевах из цервикального канала преобладали Enterococcus faecalis (28%) и Enterobacter spp. (26%), кишечная палочка (20%), Staphylococcus saprophyticus (14%). Кроме того, выявлены Staphylococcus agalactiae (12%), Staphylococcus carnosus (2%), Staphylococcus halmophilus (2%), вирус генитального герпеса (44%), цитомегаловирусная инфекция — ЦМВ (22%), вирус папилломы человека — ВПЧ (48%), вирус Эпштейна—Барр (12%), Ureaplasma urealyticum (32%), Mycoplasma genitalium (24%), Chlamydia trachomatis (4%), Gardnerella vaginalis (52%), а также грибы рода Candida (58%) (рис. 1).

Рис. 1. Микрофлора отделяемого из цервикального канала (ц/к) и полости матки (п/м) у пациенток с привычным невынашиванием беременности и хроническим эндометритом.
В посевах из полости матки преобладала вирусная (ВПГ 1-го и 2-го типов — 14%; ВПЧ — 12% и ЦМВ — у 2%) и грибковая флора (Candida albicans — 8% и Candida glabrata — 4%), также выявлены Mycoplasma genitalium (8%); Ureaplasma urealyticum (6%); Staphylococcus carnosus (8%); Enterobacter spp. (4%), Staphylococcus haemophilus (4%); Escherichia coli (8%), Enterococcus avium (4%), Staphylococcus warneri (2%), Staphylococcus epidermalis (2%); Enterococcus faecalis (20%); Candida (albicans/glabrata; 12%) (см. рис. 1).
Нужно отметить, что процент выявления условно-патогенной флоры в цервикальном канале был выше, чем в полости матки; вероятнее всего, это обусловлено защитным характером цервикальной слизи для условно-патогенной флоры, препятствующей восхождению инфекции. Полученные нами данные [13] совпадают с мнением ученых о том, что у пациенток с ХЭ почти в 2 раза сократилась частота выявления бактериальных возбудителей с 71 до 37%, в то время как определение вирусных агентов как этиологического фактора возросло почти на 1/3.
Исследование интерферонового статуса у наших пациенток выявило нарушение выработки интерферонов у 90%. Так, недостаточность выработки α-интерферонов различной степени наблюдалась у 26 (52%) обследуемых и γ-интерферонов — у 19 (38%).
Всем пациенткам в I и II фазы цикла проводилось ультразвуковое исследование органов малого таза, включающее трехмерную эхографию и трехмерную допплерометрию матки и эндометрия. Дополнительно пациенткам с привычным невынашиванием беременности проводилось ультразвуковое исследование в двухмерном режиме. При двухмерной эхографии в I фазу менструального цикла наличие гиперэхогенных образований диаметром 0,1—0,3 см, представляющих собой очаги фиброза и кальциноза базального слоя эндометрия, выявлено у 27 (54%) пациенток, асимметрия передней и задней стенок эндометрия и истончение М-эха — у 12 (24%), истончение эндометрия (менее 0,8 см) на 22—24-й день менструального цикла при нормальных размерах желтого тела (1,9—2,5 см) — у 11 (22%).
С целью выявления патологии эндометрия нами дополнительно были обследованы 25 пациенток (группа сравнения) в возрасте от 19 до 27 лет с нормальным уровнем гормонов в I и II фазах менструального цикла, без ИППП, эндокринной и соматической патологии.
При трехмерной эхографии в основной группе объемы тела матки и эндометрия в I фазу менструального цикла составили соответственно 38,2±1,1 и 3,4±0,3 см 3 , во II фазу — 39,0±1,5 и 3,3±0,4 см 3 . В группе сравнения в I фазу менструального цикла они составили 38,5±1,2 и 4,2±0,56 см 3 , во II фазу — 40,53±2,6 и 6,03±0,91 см 3 соответственно (табл. 1). Исключение составили 3 (6%) пациентки с гиперплазией эндометрия, объемы тела матки и эндометрия которых были больше полученных нами средних чисел.

Таблица 1. Параметры трехмерной эхографии у обследованных пациенток Примечание. * — здесь и в табл. 2: различие показателей основной группы и группы сравнения достоверно (р<0,05).
В I фазу показатели индекса васкуляризации (VI) матки и эндометрия у пациенток основной группы соответствовали 1,05±0,2 и 0,63±0,05 против показателей группы сравнения соответственно 1,97±0,1 и 1,85±0,09; индекса кровотока (FI) у пациенток основной группы 23,3±2,5 и 20,5±2,7 против показателей группы сравнения 32,3±2,0 и 30,5±2,23; васкуляризационно-поточный индекс (VFI) основной группы 0,43±0,03 и 0,4±0,1 против показателей группы сравнения 0,68±0,09 и 0,6±0,18.
Во II фазу цикла индекс васкуляризации матки и эндометрия у пациенток основной группы составил 1,52±0,1 и 0,9±0,16 против 2,83±0,18 и 2,41±0,12 у пациенток группы сравнения; индекс кровотока у пациенток основной группы 25,0±1,4 и 19,0±1,5 против 35,4±1,6 и 32,6±1,8 у пациенток группы сравнения; васкуляризационно-поточный индекс основной группы 0,57±0,02 и 0,5±0,09 против 0,9±0,01 и 0,78±0,09 у пациенток группы сравнения (табл. 2).

Таблица 2. Параметры трехмерной допплерометрии у обследованных пациенток
При оценке полученных данных выявлено достоверное снижение показателей васкуляризации всей матки и эндометрия у пациенток с ХЭ по сравнению с показателями у здоровых пациенток (группа сравнения). Полученные данные свидетельствовали о выраженных дисциркуляторных процессах на фоне длительно текущего воспалительного процесса.
Для оценки состояния эндометрия пациенткам проводились офисная гистероскопия со взятием биоматериала и дополнительно пайпель-биопсия эндометрия на 7—11-й день менструального цикла. Четких гистероскопических критериев диагностики ХЭ в отличие от острого нет. Результаты морфологического исследования биоптатов, полученных при офисной гистероскопии, были сопоставимы с результатами гистологического исследования, полученными при проведении пайпель-биопсии эндометрия. В то же время при офисной гистероскопии «симптом клубники» — единичные или множественные очаги гиперемии со светлым точечным центром — были выявлены только у 4 (8%) пациенток, полипы эндометрия — у 7 (14%), синехии у 3 (6%), перегородки в полости матки — у 2 (4%). По мнению F. Polisseni и соавт. [14], чувствительность гистероскопии при диагностике заболевания составляет 16,7%, а специфичность — 93,2%. Важнейшим признаком ХЭ при гистероскопии являются микрополипы, отек и гиперемия слизистой оболочки матки [15].
Морфологическое исследование эндометрия позволило выявить отек стромы и лимфоидную инфильтрацию эндометрия с гранулоцитами, располагающимися в базальном слое и во всех отделах функционального слоя слизистой оболочки, у 100% пациенток; изменения железистого компонента по типу «спрессованных желез» — у 82%; инфицированную слизь с плазматическими клетками, лейкоцитами и лимфоцитами между фрагментами эндометрия — у 78%, скопления гистиоцитов вокруг спиральных артериол — у 58%, склероз и фиброз стромы — у 52%; кроме того, выявлены фиброзные полипы и простая очаговая гиперплазия эндометрия у 8 и 6% пациенток соответственно (рис. 2, а, б).

Рис. 2. Деструкция эндометриальных желез в пайпель-биоптатах с хроническим эндометритом: а — разнообразные по калибру и строению эпителия железы возле участка склероза эндометрия, ×100; б — «спрессованные» железы, вверху — обычная железа с многослойным расположением ядер эпителиоцитов, ×640. Окраска гематоксилином и эозином.
В комплексном лечении пациенток 1-й подгруппы наряду с антибиотикотерапией (моксифлоксацин 400 мг 1 раз в сутки в течение 14 дней) с 1-го дня менструации всем назначался противовирусный иммуномодулирующий препарат на основе аллоферона-альфа согласно схеме через день по 1 мл подкожно, всего 6 инъекций, затем через 3 нед от последней инъекции по 1 мл подкожно 1 раз в неделю еще 3 нед (всего на курс лечения 9 инъекций).
Пациенткам 2-й подгруппы проводилась антибактериальная терапия (моксифлоксацин 400 мг 1 раз в сутки в течение 14 дней) вместе со специфической противовирусной терапией (препараты интерферонов и ацикловир) по показаниям, с учетом результатов обследования.
С целью нормализации микробиоценоза влагалища всем назначался интравагинально трибиотик, содержащий культуры лактобактерий Lactobacillus casei rhamnosus Doderleini, по 1 вагинальной капсуле 2 раза в сутки в течение 7 дней или по 1 капсуле ежедневно в течение 14 дней.
Через 3 мес терапии проводилось контрольное обследование. Бактериологический контроль микрофлоры из эндометрия после лечения выявил 100% эрадикацию бактериальной микрофлоры и снижение вирусной нагрузки до клинически незначимых уровней у всех пациенток 1-й подгруппы и лишь у 11 (44%) из 25 пациенток 2-й подгруппы.
Анализ восстановления менструальной функции на фоне различных схем лечения выявил более выраженный положительный эффект при использовании в терапии противовирусного иммуномодулирующего препарата на основе аллоферона.
У пациенток 1-й группы по результатам 3D-допплерометрии в 70% наблюдений отмечалось повышение индексов внутриматочного кровотока и васкуляризации (табл. 3).

Таблица 3. Динамика показателей 3D-допплерометрии в обследованных группах до лечения и после него Примечание. * — различие показателей в 1-й и 2-й подгруппах после лечения (р<0,05).
Морфологические признаки эндометрита после лечения исчезли у 92% пациенток 1-й подгруппы, и гистоструктура эндометрия стала соответствовать нормальной средней стадии пролиферации. Только у 1 (4%) пациентки 1-й подгруппы наблюдалась неполноценность щеточной каймы и у 2 (8%) — изменения желез по типу «спрессованных».
В то же время во 2-й подгруппе морфологические признаки эндометрита сохранялись у 10 (40%) пациенток, неполноценность щеточной каймы — у 8%, изменения железистого компонента — у 20%, у 4 (16%) больных сохранялась воспалительная инфильтрация в миометрии; склероз и фиброз стромы — у 3 (12%) пациенток.
С целью продолжения прегравидарной подготовки пациенток применялся микродозированный дроспиренонсодержащий комбинированный контрацептив с левомефолатом кальция в течение 3—6 мес с последующей коррекцией недостаточности лютеиновой фазы назначением препарата прогестерона — дидрогестерона.
Таким образом, высокая частота выявления вирусных инфекций (ВПГ 1-го и 2-го типов — у 44%, ЦМВ — у 22%, ВЭБ — у 12%, ВПЧ ВКР — у 48%) у пациенток с привычным невынашиванием беременности и ХЭ, а также снижение продукции α-интерферонов (44%) и γ-интерферонов (40%) определяют необходимость применения не только антибактериальной, но и противовирусной и иммуномодулирующей терапии.
Выводы
1. Полученные данные позволяют с уверенностью утверждать, что включение в комплексную терапию пациенток с привычным невынашиванием беременности и хроническим эндометритом отечественного противовирусного препарата локального иммуномодулирующего действия на основе аллоферона-альфа способствует купированию клинических симптомов, нормализации морфологической и эхографической картины эндометрия, элиминации возбудителя и нормализации показателей иммунного статуса.
2. Предложенная нами комбинированная тактика является доступной, более эффективной и может быть использована на этапе прегравидарной подготовки у пациенток с привычным невынашиванием беременности и хроническим эндометритом.
Эндометрит — симптомы и лечение
Что такое эндометрит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Делеске Инны Александровны, гинеколога со стажем в 11 лет.
Над статьей доктора Делеске Инны Александровны работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
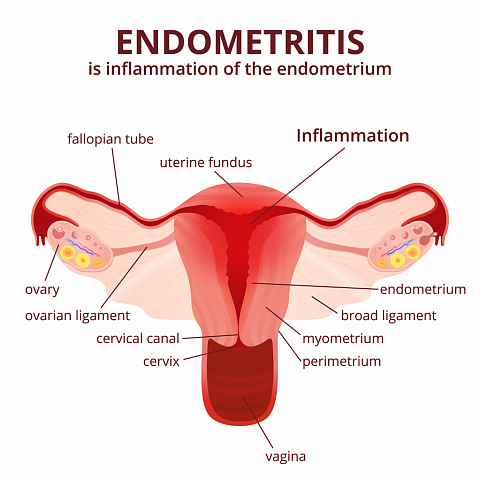
Эндометрит — это воспаление внутреннего слоя матки (эндометрия), которое приводит к изменению его функций. Возникает в результате заражения этой области микробами, вирусами и грибковыми инфекциями.
Эндометрит — одно из наиболее распространенных гинекологических заболеваний. По данным зарубежных источников, распространенность эндометрита составляет 20% в популяции, отечественные авторы указывают до 60-70%, чаще всего болеют женщины репродуктивного возраста [9] [11] . Стабильный рост заболеваемости отмечается последние 20-30 лет [1] [10] . Часто встречается в сочетании с ранним началом половой жизни, отсутствием контрацепции, абортами, наличием хронических воспалительных заболеваний нижнего отдела репродуктивного тракта. [7] [8] .
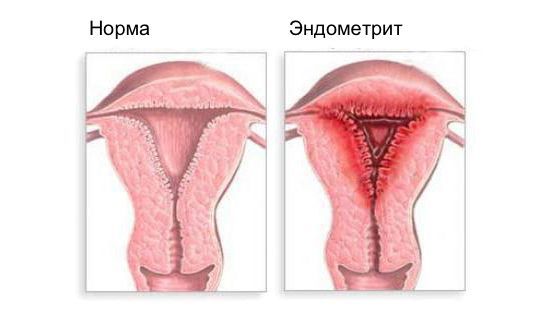
Эндометрит часто является причиной бесплодия, привычного невынашивания (два и более выкидыша в анамнезе), нарушения менструального цикла, осложнений беременности, родов и послеродового периода, неудачных попыток ЭКО, гиперпластических заболеваний эндометрия и сексуальных проблем [1] .
Чем эндометрит отличается от эндометриоза
Эндометриоз — это разрастание эндометриоидной ткани. Эндометриоз может поражать полость матки, её оболочки, маточные трубы, яичники, брюшину и области вне половых органов. Эндометритом же называют воспаление внутреннего слоя матки.
Причины эндометрита
В женском репродуктивном тракте присутствуют различные микроорганизмы, среди которых преобладают Lactobacillus spp. Эндометрит чаще ассоциирован с чрезмерным размножением бактерий Enterobacter, Enterococcus, Streptococcus, Staphylococcus, Ureaplasma, Mycoplasma.
Эндометрит вызывают также вирусные инфекционные агенты: вирус герпеса, цитомегаловирус, вирус папилломы человека, энтеровирусы и аденовирусы.
Возможен эндометрит специфической этиологии: гонорейный, туберкулезный, актиномикотический (грибковая инфекция) и неспецифический. [8] [7] [10] .
Риск развития эндометрита увеличивают:
- манипуляции в полости матки — аборты, выскабливания, метросальпингография (контрастное рентгенологическое исследование полости матки и проходимости фаллопиевых труб), введение внутриматочного контрацептива, инсеминация (введение спермы), ЭКО;
- заболевания мочевыделительной системы;
- операции на органах малого таза;
- послеродовые гнойно-воспалительные осложнения;
- другие гинекологические заболевания (хронический сальпингоофорит, цервицит, гиперплазия эндометрия, полип эндометрия);
- частая смена половых партнеров;
- незащищенные половые связи;
- предшествующие прерывания беременности;
- кесарево сечение до 28 недель гестации;
- длительный безводный период в родах;
- ручное отделение плаценты;
- инвазивные исследования для пренатальной диагностики;
- длительное ношение внутриматочного контрацептива.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы эндометрита
Воспаление может протекать в острой и хронической форме. Чаще всего симптомы эндометрита появляются на четвёртый день после инфицирования. При острой форме эндометрита отмечаются общие симптомы воспаления, такие как слабость, быстрая утомляемость, повышение температуры тела, изменения в общем анализе крови (сдвиг лейкоцитарной формулы влево и повышение СОЭ).
К локальным симптомам острого эндометрита можно отнести:
- периодические умеренные или острые тянущие боли внизу живота, иногда отдающие вниз спины и в пах;
- жидкие гноевидные выделения из половых путей с неприятным запахом (возможно с примесью крови);
- диспареуния (боль при половом акте).
При отсутствии правильного и своевременного лечения эндометрита в течении 10 дней возможен переход в хронический воспалительный процесс. При этом держится повышенная температура, появляются новые симптомы:
- нарушение менструального цикла, мажущие кровянистые выделения в середине цикла;
- привычное невынашивание беременности;
- серозно-гнойные выделения из половых путей;
- ноющие боли внизу живота;
- боль во время секса [3][5][8] .
Течение острого послеродового эндометрита более тяжёлое, проявляется в следующих симптомах:
- повышение температуры тела до 38-39 °C ;
- озноб, потливость, тахикардия;
- умеренные тянущие боли внизу живота;
- лохии (послеродовые кровянистые выделения с примесью слизи), мутные или гнойные с неприятным запахом;
- матка болезненная и увеличена.
Эндометрит при беременности
Эндометрит препятствует имплантации плодного яйца, из-за чего оно может отторгнуться полностью или возникнет нарушение процессов имплантации. В дальнейшем это может привести к выкидышу или замершей беременности.
Если воспалительный процесс усиливается, может развиться хориоамнионит — воспаление плаценты, которое приводит к разрыву плодных оболочек, излитию околоплодных вод и преждевременным родам.
Чтобы избежать возможных осложнений, женщинам с хроническим эндометритом при планировании беременности необходимо пройти комплексное лечение.
Патогенез эндометрита
На начальном этапе воспаления инфекционный агент (бактерии, вирусы или грибки) внедряется в слизистую оболочку матки. Начинается выработка медиаторов воспаления, которая приводит к нарушению микроциркуляции крови в его очаге. Миграция лейкоцитов в зону повреждения, активация нейтрафилов и макрофагов ведёт к активной выработке цитокинов и перекиси водорода, запуску перекисного окисления липидов с повреждением мембран клеток. В это время на фоне повышенной выработки цитокинов и факторов роста происходит деградация матрикса клеток. Нарушение микроциркуляции крови приводит к развитию локальной ишемии и гипоксии ткани, которые затем активируют процессы склерозирования. При длительной стимуляции иммунной системы происходит её истощение и появление аутоиммунных реакций.
В 95% случаев эндометрит является первичным — патогенные микроорганизмы попадают в полость матки восходящим путём, при половом контакте или гинекологических манипуляциях . В 5% случае эндометрит носит вторичный характер: инфекция попадает в эндометрий гематогенным путем, либо же лимфогенным или нисходящим путём (с верхних отделов репродуктивного тракта).
При длительности воспалительного процесса более 2 месяцев можно расценивать его как хронический процесс. Развиваются изменения в структуре и функции ткани, происходит нарушение пролиферации (деления клеток) и физиологической циклической трансформации эндометрия. В связи с этим возможно нарушение нормальной имплантации эмбриона при беременности.
Существует аутоиммунная теория патогенезе хронического эндометрита. Она говорит о том, что при длительном воздействии инфекционного агента на иммунную систему происходит вторичное повреждение эндометрия. При этом нарушается процесс апоптоза (запрограммированной гибели клетки) [11] .
Классификация и стадии развития эндометрита
Эндометрит можно разделить на острую и хроническую форму.
Острый эндометрит возникает при абортах, диагностических манипуляциях, выскабливании, развивается быстро, воспаление сопровождается острыми или ноющими болями и повышением температуры. Наиболее частый путь инфекции при нём — восходящий. Распространение инфекции из влагалища в верхние отделы репродуктивного тракта происходит при несостоятельности барьера шейки матки. Воспаление может локализоваться в эндометрии, а также переходить на миометрий. При несвоевременном и неполноценном лечении возможно развитие пельвиоперитонита (воспаление оболочки брюшины в области малого таза).
Отдельно выделяется острый послеродовый эндометрит — начинается на 2-4 сутки после родов, ему может предшествовать хориоамнионит (инфицирование оболочек плода и жидкости).
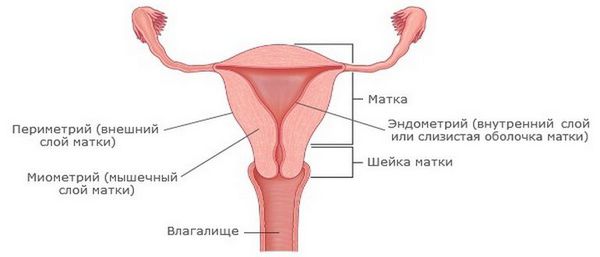
При хроническом эндометрите симптоматика сглажена. Характерны периодические обострения и рецидивы после переохлаждения и воспаления другой локализации урогенитального тракта.
По клиническим проявлениям эндометрит подразделяется на клиничеcки выраженную и субклиническую форму.
По характеру воспалительного процесса эндометрит можно разделить на:
- Катаральную форму (поражение поверхностных слоев слизистой оболочки матки и выделение слизистого экссудата).
- Катарально-гнойную форму.
- Гнойную форму.
- Некротическую форму.
- Гангренозную форму.
По морфологическим признакам:
- Атрофический эндометрит — наблюдается атрофия желез эндометрия, фиброз стромы, инфильтрация лимфоидными элементами;
- Кистозный эндометрит — сдавление протоков желез фиброзной тканью, образование кистозных элементов в эндометрии;
- Гипертрофический эндометрит — характеризуется гипертрофией желез эндометрия в результате хронического воспаления [5] .
Осложнения эндометрита
Осложнения у эндометрита могут быть достаточно серьёзными.
Метротромбофлебит (тромбоз тазовых вен) развивается через 2-3 недели от начала заболевания эндометритом. Пациентки отмечают общие симптомы воспаления, сохраняющуюся повышенную температуру тела, тянущие или острые боли внизу живота, выделения из половых путей [1] [2] .
Параметрит — воспаление околоматочной клетчатки. После внедрения инфекционного возбудителя в параметрий возможно образование диффузного воспалительного инфильтрата. При отсутствии лечения происходит нагноение и переход в хроническое течение. При переходе на всю клетчатку развивается пельвиоцеллюлит (воспаление клетчатчки малого таза) [2] [9] [10] .
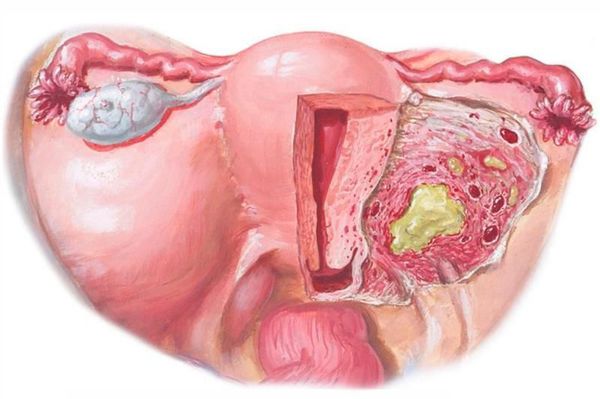
Пельвиоперитонит — воспаление выходит за пределы матки, в процесс вовлекаются листки брюшины. Пациентки отмечают резкое повышение температуры, симптомы интоксикации, тошноту, рвоту, интенсивные боли внизу живота (основная локализация ниже пупка), симптом раздражения брюшины ( резкое усиление боли в животе при быстром надавливании и снятии руки).
Сальпингоофорит — воспалительный процесс в маточных трубах и яичнике. Наиболее частые осложнения при несвоевременном лечении: пиовар (гнойное воспаление яичника) и туюоовар (формирование единого гнойного конгламерата из воспаленного яичника и маточной трубы). Все вышеперечисленные осложнения требуют оперативного лечения [2] [9] [10] .
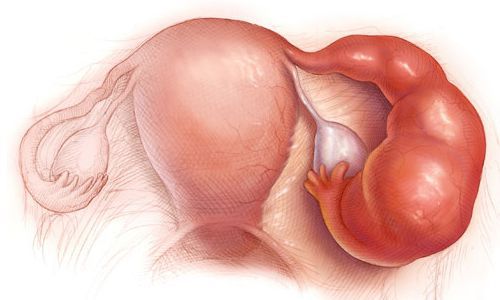
Другими осложнениями могут быть бесплодие, нарушение менструального цикла, выкидыши, внематочная беременность, спаечный процесс в малом тазу [1] [2] [3] .
В некоторых случаях возникает септический шок — угрожающее жизни осложнение, в условиях которого критически нарушается кровоснабжение тканей и клеточный метаболизм. Главные симптомы сепсиса — высокие показатели температуры тела, симптомы интоксикации, снижение давления и тахикардия, изменения в общих анализах крови, обильное потоотделение, спутанность сознания [8] [9] .
Диагностика эндометрита
Диагностика хронического эндометрита должна быть основана на комплексном подходе анализа жалоб пациентки, анамнеза, симптомов, результатов эхографических исследований, лабораторной диагностики, данных морфологического исследования эндометрия и иммунного статуса.
Пайпель-биопсия эндометрия
Хронический эндометрит диагностируют прежде всего с помощью морфологического исследования [8] .
Гистологический материал получают при выскабливании стенок полости матки под контролем гистероскопа или пайпель-биопсии. Пайпель-биопсия — это получение гистологического материала с помощью тонких канюль при аспирации (удалении) эндометрия. Данный метод имеет большую диагностическую ценность в амбулаторных условиях.
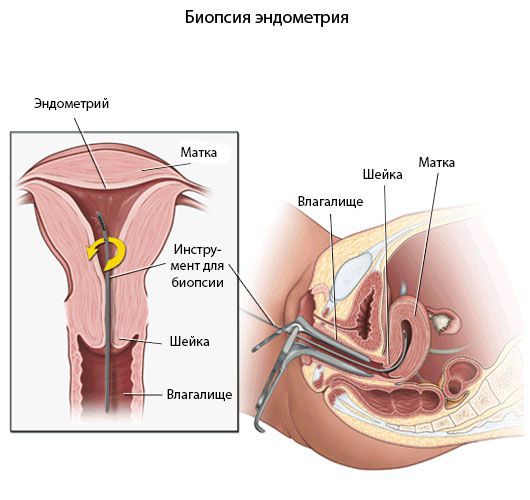
Критериями хронического эндометрита является наличие очаговых или диффузных лимфоидных инфильтратов, склероз стенок спиральных артерий, фиброз стромы и наличие плазматических клеток. При этом к абсолютным признакам хронического эндометрита относят плазматические клетки.
Микробиологическое исследование
Микробиологические посевы используются для выявления возбудителя воспалительного процесса.
Иммуногистохимическое исследование
Иммуногистохимическое исследование при эндометрите заключается в исследовании биоптата слизистой оболочки матки с целью определения мембранного белка, который является маркером плазматических клеток. Информативность гистологического исследования при этом возрастает до 85-90%, можно установить и иммунный характер повреждения эндометрия [5] [7] [8] .
УЗИ при эндометрите
При эхографии (УЗИ) хронический эндометрит определяют по:
- изменениям в структуре эндометрия;
- участкам повышенной эхогенности различной формы и величины в зоне М-Эхо;
- наличию сниженной эхогенности в эндометрии;
- наличию жидкости в полости матки;
- присутствию мелких кальцинатов 1-3 мм в эндометрии;
- участкам фиброза в эндометрии разной степени;
- наличию внутриматочных синехий.
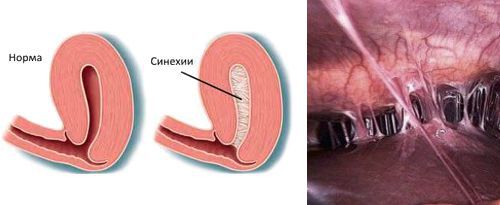
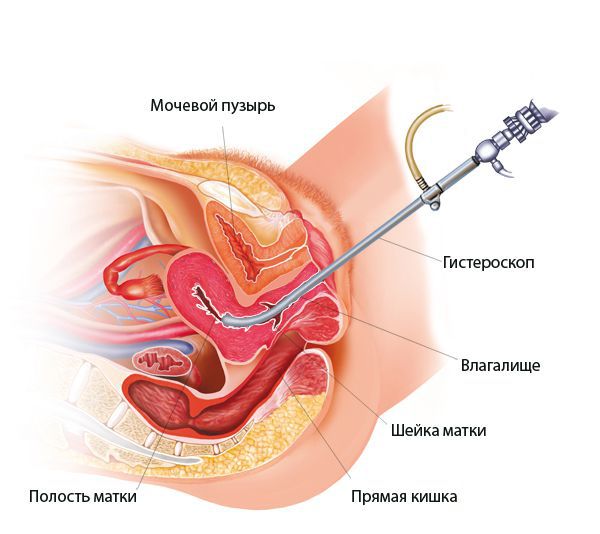
Гистероскопия при эндометрите
При гистероскопии определяются следующие признаки хронического эндометрита: гиперемия слизистой оболочки матки, неровномерная толщина эндометрия, полипообразные образования, кровоизлияния, очаговая гиперплазия эндометрия.
Лечение эндометрита
Лечение эндометрита на первом этапе заключается в устранении бактериального или грибкового возбудителя, а для эндометрита вирусной этиологии — снижении вирусной нагрузки [7] . Для этого проводят комплексное лечение, включающее в себя антибактериальную терапию, анаэробные средства, противовоспалительные и противовирусные лекарственные средства [5] [6] [8] .
Второй этап заключается в восстановлении рецептивности эндометрия и его функциональности. Успешное восстановление рецепторного аппарата эндометрия должно происходить без снижения пролиферации (размножения, разрастания) клеток. Устраняются последствия ишемии, склеротические процессы, восстановливается отток крови. Длительность и объёмы терапии зависят от тяжести воспалительного процесса и сопутствующей гинекологической патологии. После проведения основных этапов лечения необходим курс реабилитации (физио-терапевтическое лечение) [7] [8] [10] .
Иммуностимулирующую терапию применяют при комплексном лечении хронического эндометрита, если выявлена вирусная инфекция: вирус папилломы человека, герпеса, Эпштейна — Барр, цитомегаловирус.
Гормональную терапию используют для подготовки эндометрия, чаще всего перед ЭКО. Для применения гормональных препаратов необходимо гистологическое подтверждение патологии эндометрия.
Контрольные критерии эффективности терапии хронического эндометрита:
- допплерометрическое исследование сосудов матки с ЦДК во 2 фазу менструального цикла;
- определение ангиогенных факторов;
- клиническое улучшение.
Рекомендации по диагностике и лечении эффективны лишь у половины больных, а частота рецидивов остается на уровне 25 % [13] .
Прогноз. Профилактика
При своевременном и полноценном лечении прогноз благоприятный. Пациентки отмечают улучшение состояния в течении двух суток. При запоздалом лечении эндометрита возможно развитие септического шока.
Эндометрит: симптомы и лечение у женщин

Эндометритом называется воспаление слизистой оболочки матки, которое начинается из-за паразитирования микроорганизмов: они повреждают слизистую, активируют иммунную систему и мигрируют в область воспаления. Есть несколько видов таких «вредителей»:
- бактерии — наиболее частый виновник эндометрита. Выделяются специфичные и неспецифичные возбудители: к первым относятся хламидии, уреаплазмы, бледная трепонема сифилиса, микобактерии туберкулеза, ко вторым — синегнойная и кишечная палочка, стрептококки, стафилококки;
- грибки: чаще заболевание вызывают так называемые актиномицеты на фоне сниженного иммунитета;
- определенные виды вирусов;
- зачастую к развитию болезни приводит столкновение сразу нескольких возбудителей.
Симптомы и лечение эндометрита связаны со сложностью заболевания. При тяжелом течении эндометрита (помимо стандартного воспаления) развивается гнойный процесс. Гной образуется из погибших «бойцов» в борьбе за здоровье организма — микроорганизмов и лейкоцитов — и значительно утяжеляет течение заболевания. Иногда у больных проявляется пиометра — состояние, при котором полость матки заполняется гноем.
Возбудители проникают в матку двумя путями: восходящим и нисходящим. В первом случае бактерии попадают в полость из влагалища через шейку матки. Нисходящий путь бывает гематогенным или лимфогенным: иными словами, если в организме уже запущен какой-то воспалительный процесс, возбудитель попадает в матку через кровь или лимфу.
На развитие и течение воспаления влияет ряд провоцирующих факторов:
- Механическое повреждение (травмы) слизистой: аборты, выскабливание дна матки, кесарево сечение, вагинальные обследования с введением гинекологических инструментов.
- При менструации отторгается поверхностный слой эндометрия и формируется раневая (уязвимая) поверхность. К развитию эндометрита приводит и незащищенный секс во время месячных: заражение проходит по восходящему пути.
- Снижение местного или общего иммунитета на фоне врожденного или приобретенного иммунодефицита: прием иммунодепрессантов, ВИЧ, гиповитаминоз, нарушения питания. В этом случае возможно как восходящее, так и нисходящее заражение.
Другие, не менее опасные факторы — появление в полости матки остатков плаценты после кесарева сечения или родов, а также наличие там децидуальной (отпадающей) ткани, сгустков крови, плодного яйца. Поэтому аборт (особенно в нестерильных условиях) и выскабливание могут привести к воспалению.
Симптомы эндометрита матки
Лейкоциты — клетки иммунной системы — вырабатывают медиаторы воспаления простагландины. Этот процесс проявляется в ряде симптомов:
- у пациенток наблюдается отек, так как повышается проницаемость стенок сосудов, и потому плазма крови выходит в межклеточное вещество;
- боль появляется из-за того, что простагландины раздражают чувствительные нервные окончания и сдавливают их вследствие отека;
- застой крови усиливается в области воспаления из-за сужения (спазма) венозных сосудов и ухудшения оттока крови. Внешне реакция проявляется в виде покраснения воспаленного участка;
- в попытках защититься организм вырабатывает антитела и увеличивает активность лейкоцитов, из-за чего поднимается температура. Подъем только на 0,1° С может усилить активность нашего иммунитета в 10 раз.
При эндометрите проявляется острое либо хроническое воспаления: первое характеризуется яркой симптоматикой, второе нередко протекает бессимптомно. Острый воспалительный процесс чаще связан с воздействием сразу нескольких микроорганизмов. Реже слизистая оболочка поражается изолированно: обычно воспаляется мышечная оболочка матки наравне с развитием миоэндометрита.
При остром эндометрите симптомы проявляются на 3-4 день: повышается температура, наблюдается слабость, головная боль и боль внизу живота, гнойные и (или) кровянистые выделения. Острая стадия длится от 8 до 10 дней и полностью проходит при правильном и своевременном лечении. Если же этого не произошло, острая форма может перетечь в хроническую.
Хронический эндометрит легко не заметить: часто женщины узнают о заболевании только на приеме у гинеколога или при планировании беременности. Наиболее яркий симптом заболевания — нарушение менструального цикла. Температура у пациенток обычно нормальная, иногда бывают ноющие боли в пояснице и внизу живота. Поэтому окончательный диагноз ставится только на основе гистологического исследования эндометрия.
При обсуждении репродуктологии важнее говорить о хроническом эндометрите (ХЭ). Острая патология замечается почти сразу и потому оперативно устраняется. А вот хроническая фаза требует долгого лечения в течение нескольких месяцев, ведь при такой форме заболевания эндометрий сильно видоизменяется, не может трансформироваться и обновляться.
Чаще всего болезнь проявляется у женщин от 26 до 35 лет. Национальный центр контроля заболеваемости сообщает, что каждый год в США регистрируют около 1 млн воспалительных заболеваний органов малого таза. В России такие диагнозы ставятся от 28 до 34 % пациенток гинекологии. При хроническом эндометрите часто развивается бесплодие или привычное невынашивание беременности: до 65 % и до 70 % случаев соответственно. Плодное яйцо не может прикрепиться к измененному эндометрию, из-за чего беременность не наступает или протекает неудачно.
Клинические проявления хронического эндометрита таковы:
- аномальные маточные кровотечения и выделения из половых путей;
- синдром тазовых болей;
- диспареуния (болезненный половой акт);
- бесплодие и/или неудачные ЭКО, привычное невынашивание беременности;
- преждевременные роды.
Однако единого мнения насчет клинической картины хронического эндометрита не существует. Даже при явных симптомах невозможно понять, какова глубина функциональных и структурных изменений эндометрия.
Лечение эндометрита у женщин разного возраста
Симптомы и лечение эндометрита у женщин мало связаны с возрастом. После 40 лет острый эндометрит обычно проявляется более ярко: на это влияют изменения гормонального фона из-за предстоящего климакса. Переход острой формы в хроническую в этом возрасте происходит намного быстрее, однако формат лечения в 25 и 45 лет не различается.
Борьба с заболеванием — сложная, но важная задача, особенно у женщин, переживших выкидыш или неудачное ЭКО. Чтобы поставить точный диагноз и подобрать индивидуальное лечение, врачи МЦРМ собирают детальный анамнез. Необходимо выяснить информацию о менструальной функции, течении и исходе беременностей, абортах и выкидышах. Это позволит верно диагностировать патологию и подготовить эндометрий к беременности с помощью специально подобранных препаратов.
В комплексное лечение входят антибиотики широкого спектра с высокой способностью проникновения в клетку, а также (в зависимости от вида возбудителя) противогрибковые (антимикотики) и противовирусные препараты, местные комбинированные лекарства, системная энзимотерапия (применение ферментов) и физиотерапия в момент реабилитации. Для профилактики кандидоза на фоне антибиотиков назначаются противогрибковые препараты.
Следующий этап — гормональная терапия: комбинированные оральные контрацептивы. Во вторую фазу цикла при планировании беременности врач назначает прогестерон. Лечение начинается с первого дня менструации.
Перед назначением препаратов в нашей клинике проходит комплексная диагностика:
- ультразвуковое исследование органов малого таза;
- гистероскопия — осмотр внутренней оболочки матки (в сочетании с лапароскопией или изолированно);
- исследование эндометрия (получение материала во время гистероскопии, раздельного диагностического выскабливания или аспирационной биопсии);
- иммуногистохимическое и микробиологическое исследование эндометрия;
- ПЦР (фемофлор-скрининг): метод выявит патогенную микрофлору и причины развития воспалительного процесса.
После диагностики мы подбираем индивидуальное лечение. На первом этапе необходимо уничтожить инфекционного агента, на втором — восстановить функционал эндометрия: благодаря лечению устраняются повреждения, завершается регенерация, восстанавливается локальная гемодинамика (движение крови в сосудах) и активность рецепторов эндометрия.
В стенах клиники мы много лет разрабатывали схемы, которые помогают наиболее эффективно бороться с заболеванием. Прежде всего на весь период лечения (два-три менструальных цикла) прописываются следующие препараты:
- Монофазные комбинированные оральные контрацептивы (Ярина, Джес, Жанин, Фемоден и др.).
- Витаминотерапия: Фемибион, Ангиовит или Элевит (одна капсула в сутки).
- Иммунотерапия: Вобэнзим — три капсулы три раза в день за 30 минут до приема пищи.
Препараты в первый месяц лечения:
1. При обнаружении патогена по результатам фемофлор-скриннинга с первого дня менструального цикла назначается антибактериальная либо противовирусная терапия — в зависимости от вида возбудителя. Если в результате фемофлор-скрининга патоген не найден, антибиотики пить не нужно!
2. Также важна поддержка нормальной флоры желудочно-кишечного тракта и влагалища, поэтому:
- первый и последний дни приема антибиотиков назначается Дифлюкан: 150 мг перорально.
- Препараты, регулирующие равновесие кишечной микрофлоры, на выбор:
- Бифиформ — одна капсула 3 раза в день во время еды в течение трех недель,
- Аципол — две капсулы 3 раза в день на протяжении трех недель,
- Энтерол — по одной капсуле 2 раза в сутки 10 дней.
- Лактожиналь — по одной свече во влагалище на ночь в течение двух недель;
- Лактагель — по одному тюбику во влагалище на протяжении двух недель;
- Вагинорм-С — одна вагинальная капсула в течение 12 дней.
Препараты во второй месяц лечения:
1. Активная иммунотерапия: 10 дней после менструации принимается Генферон — 250 тыс. ед. два раза в сутки интравагинально.
2. Препараты, которые активируют обмен веществ в тканях, улучшают трофику (питание клеток) и стимулируют процесс регенерации: Актовегин — одно драже 3 раза в сутки перед приемом пищи на протяжении 30 дней.
3. Физиотерапевтические методы благоприятно влияют на пораженные ткани, помогают снять воспалительные процессы, улучшить состояние сосудов и эндометрия.
В третий месяц лечения важно закрепить результат: лучше всего отправиться на санаторно-курортное лечение. Можно поехать в «Балтийский Берег» в Зеленогорске (50 км от центра Санкт-Петербурга): там работают врачи-партнеры, сопровождающие наших пациентов на месте. Специалисты будут знать всё о вашем диагнозе и дадут своевременный совет. Стоимость индивидуальной программы составляет от 2060 рублей в сутки.
Хронический эндометрит и беременность
Как уже было сказано ранее, при хроническом эндометрите часто наблюдается бесплодие или привычное невынашивание беременности. Необходимо, чтобы слой эндометрия постоянно регенерировался: только тогда зародыш будет успешно имплантирован в матку. При хроническом эндометрите регенерация невозможна из-за воспалительного процесса, поэтому плодное яйцо не может закрепиться на эндометрии.
Даже если это происходит, беременность редко оказывается успешной: риск выкидыша сохранится на протяжении вынашивания. Такую беременность сопровождают нарушения и осложнения: в частности, возбудители заболевания могут поразить ткани плода, что приведет к его гибели.
Нарушение развития эмбриона — еще одно возможное последствие беременности при эндометрите. Поврежденному эндометрию не хватает поступления крови из-за застоя: ткань не получает кислород, витамины, питательные вещества и не передает их эмбриону. Из-за этого ребенок может родиться с патологиями. Кроме того в несколько раз повышается вероятность рождения раньше срока, может нарушиться формирование плаценты, так что при планировании беременности следует немедленно начать лечение этого заболевания.
В общей сложности выкидыши и бесплодие из-за хронического эндометрита связаны сразу с несколькими причинами:
- Нарушение морфологии эндометрия, из-за чего оплодотворенная яйцеклетка не закрепляется в матке и выходит вместе с выделениями — в таком случае женщина может даже не знать, что была беременна.
- Проблемы с синтезом прогестерона: этот гормон поддерживает состояние беременности, утолщая эндометрий и подготавливая слизистую матки. При хроническом эндометрите прогестерон вырабатывается слабо, а беременность прерывается на раннем сроке.
- Мужские сперматозоиды инактивируются уже при зачатии. При воспалении фагоцитарные клетки организма уничтожают чужеродные тела, за которые принимают и сперматозоиды.
Поэтому перед планированием беременности необходимо пройти полный курс лечения от эндометрита: в таком случае вероятность забеременеть может возрасти до 100 %. В случае с ЭКО основная проблема связана именно с закреплением половых клеток в матке, поэтому для эффективности стоит сделать несколько попыток подсадить оплодотворенную яйцеклетку. Помимо приема препаратов необходимо поберечь себя: постараться исключить стрессы, ограничить физическую нагрузку и не поднимать тяжести.
Источник https://www.mediasphera.ru/issues/rossijskij-vestnik-akushera-ginekologa/2017/5/1172661222017051029
Источник https://probolezny.ru/endometrit/
Источник https://www.mcrm.ru/encyclopedia/articles/vse-o-besplodii/endometrit/