Рак желудка
Пользователи протокола: онкологи (онкохирурги, химиотерапевты, радиологи), общие хирурги, гастроэнтерологи, врачи общей практики, врачи скорой и неотложной помощи, патологоанатомы, морфологи, диетологи.
Категория пациентов: взрослые.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с не высоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++или+), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование, или мнение экспертов. |
| GPP | Наилучшая фармацевтическая практика. |

Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
— 800 RUB / 5500 KZT / 27 BYN — 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место — 800 RUB / 5500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
Клиническая классификация
- Аденокарцинома — наиболее частая форма (95%):
- Железисто-плоскоклеточный рак;
- Плоскоклеточнй рак;
- Недифференцируемый рак;
- Мелкоклеточный рак.
- Полиповидный рак;
- Изъязвленный рак с четкими границами;
- Изъязвленный рак с нечеткими границами;
- Диффузно-инфильтративный.
Международная классификация TNM:
Последний пересмотр этой классификации состоялся в 2017г. – 8-е издание, и она была одобрена всеми национальными комитетами по классификациям заболеваний. Классификация применима только для рака желудка, при гистологическом подтверждение диагноза.
ПРАВИЛА ДЛЯ КЛАССИФИКАЦИИ
Классификация распространяется только на карциному. Должно быть гистологическое подтверждение болезни. Рак, связанный с эзофагогастральным соединением (ЭГС), эпицентром которого является в проксимальные 2 см кардии (типы Siewert I / II) должны быть поставлены как рак пищевода. Опухоли, эпицентр которых находится на расстоянии более 2 см от ЭГС, будут проводиться с использованием TNM и стадии рака желудка, даже если задействован ЭГС.
Анатомические области

Регионарными лимфатическими узлами для желудка являются лимфатические узлы, расположенные вдоль малой (1, 3, 5) и большой (2, 4а, 4б, 6) кривизны, вдоль левой желудочной (7), общей печеночной (8), селезеночной (10, 11) и чревной (9) артерий, а также гепатодуоденальные узлы (12). Поражение других внутрибрюшинных лимфатических узлов, таких как ретропанкреатические, мезентериальные и парааортальные, классифицируются как отдаленные метастазы.
Клиническая классификация TNM 8-е издание 2017г [5] (УД — А):
Т – Первичная опухоль
Тх – Первичная опухоль не может быть оценена;
То – Отсутствие данных о первичной опухоли;
Tis – Карцинома in situ, интраэпителиальная опухоль без инвазии в собственную пластинку слизистой оболочки, тяжелая дисплазия;
Т1а – Опухоль прорастает в собственную пластинку слизистой оболочки или мышечную пластинку слизистой оболочки;
T1b – Опухоль прорастает в подслизистую основу;
Т2 – Опухоль прорастает в мышечную оболочку;
Т3 – Опухоль прорастает в подсерозную основу без инвазии в висцеральную брюшину или соседних структур 1 ;
Т4а – Опухоль прорастает в серозную оболочку (висцеральная брюшина);
T4b – Опухоль врастает в соседние структуры 2 .
1 Опухоль, которая распространяется на желудочно-ободочную или желудочно- печѐночную связку, большой или малый сальник, но не прорастает в висцеральную брюшину, классифицируют как Т3.
2 Соседними структурами для желудка являются селезѐнка, поперечная ободочная кишка, печень, диафрагма, поджелудочная железа, брюшная стенка, надпочечники, почки, тонкая кишка, забрюшинное пространство.
N – Региональные лимфатические узлы
NX – Региональные лимфатические узлы не могут быть оценены; N0 – Нет метастазов в региональных лимфатических узлах;
N1 –Метастазы в 1 – 2 региональных лимфатических узлах; N2 – Метастазы в 3—6 региональных лимфатических узлах;
N3 – Метастазы в 7 и более региональных лимфатических узлах.
М – Отдаленные метастазы
М0 – Нет отдаленных метастазов;
М1 – Есть отдаленные метастазы или наличие опухолевых клеток в асцитической жидкости.
Гастроинтестинальная стромальная опухоль [5] (УД — А)
Клиническая классификация TNM:
Т – Первичная опухоль;
ТХ – Первичная опухоль не может быть оценена; ТО – Отсутствие данных о первичной опухоли; Т1 – Опухоль не более 2 см;
Т2 – Опухоль более 2 см, но не более 5 см в наибольшем измерении; Т3 – Опухоль более 5 см, но не более 10 см в наибольшем измерении; Т4 – Опухоль более 10 см в наибольшем измерении;
N – Региональные лимфатические узлы
NX — Региональные лимфатические узлы не могут быть оценены;
N0 — Метастазы региональных лимфатических узлов отсутствуют;
N1 — Метастазы в 1-2 региональных лимфатических узлах;
N2 — Метастазы в 3-6 региональных лимфатических узлах;
N3 — Метастазы в 7 или более региональных лимфатических узлах;
N3a — Метастазы в 7-15 региональных лимфатических узлах;
N3b – Метастазы в 16 или более региональных лимфатических узлах;
*При GIST региональные лимфатические узлы вовлекаются редко, поэтому те случаи, когда статус лимфатических узлов не может быть оценен клинически или морфологически, рассматривают как N0 вместо NX или pNX.
М – Отдаленные метастазы
М0 – Нет отдаленных метастазов;
М1 – Есть отдаленные метастазы.
Патогистологическая классификация pTNM:
Требования к определению категорий pT, pN, pM соответствуют требованиям к определению категорий T, N, M.
Примечание: pN0 гистологическое исследование включает обычно 15 и более регионарных лимфатических узлов.
G – гистопатологическая дифференцировка
GX – степень дифференцировки не может быть установлена;
G1 – высокая степень дифференцировки;
G2 – средняя степень дифференцировки;
G3 — низкая степень дифференцировки;
G4 — недифференцируемый рак.
| Группировка по стадиям: | |||
| Стадия | T | N | M |
| СТАДИЯ 0 | Tis | N0 | М0 |
| СТАДИЯ IА | Т1 | N0 | М0 |
| СТАДИЯ IB | Т1 | N1 | М0 |
| Т2 | N0 | М0 | |
| СТАДИЯ IIA | Т1 | N2 | М0 |
| Т2 | N1 | М0 | |
| Т3 | N0 | М0 | |
| СТАДИЯ IIIА СТАДИЯ IIIB | Т1 | N3 | М0 |
| Т2 | N2 | М0 | |
| Т3 | N1 | М0 | |
| Т4a | N0 | М0 | |
| СТАДИЯ IIIC | Т2 | N3 | М0 |
| Т3 | N2 | М0 | |
| Т4a | N1 | М0 | |
| СТАДИЯ IIIА | Т3 | N3 | М0 |
| Т4a | N2 | М0 | |
| Т4b | N0-1 | М1 | |
| Т4a | N3 | М0 | |
| Т4b | N2-3 | М0 | |
| СТАДИЯ IIIB | Любая Т | Любая N | М1 |
| Прогностические факторы | Связанные с опухолью | Связанные с организмом | Связанные с окружающей средой |
| Основные | N категория M категория Статус HER2 | Остаточная болезнь: R0, R1 or R2 | |
| Дополнительные | Со стороны опухоли: кардиа или дистальный желудок Гистологический тип Инфильтрация сосудов | Возраст | Степень резекции |
| Новые и перспективные | Молекулярный профиль | Расса: Азиат или не Азиат |
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Диагностические критерии постановки диагноза
Жалобы и анамнез:
Патогномоничных симптомов рака желудка не установлено. Жалобы больного могут соответствовать проявлениям различных заболеваний желудка (хронический гастрит, язвенная болезнь желудка и т.д.):
- Боли в эпигастральной области;
- Дисфагию;
- Тошноту;
- Рвоту (в том числе «кофейной гущей»);
- Потеря аппетита;
- Снижение веса.
Физикальное обследование:
- Положение больного при поздних стадиях рака желудка, чаще вынужденное с выраженной адинамией.
- При осмотре лица – может встречаться уменьшение блеска и живости глаз.
- Бледность кожных покровов может быть указанием на желудочно-кишечное кровотечение. Восковидный или землистый оттенок приобретают кожные покровы у больных с поздними стадиями рака желудка.
- В некоторых случаях при развитии метастазов в симпатические узлы брюшной полости можно наблюдать и выраженную диффузную гиперпигментацию кожных покровов.
- В далеко зашедших стадиях рака желудка отмечаются также сухость кожи и снижение ее тургора.
- Выраженное похудание, достигающее степени кахексии, встречается при раке дистального отдела желудка. В таких случаях у больных появляются и безбелковые отеки.
- В поздних стадиях в надключичной области слева между ножками грудиноключично-сосцевидной мышцы иногда удается определить плотный лимфатический узел с неровной поверхностью, не спаянный с прилегающей кожей (метастаз Вирхова).
- При осмотре полости рта у больных раком желудка может появиться зловонный запах изо рта – признак распада злокачественной опухоли желудка.
- Выбухание стенки живота в подложечной области наблюдается при запущенных формах рака желудка. При резком похудании в ряде случаев удается визуально определить контуры желудка, его малую и большую кривизну.
- При развитии опухолевого стеноза привратника у некоторых больных определяются периодические волнообразные движения, приподнимающие в ограниченных участках переднюю брюшную стенку, которые становятся более отчетливыми после предварительного легкого поколачивания брюшной стенки в эпигастральной области.
- При пальпации передней брюшной стенки опухоли желудка отчетливо пальпируются в тех случаях, если они располагаются преимущественно в дистальных отделах желудка (антральном, пилорическом) и достигают нескольких сантиметров в диаметре.
- При перкуссии можно уточнить положение нижней границы желудка, обнаружить изменение пространства Траубе (при раке субкардиального отдела желудка).
Лабораторные исследования:
Цитологическое исследование
(увеличение размеров клетки вплоть до гигантских, изменение формы и количества внутриклеточных элементов, увеличение размеров ядра, его контуров, разная степень зрелости ядра и других элементов клетки, изменение количества и формы ядрышек);
Гистологическое исследование (крупные полигональные или шиповидные клетки с хорошо выраженной цитоплазмой, округлыми ядрами с четкими ядрышками, с наличием митозов, клетки располагаются в виде ячеек и тяжей с или без образования кератина, наличие опухолевых эмболов в сосудах, выраженность лимфоцитарно-плазмоцитарной инфильтрации, митотическая активность опухолевых клеток).
Инструментальные исследования:
- фиброэзофагогастродуоденоскопия (позволяет увидеть дефект слизистой, определить его размеры и характер, взять кусочек ткани для гистологического исследования);
- рентгеноскопическое исследование пищевода с контрастированием, рентгеноскопическое исследование желудка с контрастированием (двойное контрастирование) (позволяет определить распространенность и протяженность ЗНО желудка, а так же определить тактику хирургического вмешательства);
- ультразвуковая диагностика комплексная (печень, желчный пузырь, поджелудочная железа, селезенка, почек, надключичных л/узлов) (эхогенное наличие увеличенных л/узлов брюшной полости и забрюшинного пространства, наличие метастазов в брюшной полости, а так же прорастание ЗНО желудка в соседние структуры);
- компьютерная томография органов брюшной полости и забрюшинного пространства (более четка визуализация наличий увеличенных л/узлов брюшной полости и забрюшинного пространства, наличий метастазов в брюшной полости, а так же прорастание ЗНО желудка в соседние структуры).
- морфологическое исследование – основной метод дифференциальной диагностики рака желудка с другими заболеваниями. Обнаружение в биоптате злокачественных клеток однозначно свидетельствует о раке пищевода, хотя отсутствие признаков опухоли в однократно полученном материале не исключает это заболевание. Только при многократных отрицательных результатах наряду с динамическим наблюдением можно считать патологический процесс доброкачественным.
Показания для консультации специалистов:
- консультация кардиолога (пациентам 50 лет и старше, так же пациенты моложе 50 лет при наличии сопутствующей патологии со стороны ССС или патологических изменении на ЭКГ);
- консультация невропатолога (при сосудистых мозговых нарушениях, в том числе инсультах, травмах головного и спинного мозга, эпилепсии, миастении, нейроинфекционных заболеваниях, а также во всех случаях потери сознания);
- консультация нейрохирурга (при наличии метастазов головной мозг, позвоночник);
- консультация эндокринолога (при наличии сопутствующей патологии эндокринных органов, например – сахарный диабет).
- консультация других специалистов по поводу наличия сопутствующих патологий: гинеколога (острые и хронические заболевания женских половых органов), фтизиатра (туберкулез в анамнезе), инфекционист (хронический гепатиты) и др.
- консультация нефролога (при наличии сопутствующей патологии со стороны почек, гиперазотемия).
Дифференциальный диагноз
Дифференциальный диагноз:
| Язвенная болезнь | Полипы желудка | Лимфома желудка | Саркома желудка |
| Для исключения злокачественного характера язвы необходима множественная биопсия по краям дефекта и из дна язвы. | Для исключения злокачественного характера полипов необходима биопсия. | Часто связана с инфекцией Helicobacter pylori. | Наиболее часто представлена лейомиосаркомой, занимающей переднюю или заднюю стенку желудка. |
| обязательно выполняют ФЭГДС и биопсию через 8— 12 нед после установления диагноза язвенной болезни. | Размер полипов варьирует от небольшого выбухания до крупных полипоидных масс, имитирующих рак желудка. | Характерны выраженная общая слабость, быстрая утомляемость, боли в эпигастральной области, чувство быстрого насыщения, анорексия. | Характеризуется медленным ростом, изъязвлением и кровоточивостью; поражение лимфатических узлов не характерно. |
| Необходимо помнить о возможности заживления язвенной формы рака желудка на фоне противоязвенной терапии. | Полипы, как правило, бывают случайной находкой при ФЭГДС или рентгеновском обследовании. | Для верификации и типирования необходима глубокая биопсия с иммуно- гистохимическим исследованием, наиболее часто речь идет о В-клеточной лимфоме. | Для верификации и типирования необходима биопсия для верификации диагноза. |
| При отсутствии атипичных клеток рекомендовано консультация гастроэнтеролога с назначением противоязвенной терапии с последующим контрольным ФЭГДС через месяц. | Рекомендовано эндоскопическое удаление с гистологическим исследованием и дальнейшим наблюдением у гастроэнтеролога; Контрольный ФЭГДС каждые 3 месяца в течении трех лет. | Рекомендовано дальнейшее лечение у онкогематологов. Показания к оперативному лечению при лимфоме желудка: кровотечение угрожающее жизни. | Рекомендовано оперативное лечение первым этапом при операбельности процесса с последующим проведением курсов химиотерапии. |
Лечение
Препараты (действующие вещества), применяющиеся при лечении
| Апрепитант (Aprepitant) |
| Бевацизумаб (Bevacizumab) |
| Гранисетрон (Granisetron) |
| Дакарбазин (Dacarbazine) |
| Дарбэпоэтин альфа (Darbepoetin alfa) |
| Дексаметазон (Dexamethasone) |
| Доцетаксел (Docetaxel) |
| Железа (III) гидроксид декстран (Ferric (III) hydroxide destrane) |
| Железа (III) гидроксид сахарозный комплекс (Ferric (III) hydroxide sacharose complex) |
| Железа карбоксимальтозат (Ferric carboxymaltosate) |
| Иматиниб (Imatinib) |
| Интерферон альфа (Interferon alfa) |
| Иринотекан (Irinotecan) |
| Кальция фолинат (Calcium folinate) |
| Капецитабин (Capecitabine) |
| Карбоплатин (Carboplatin) |
| Ленограстим (Lenograstim) |
| Липэгфилграстим (Lipegfilgrastim) |
| Нетупитант (Netupitant) |
| Оксалиплатин (Oxaliplatin) |
| Октреотид (Octreotide) |
| Оланзапин (Olanzapine) |
| Ондансетрон (Ondansetron) |
| Паклитаксел (Paclitaxel) |
| Палоносетрон (Palonosetron) |
| Пембролизумаб (Pembrolizumab) |
| Пэгфилграстим (Pegfilgrastim) |
| Рамуцирумаб (Ramucirumab) |
| Ролапитант (rolapitant) |
| Сунитиниб (Sunitinib) |
| Темозоломид (Temozolomide) |
| Трастузумаб (Trastuzumab) |
| Трописетрон (Tropisetron) |
| Филграстим (Filgrastim) |
| Фолиевая кислота (Folic acid) |
| Фосапрепитант (Fosaprepitant) |
| Фторурацил (Fluorouracil) |
| Цианокобаламин (Cyanocobalamin) |
| Цисплатин (Cisplatin) |
| Эверолимус (Everolimus) |
| Эмпэгфилграстим (Empegfilgrastimum) |
| Эпирубицин (Epirubicin) |
| Эпоэтин альфа (Epoetin alfa) |
| Эпоэтин бета (Epoetin Beta) |
| Эпоэтин тета (Epoetin theta) |
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ
Немедикаментозное лечение
Соблюдение диеты №1 для больных раком желудка — пожизненное.
Ношение бандажа, ограничение физической нагрузки – в течении 6-и месяцев;
Медикаментозное лечение
Химиотерапия – это медикаментозное лечение злокачественных раковых опухолей, направленное на уничтожение или замедление роста раковых клеток с помощью специальных препаратов, цитостатиков. Лечение рака химиотерапией происходит систематически по определенной схеме, которая подбирается индивидуально. Как правило, схемы химиотерапии опухолей состоят из нескольких курсов приема определенных комбинаций препаратов с паузами между приемами, для восстановления поврежденных тканей организма.
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ
Карта наблюдения пациента, маршрутизация пациента: нет.
- полное или частичное удаление органа со злокачественным новообразованием; достижение полной или частичной регрессии, стабилизации опухолевого процесса
Лечение в зависимости от стадии; Стадии 0, I А, I В, IIА, IIВ:
- Дистальная субтотальная гастрэктомия.
- Проксимальная субтотальная гастрэктомия.
- Лапароскопическая дистальная гастрэктомия (при наличия соответствующего оборудования)
- Гастрэктомия (тотальная).
- Эндоскопическая мукозэктомия (Tis или T1а) при условии овладения техники проведения операций).
- Обязательным компонентом стандартных операций является лимфодиссекция в объеме D2. Стадии заболевания Т3, N1-2 предполагают курсы адъювантной полихимиотерапии.
Стадии IIIА, IIIВ, IIIС
- Гастрэктомия.
- Обязательным компонентом стандартных операций является лимфодиссекция в объеме D2. Установление до операции местнораспространенной формы (Т3-Т4), наличие метастазов в регионарных (N1-N2), а также низкодифференцированные гистологические формы опухолевого процесса предполагает проведение курсов (2- 3) неоадъювантной лекарственной терапии при условии согласия пациентов на проведение лекарственной терапии в предоперационном режиме, а также отсутствием противопоказаний к ней (опухолевые стенозы, кровотечения и др.).
- Адъювантные курсы полихимиотерапии с учетом ответа опухоли на проводимую предоперационную лекарственную терапию.
Стадия IV
- Оперативное лечение с паллиативной целью, например при опухолевой обструкции, перфорации или сильного кровотечения. Может быть выполнена циторедуктивная гастрэктомия, гастро-энтероанастомоз. Лимфодиссекция не выполняется. Могут рассматриваться варианты гастростомии и/или еюностомии, а также стентирование при желудочной обструкции.
- Адъювантные курсы полихимиотерапии;
- Самостоятельные курсы паллиативной полихимиотерапии.
Рецидив
- различные по объему радикальные и паллиативные оперативные вмешательства;
- эндоскопическое разрушение опухоли;
- установка стентов.
Паллиативная химиотерапия (индивидуализированно)
Критерии эффективности лечения
Эффект от проведенного лечения оценивается по критериям ВОЗ:
Полный эффект – исчезновение всех очагов поражения на срок не менее 4х недель. Частичный эффект – большее или равное 50% уменьшение всех или отдельных опухолей при отсутствии прогрессирования других очагов.
Стабилизация – (без изменений) уменьшение менее чем на 50% или увеличение менее чем на 25% при отсутствии новых очагов поражения.
Прогрессирование – увеличение размеров одной или более опухолей более 25% либо появление новых очагов поражения.
Немедикаментозное лечение
Режим, диета
Двигательные режимы, используемые в больницах и госпиталях, делятся на: I — строгий постельный, II — постельный, III — палатный (полупостельный) и IV — свободный (общий).
При проведении неоадъювантной или адъювантной химиотерапии — режим III (палатный). В раннем послеоперационном периоде — режим I (строгий постельный), с дальнейшим его расширением до II, III по мере улучшения состояния и заживления швов.
Диета. Для больных в послеоперационном периоде – голод, с переходом на стол №1, 1а. Для пациентов получающих химиотерапию стол — №1, 1а.
Соблюдение диеты в послеоперационном периоде, для больных раком желудка — пожизненное.
Медикаментозное лечение
- неоадъювантная химиотерапия опухолей назначается до операции, с целью уменьшения неоперабельной опухоли для проведения операции, а так же для выявления чувствительности раковых клеток к препаратам для дальнейшего назначения после операции.
- адъювантная химиотерапия назначается после хирургического лечения для предотвращения метастазирования и снижения риска рецидивов.
- лечебная химиотерапия назначается для уменьшения метастатических раковых опухолей.
Показания к химиотерапии:
- гистологически верифицированные ЗНО желудка;
- при лечении нерезектабельных опухолей;
- отдаленные метастазы или отдаленных лимфатических узлах;
- рецидив опухоли;
- удовлетворительная картина крови у пациента: нормальные показатели гемоглобина и гемокрита;
- сохраненная функция печени, почек, дыхательной системы и ССС;
- возможность перевода неоперабельного опухолевого процесса в операбельный;
- отказ пациента от операции;
- улучшение отдаленных результатов лечения при неблагоприятных гистотипах опухоли (низкодифференцированный, недифференцированный).
Противопоказания к химиотерапии:
Противопоказания к химиотерапии можно разделить на две группы: абсолютные и относительные.
Абсолютные противопоказания:
- гипертермия >38 градусов;
- заболевание в стадии декомпенсации (сердечно-сосудистой системы, дыхательной системы печени, почек);
- наличие острых инфекционных заболеваний;
- психические заболевания;
- неэффективность данного вида лечения, подтвержденная одним или несколькими специалистами;
- распад опухоли (угроза кровотечения);
- тяжелое состояние больного по шкале Карновского (таблица см. приложение 1) 50% и меньше.
Относительные противопоказания:
- беременность;
- интоксикация организма;
- активный туберкулез легких;
- стойкие патологические изменения состава крови (анемия, лейкопения, тромбоцитопения);
- кахексия.
ПРЕДОПЕРАЦИОННАЯ ХИМИОТЕРАПИЯ
- Фторурацил и оксалиплатин:
Оксалиплатин 85 мг/м2 в/в в 1 день;
Кальция фолинат (или натрия фолинат) 200 мг/м2 в/в в 1-й день
Фторурацил 2600 мг/м2 в/в в непрерывной инфузии в течение 24 часов в 1 день — цикл каждые 14 дней;
- FLOT
- Фторурацил и цисплатин
ПРЕДОПЕРАЦИОННАЯ ХИМИОЛУЧЕВАЯ ТЕРАПИЯ
- Паклитаксел и карбоплатин
- Фторурацил и оксалиплатин
- Капецитабин и оксалиплатин
- Фторурацил и цисплатин
- Капецитабин и цисплатин
- Паклитаксел и Фторурацил
Паклитаксел 45-50 мг/м2 в/в в 1-й день;
Капецитабин 625-825 мг/м2 внутрь, в 1-5 дни в течение 5 недель.
- Фторурацил (болюс) и Кальция фолинат (или натрия фолинат) (УД-А)
Цикл 2 (с облучением)
Кальция фолинат (или натрия фолинат) 20 мг/м2 в/в струйно на 1-4 дни и 31-33 дни;
Фторурацил 400 мг/м2 в/в струйно ежедневно на 1-4 и 31-33 дни;
Цикл каждые 35 дней.
1 цикл до и 2 цикла после химиолучевой теарпии:
Капецитабин 750-1000 мг/м2 внутрь, в 1-14 дни. Цикл каждые 28 дней.
2 цикла до и 4 цикла после химиолучевой терапии:
Кальция фолинат (или натрия фолинат) 400 мг/м2 в/в в 1-й день;
Фторурацил 400 мг/м2 в/в струйно в 1-й день;
Фторурацил 2400 мг/м2 в/в в виде непрерывной инфузии в течение 46 часов в день в первый день;
Цикл каждые 14 дней.
Совместно с лучевой терапией:
Фторурацил 200-250 мг/м2 в/в в виде непрерывной инфузии в течение 24 часов ежедневно в 1-5 или 1-7 дни;
Еженедельно в течение 5 недель.
Совместно с лучевой терапией:
Капецитабин 625-825 мг/м2 внутрь в 1-5 или 1-7 дни в течение 5 недель.
ПОСЛЕОПЕРАЦИОННАЯ ХИМИОТЕРАПИЯ
(для пациентов, подвергшихся первичной диссекции лимфатических узлов D2).
1. Капецитабин и оксалиплатин
Капецитабин 1000 мг/м2 внутрь в 1-14 дни;
Оксалиплатин 130 мг/м2 в/в в 1-й день;
Цикл каждые 21 день — 8 курсов.
СИСТЕМНАЯ ТЕРАПИЯ ДЛЯ МЕТАСТАТИЧЕСКОГО ИЛИ МЕСТНО-РАСПРОСТРАНЕННОГО РАКА (ПРОВЕДЕНИЕ ЛОКАЛЬНОГО ЛЕЧЕНИЯ НЕ ПОКАЗАНО)
- Трастузумаб (с химиотерапией)
- Фторурацил и цисплатин
Цисплатин 50 мг/м2 в/в ежедневно в 1день;
Кальция фолинат (или натрия фолинат) 200 мг/м2 в/в в 1 день;
Фторурацил 2000 мг/м2 в/в в виде непрерывной инфузии в течение 24 часов в 1 день;
Цикл каждые 14 дней.
- Фторурацил и оксалиплатин
Оксалиплатин 85 мг/м2 в/в в 1 день;
Кальция фолинат (или натрия фолинат) 200 мг/м2 в/в в 1 день.
Фторурацил 2600 мг/м2 в/в в виде непрерывной инфузии в течение 24 часов в 1 день;
Цикл каждые 14 дней.
Капецитабин 1000 мг/м2 внутрь, в 1-14 дни;
Оксалиплатин 130 мг/м2 в/в в 1-й день;
Цикл каждые 21 день.
- Паклитаксел с цисплатином или карбоплатином
Паклитаксел 90 мг/м2 в/в в 1 день;
Цисплатин 50 мг/м2 в/в в 1 день;
Цикл каждые 14 дней.
- Доцетаксел и цисплатин
- Фторпиримидины:
Фторурацил 800 мг/м2 в/в в виде непрерывной инфузии в течение 24 часов ежедневно в 1-5 дни;
Цикл каждые 28 дней.
- Таксаны:
Паклитаксел 135-250 мг/м2 в/в в 1 день;
Цикл каждые 21 день.
- Фтороурацил и иринотекан
- Модифицированный DCF
Доцетаксел 50 мг/м2 в/в в 1-й день;
Оксалиплатин 85 мг/м2 в/в в 1-й день;
Фторурацил 1200 мг/м2 в/в в виде непрерывной инфузии в течение 24 часов ежедневно в 1 и 2 дни;
Цикл каждые 14 дней.
- ECF
- Модифицированная ECF
Эпирубицин 50 мг/м2 в/в в 1 день;
Цисплатин 60 мг/м2 в/в в 1 день;
Капецитабин 625 мг/м2 внутрь, в 1-21 дни;
Цикл каждые 21 день.
Эпирубицин 50 мг/м2 в/в в 1 день;
Оксалиплатин 130 мг/м2 в/в в 1 день;
Капецитабин 625 мг/м2 внутрь в 1-21 дни;
Цикл каждые 21 день.
ВТОРАЯ И ПОСЛЕДУЮЩИЕ ЛИНИИ ТЕРАПИИ
- Рамуцирумаб и паклитаксел
- Таксаны:
Паклитаксел 135-250 мг/м2 в/в в 1 день;
Цикл каждые 21 день.
Паклитаксел 80 мг/м2 в/в в 1 день, еженедельно;
Цикл каждые 28 дней.
- Иринотекан
Иринотекан 150-180 мг/м2 в/в в 1 день;
Цикл каждые 14 дней.
- Фторурацил и иринотекан
- Рамуцирумаб
- Иринотекан и цисплатин
- Пембролизумаб
- Доцетаксел и иринотекан
Функционирующие НЭО G1-G3: аналоги соматостатина (симптоматическая терапия).
Октреотид 0,1 мг п/к 3 раза в сутки в течение короткого периода времени (примерно 2 недели) с целью оценки его эффективности и общей переносимости, затем Октреотид 20 мг внутримышечно 1раз/28 дней
Если в течение 3 месяцев обеспечивается адекватный контроль клинических проявлений и биологических маркеров заболевания – октреотид 10 мг внутримышечно 1раз/28 дней.
Если в течение 3 месяцев обеспечивается только частичный контроль клинических проявлений и биологических маркеров заболевания – октреотид 30 мг внутримышечно каждые 4 недели.
Распространенные нейроэндокринные опухоли толстой кишки или с неизвестной локализацией первичной опухоли – октреотид 30 мг внутримышечно 1раз/28 дней до прогрессирования.
- аналоги соматостатина,
- α-интерферон,
- эверолимус 10мг внутрь ежедневно до прогрессирования,
- эверолимус 10мг внутрь ежедневно в комбинации с октреотид 1раз/28 дней, до прогрессирования
- фторурацил+эверолимус,
- темозоломид+капецитабин,
- аналоги соматостатина Ki67>20%, G3:
- карбоплатин/цисплаин+этопозид,
- темозоломид+бевацизумаб,
- темозоломид+капецитабин+бевацизумаб,
- аналоги соматостатина
- Цисплатин — 80 мг/м² в/в капельно в 1-й день. Этопозид — 120мг/м² в/в капельно в 1-3-й день. Повторение цикла каждые 4 недели;
- Карбоплатин – AUC 4-5. Этопозид100мг/м² в/в 1-3-й день. Повторение цикла каждые 4 недели;
- Дакарбазин – 200 мг/м² в/в в 1-3-й день Эпирубицин – 25 мг/м² в/в в 1-3-й день Фторурацил – 250 мг/ м² в/в в 1-3-й день Повторение цикла каждые 3 недели;
- Темозоломид — 150 мг/ м² /сут внутрь 7 дней, перерыв 7 дней Бевацизумаб – 5 мг/кг в/в 1 раз в 2 недели
- Темозоломид — 150 мг/ м² /сут внутрь в 1 — 5-й день
- XELOX: оксалиплатин 130 мг/м 2 в 1й день, капецитабин 2000 мг/м 2 в сутки (разделить в 2 приема, утором и вечером) в 1-14й дни;
- α – интерферон 3-5 млн. ЕД п/к 3 раза в неделю. Доза подбирается индивидуально по переносимости.
Хирургическое вмешательство
Виды хирургических вмешательств:
- Комбинированная расширенная гастрэктомия с лимфодиссекцией D-2;
- Внутриплевральная проксимальная субтотальная гастрэктомия с резекцией нижней трети пищевода при кардиоэзофагеальном раке, из комбинированного левостороннего торакофренолапаротомного доступа (Osawa- Garlok).
- Внутриплевральная гастрэктомия с резекция нижней трети пищевода при раке проксимального отдела желудка с распространением на абдоминальный отдел пищевода, из комбинированного левостороннего торакофренолапаротомного доступа (Osawa- Garlok).
- Проксимальная субтотальная гастрэктомия;
- Дистальная субтотальная гастрэктомия;
- Лапароскопическая дистальная субтотальная гастрэктомия (при наличии соответственного оборудования).
Показания к хирургическому лечению:
- гистологически верифицированные операбельные ЗНО желудка;
- при отсутствии противопоказании к хирургическому лечению.
Противопоказания к хирургическому лечению при ЗНО желудка:
- наличие у больного признаков неоперабельности и тяжелой сопутствующей патологии;
- при отделенных метастазах (в печень, легкие, головной мозг и т.д.);
- при отделенных метастазах в лимфатические узлы шеи;
- при наличии опухолевых клеток в асцитической жидкости;
- обширные гематогенные метастазирования, диссеминированного опухолевого процесса;
- хронические декомпенсированные и/или острые функциональные нарушения дыхательной, сердечно-сосудистой, мочевыделительной системы;
- аллергия на препараты, используемые при общей анестезии.
Паллиативная помощь:
- При выраженном болевом синдроме лечение осуществляется в соответствии с рекомендациями протокола «Паллиативная помощь больным с хроническими прогрессирующими заболеваниями в инкурабельной стадии, сопровождающимися хроническим болевым синдромом», утвержден протоколом заседания Экспертной комиссии по вопросам развития здравоохранения МЗ РК №23 от «12» декабря 2013 года.
- При наличии кровотечения лечение осуществляется в соответствии с рекомендациями протокола «Паллиативная помощь больным с хроническими прогрессирующими заболеваниями в инкурабельной стадии, сопровождающимися кровотечением», утвержден протоколом заседания Экспертной комиссии по вопросам развития здравоохранения МЗ РК №23 от «12» декабря 2013 года.
Дальнейшее ведение
- первый год – 1 раз в 3 мес.;
- второй год – 1 раз в 6 мес.;
- в последующем, пожизненно — 1 раз в год. Методы обследования:
- фиброгастроскопия;
- рентгенконтрастное исследование пищевода, анастомоза;
- УЗИ органов брюшной полости;
- Рентгенологическое исследование легких;
- УЗИ периферических лимфатических узлов;
- пальцевое исследование прямой кишки;
- осмотр гинеколога (у женщин);
- общий анализ крови. По показаниям:
- Фиброколоноскопия;
- Ирригоскопия;
- КТ органов брюшной полостей и грудной клетки
- Ангиография сосудов брюшной полости
- МРТ органов брюшной полостей и грудной клетки;
- Сцинтиграфия костей скелета;
- Позитронно-эмиссионная томография (ПЭТ) + компьютерная томография всего тела
- Соблюдение режима питания;
- профилактика хеликобактерной инфекции;
- выявление больных атрофическими гастритам, формирование «групп риска».
- ахилическое состояние желудка;
- оставление вредных привычек: курение, алкоголь;
- эндоскопическое обследование минимум 1 раз в год людей старше 45 лет, а так же членов семей с семейным анамнезом рака желудочно-кишечного тракта.
Индикаторы эффективности лечения:
- «ответ опухоли» — регрессия опухоли после проведенного лечения;
- без рецидивная выживаемость (трех и пятилетняя);
- «качество жизни» включает кроме психологического, эмоционального и социального функционирования человека, физическое состояние организма больного
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ
Показания для плановой госпитализации:
Наличие у больного морфологически верифицированного ЗНО желудка, подлежащего специализированному лечению.
Показания для экстренной госпитализации: нет.
Информация
Источники и литература
- Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2018
- 1. Руководство по химиотерапии опухолевых заболеваний под редакцией Н.И.Переводчиковой, В.А. Горбуновой. Москва 2015г; 2. Tu Lai-Hui, Wu Tao, Jian-Ming Acad. J. Second Mil. Med. Univ.-2003; 3. Xue Zhi-giang,Wang Ru-wen. Chin. J. Clin. Thorac. And Cardiol. Surg.-2003. 4. Оkumura Meinoshi, Ohta Mitsunori Jap.J. Thorac. and Cardiov. Surg.-2001. 5. American Joint Committee on Cancer (AJCC). AJCC Cancer Staging Manual, 7th ed. Давыдов М.И., Тер-Аванесов М.Д., «Клиническая онкология», стр. 384, 2005г. 6. Soetikno R, Kaltenbac T, Yeh R. Gotoda T. Endoscopic mucosal resection for early cancers of the upper gastrointestinal tract. J Clin Oncol 2005;23:4490-4498. 7. Щепотин И.Б., «Рак желудка», 227 с., 2000г. 8. Черноусов А.Ф., Поликарпов С.А., «Расширенная лимфаденэктомия в хирургии рака желудка», 159 с., 2000г. 9. ESMO (клинические рекомендации, г.Барселона, 2013г.) 10. Bethesda Handbook of Clinical Oncolology (James Abraham, James L.Gulley, Carmen J.Allegra, 2010) 11. Oxford Handbook of Oncology (Jim Cassidy, Donald Bisset, Roy A.J.Spence, Miranda Payne, 2010) 12. Pocket Guide to Chemotherapy Protocols (Edward Chu, 2008) 13. Principles and Practice of Gastrointestinal Oncology (D.Kelsen et al., 2009) 14. NCCN guidelines 2015 http://www.nccn.org/professionals/physician 15. GLOBOCAN 2012: Estimated cancer incidence, mortality and prevalence worldwide in 2012. Accessed November 4th, 2014. 16. Yao JC, et al. Gastrointestinal Cancers Symposium; January 20‐22, 2011; San Francisco, CA. Abstract 159 17. Pavel ME, Hainsworth JD, Baudin E, et al. Everolimus plus octreotide long-acting repeatable for the treatment of advanced neuroendocrine tumours associated with carcinoid syndrome (Radianr -2): a randomized, placebo-controlled, phase 3 study. Lancet 2011;378:2005-2012.Available at: http://www.ncbi.nih.gov/pubmed/22119496. 18. ESMO Upper Gastrointestinal Cancers Guidelines 2014/ Ann Oncol 2013: 24 (Suppl): vi57-63 19. American Joint Committee on Cancer (AJCC). AJCC Cancer Staging Manual, 7th ed. Edge S.B., Byrd D.R., Carducci M.A. et al., eds. New York: Springer; 2009. 20. Murphy B.A Carcinoma of the head and neck. In: Handbook of cancer chemotherapy. Skeel R.Т., Khleif S.N.(eds). 8 th Edition. Lippincott Williams & Wilkins.2011: 69-63. 21. Руководство по химиотерапии опухолевых заболеваний. Под редакцией Н.И. Переводчиковой, В.А. Горбуновой. 4-е издание, расширенное и дополненное. Практическая медицина. Москва 2015г. 22. Санитарно-эпидемиологические требования к объектам здравоохранения 23. //Постановление Правительства Республики Казахстан от 17 января 2012 года № 87. 24. Санитарно-эпидемиологические требования к обеспечению радиационной безопасности от 3 февраля 2012 года № 202 25. Санитарные правила «Санитарно-эпидемиологические требования к обеспечению радиационной безопасности», № 202 от 03.02.2012 26. Ge L, Wang HJ, Yin D, Lei C, Zhu JF, Cai XH, Zhang GQ. Effectiveness of 5- flurouracil-based neoadjuvant chemotherapy in locally-advanced gastric/gastroesophageal cancer: a meta-analysis. World J Gastroenterol. 2012 Dec 28;18(48):7384-93. http://www.ncbi.nlm.nih.gov/pubmed/23326149 27. Nagaraja V, Eslick GD. HER2 expression in gastric and oesophageal cancer: a meta-analytic review J Gastrointest Oncol. 2015 Apr;6(2):143-54. http://www.ncbi.nlm.nih.gov/pubmed/25830034 28. Gu J, Zheng L, Wang Y, Zhu M, Wang Q, Li X. Prognostic significance of HER2 expression based on trastuzumab for gastric cancer (ToGA) criteria in gastric cancer: an updated meta-analysis. Tumour Biol. 2014 Jun;35(6):5315-21 http://www.ncbi.nlm.nih.gov/pubmed/2455754 29. Sano T, Coit D, Kim HH, et al. for the IGCA Staging Project. Proposal of a new stage grouping of gastric cancer for TNM classification: International Gastric Cancer 30. Association Staging Project. Gastric Cancer 2016; in press.
Информация
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ВНЕДРЕНИЯ ПРОТОКОЛА
Список разработчиков протокола с указание квалификационных данных:
1) Ижанов Ерген Бахчанович – доктор медицинских наук, врач ЦТО АО «Казахский научно-исследовательский институт онкологии и радиологии»;
2) Менбаев Серик Кундыкович – врач первой категории, врач ЦТО АО «Казахский научно-исследовательский институт онкологии и радиологии»;
3) Канаев Али Муладимович – врач отделения ДСХТАО «Казахский научно-исследовательский институт онкологии и радиологии» ;
4) Бабажанова Анар Бейбитовна – клинический фармаколог ООД Мангыстауской области.Указание на отсутствие конфликта интересов: нет.
Рецензенты:
1) Арзыкулов Жеткерген Анесович — доктор медицинских наук, профессор, академик РАМН.
2) Есентаева Сурия Ертугыровна – доктор медицинских наук, заведующая кафедрой онкологии и маммологии с курсом визуальной диагностики НАО «Медицинский университет Караганды».Указание условий пересмотра протокола: пересмотр протокола через 5 лет после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Приложение 1
Шкала Карновского
Оценка, % Функциональная активность 100 Нормальная; жалоб и симптомов заболевания нет 90 Способен к нормальной деятельности; незначительные симптомы заболевания 80 Нормальная деятельность с усилием; присутствуют те или иные симптомы заболевания 70 Способен к самообслуживанию; способность к нормальной деятельности утрачена 60 Самообслуживание возможно, иногда требуется посторонняя помощь 50 Способность к самообслуживанию утрачена, требуется медицинская помощь 40 Инвалид; нуждается в специализированной помощи и уходе 30 Тяжелая инвалидность; нуждается в госпитализации 20 Состояние крайне тяжелое; нуждается в госпитализации и интенсивной терапии 10 Терминальное состояние 0 Смерть Приложение 2
СОПРОВОДИТЕЛЬНАЯ ТЕРАПИЯ
Антиэметическая терапия
Тошнота и рвота являются одним из наиболее частых побочных эффектов химио- терапии (ХТ) и существенно ухудшают качество жизни больных.
Тошнота и рвота, сопутствующие химиотерапии, относятся к числу наиболее неприятных аспектов этого вида лечения (1,2). Не будучи самым серьезным побочным эффектом химиотерапии, рвота, тем не менее, сильно ухудшает качество жизни и снижает ощущение благополучия (1,3). В некоторых случаях пациенты откладывают или полностью прекращают химиотерапию из-за непереносимой тошноты и рвоты (1).
Кроме того, рвота, как таковая, может представлять угрозу здоровью, поскольку неконтролируемая рвота приводит к обезвоживанию, нарушению баланса метаболитов и к анорексии (4,5).
Факторы, связанные с терапией:
Высокая эметогенная способность некоторых препаратов,
Комбинированная терапия
Режим и способ введения препаратов
Высокие дозы химиотерапевтических препаратов (6).
Под уровнем эметогенности понимается риск развития рвоты у больных, получающих тот или иной цитостатик в монорежиме без противорвотной терапии. Например, высокий уровень эметогенности означает, что после введения препарата рвота будет развиваться более чем у 90 % больных. Классификация противоопухолевых препаратов в зависимости от уровня эметогенности по рекомендациям MASCC / ESMO представлена в табл. 1.Таблица 1. Классификация противоопухолевых препаратов в зависимости от уровня эметогенности по рекомендациям MASCC / ESMO.
Уровень эметогенности Противоопухолевые препараты для внутривенного введения Противоопухолевые препараты для приема per os Высокий (рвота у 90 % больных и более) Цисплатин
Мехлорэтамин
Стрептозоцин
Циклофосфан ≥ 1500 мг / м2 Кармустин (BCNU)
ДакарбазинГексаметилмеламин Прокарбазин Схема «АС»: • эпирубицин 100 мг / м2 или • доксорубицин 60 мг / м2 + – циклофосфамид 600 мг / м2 .
2) Режимы на основе карбоплатинаУмеренный (рвота у 30–90 % больных) Оксалиплатин
Цитарабин > 1 г / м2 Карбоплатин
Ифосфамид
Циклофосфамид < 1500 мг / м2
Доксорубицин
Даунорубицин
Эпирубицин
Идарубицин
Иринотекан
Азацитидин
Бендамустиин
Клофарабин
Алемтузумаб
Трабектидин
Ромидепсин
ТиотепаЦиклофосфамид
Темозоломид
Винорельбин
Иматиниб
Кризотиниб
Церитиниб
БосутинибНизкий (рвота у 10–30 %) (Nab-) Паклитаксел
Доцетаксел
Митоксантрон
Доксорубицин липосомальный Иксабепилон
Топотекан
Этопозид
Пеметрексед
Метотрексат
Митомицин
Гемцитабин
Цитарабин ≤ 1000 мг / м2
5-фторурацил
Винфлунин
Темсиролимус
Бортезомиб
Цетуксимаб
Трастузумаб(-эмтанзин) Панитумумаб
Катумаксумаб
Пертузумаб
Афлиберцепт
ИпилимумабКапецитабин
Тегафур
Флюдарабин
Этопозид
Сунитиниб
Эверолимус
Лапатиниб
Леналидомид
Талидомид
Афатиниб
Дабрафениб
Дазатиниб
Ибрутиниб
Олапариб
Нилотиниб
Пвзопаниб
Регорафениб
Вандетаниб
ВариностатМинимальный ( < 10 % больных) Блеомицин
Бусульфан 2-хлордеоксиаденозин Флюдарабин
Винбластин
Винкристин
Винорельбин
Бевацизумаб
Офатумумаб
Ниволумаб
Пембролизумаб
Пискантрон
ПралатрексатХлорамбуцил
Гидроксиуреа
L-фенилаланин мустард
6-тиогуанин
Метотрексат
Гефитиниб
Эрлотиниб
Сорафениб
Мелфалан
Вемурафениб
Помалидомид
Руксолитинб
ВисмодегибТИПЫ ТОШНОТЫ И РВОТЫ
По срокам и механизму развития выделяют 3 основных типа тошноты и рвоты, вызванной цитостатиками: острую, отсроченную и условно-рефлекторную (anticipatory – переводят также как «предшествующую», «преждевременную», «рвоту ожидания»), дополнительно выделяют неконтролируемую (breakthrough – «прорывную») и рефрактерную (7, 8).
Острая рвота развивается в первые 24 ч после химиотерапии, отличается высокой интенсивностью, редко сопровождается тошнотой.
Отсроченная рвота развивается на 2-е–5-е сутки после начала химиотерапии, менее интенсивна, чем острая, и, как правило, сопровождается постоянной тошнотой. Механизмы развития остаются неясными. Ведущая роль отводится субстанции P, серотонин имеет меньшее значение.
Условно-рефлекторная рвота представляет собой классический условный рефлекс на химиотерапию и / или сопутствующие ей манипуляции и окружающую обстановку. Формируется в тех случаях, когда противоопухолевая терапия сопровождается тошнотой и рвотой. Риск ее развития увеличивается пропорционально числу проведенных курсов и может сохраняться в течение длительного времени после окончания химиотерапии. Ведущую роль в формировании условного рефлекса играет многодневная умеренная или тяжелая тошнота. Лучшим методом профилактики условно-рефлекторной тошноты и рвоты является адекватная антиэметическая защита пациента уже с первого курса химиотерапии.
Неконтролируемая (breakthrough – «прорывная») тошнота и рвота развивается на фоне адекватной антиэметической профилактики и требует дополнительной коррекции. Рефрактерная рвота возникает на последующих циклах химиотерапии при неэффективности противорвотной профилактики и / или препаратов резерва на предыдущих курсах лечения.ПРИНЦИПЫ СОВРЕМЕННОЙ ПРОТИВОРВОТНОЙ ТЕРАПИИ
1. Обязательность проведения, начиная с первого курса химиотерапии.
2. Введение антиэметиков до начала введения первого цитостатика.
3. Применение наиболее эффективных стандартных противорвотных комбинаций.
4. Применение каждого антиэметика, входящего в комбинацию, в адекватных дозах.
5. Соблюдение адекватной продолжительности противорвотной терапии.
6. Соблюдение необходимых для сохранения эффективной концентрации интервалов между приемами антиэметиков.
Критерием эффективности противорвотной терапии является полное отсутствие (полный контроль) рвоты и тошноты в течение 24 часов (период развития острой рвоты) с момента введения противоопухолевых препаратов.Алгоритм профилактики и терапии тошноты и рвоты
1. Определить эметогенный потенциал назначенного режима ХТ.
2. Назначить профилактическую терапию, исходя из эметогенности режима ХТ.
3. Назначить лечение в случае развития тошноты и рвоты на фоне профилактической терапии.
4. Внести изменения в профилактическую терапию тошноты / рвоты на последующих циклах ХТ.Антиэметики:
I. Антагонисты серотониновых рецепторов (5-HT3):- Ондансетрон (УД — А)
- Гранисетрон (УД — А)
- Трописетрон (УД — А)
- Палоносетрон (УД — А)
II. Кортикостероиды: Дексаметазон (УД — А)
III. Антагонисты рецепторов NK1 :
- Апрепитант (УД — А)
- Фосапрепитант (УД — А)
- Ролапитант (УД — А)
- Нетупитант (УД — А)
IV. Антипсихотическое средство (нейролептик):
- Оланзапин (УД — А) (проявляет антагонизм в отношении серотониновых 5-НТ-, допаминовых и холинорецепторов).
Профилактика острой и отсроченной тошноты и рвоты при высокоэметогенной однодневной химиотерапии и при умеренно эметогенной однодневной химиотерапии.
В настоящее время наиболее эффективной антиэметической комбинацией при высокоэметогенной однодневной химиотерапии является комбинация противорвотных препаратов, включающая антагонистов NK1-рецепторов + антагонистов рецепторов серотонина (5-HT3) + дексаметазон.
Профилактика тошноты и рвоты, возникающей при проведении химиотерапии с умеренно эметогенным потенциалом, должна начинаться до начала химиотерапии и проводиться не менее 3 дней после проведения химиотерапии. Наиболее эффективной антиэметической комбинацией является комбинация противорвотных препаратов, включающая антагонистов рецепторов серотонина (5-HT3) + дексаметазон (табл 2,3) (9, 10).Таблица 2. Обновленные рекомендации MASCC/ESMO 2016 ТРВХ.
Острая тошнота и рвота.Группы эметогенного риска Антиэметики Высокий (не АС) 5-НТ3 + DEX+NK 1 Высокий (АС) 5-НТ3 + DEX+NK 1 Карбоплатин 5-НТ3 + DEX+NK 1 Умеренный (кроме карбоплатина) 5-НТ3 + DEX Низкий 5-НТ3 или DEX или DOP Минимальный Нет рутинной профилактики ТРВХ – тошноты и рвота, вызванная химиотерапией
MASCC — Multinational Association of Supportive Care in Cancer; ESMO – European Society for Medical Oncology
5-НТ3 — антогонисты серотиновых рецепторов
DEX— дексаметазон
NK 1 — антагонисты рецепторов нейрокинина такие как Апрепитант или
Фосапрепитант или
Ролапитант или NEPA (комбинация нетупитант и палоносетрон).
DOP— антогонист допаминовых рецепторов
ВНИМАНИЕ: Если антагонисты NK1 рецепторов недоступны при использовании схемы AC, палоносетрон является предпочтительным антагонистом 5-НТ3 рецепторов.Таблица 3. Обновленные рекомендации MASCC/ESMO 2016 ТРВХ.
Отсроченная тошнота и рвота.Группы эметогенного риска Антиэметики Высокий (не АС) DEX или (если APR 125мг для острой: (МСР+DEX) или (DEX+APR) Высокий (АС) Нет или (если APR 125мг для острой:APR+DEX) Карбоплатин Нет или (если APR 125мг для острой:APR) Средний (не карбоплатин) DEX можно использовать Низкий Профилактика не предусмотрена Минимальный Профилактика не предусмотрена DEX — дексаметазон
APR — апрепитант
MCP — метоклопромидКлючевые обновления в рекомендациях по контролю ТРВХ, NCCN 2017:
Карбоплатин категоризируется как высокоэметогенный препарат при введении с площадью под кривой (ППК) ≥4, при введении с ППК Инъекция подкожного гранисетрона пролонгированного действия теперь включена в рекомендации по профилактике тошноты и рвоты при высокоэмегоненной и умеренноэметогенной ХТ.
Новая схема профилактики ТРВХ из четырех препаратов теперь включена в рекомендации по профилактике ТРВХ при высокоэметогенной ХТ (11, 12).Ключевые обновления в рекомендациях по контролю ТРВХ, ASCO 2017:
Взрослым пациентам, получающим высокоэметогенную химиотерапию цисплатином, либо комбиницией циклофосфамидов и антрациклина, к стандартному антиэметическому режиму (комбинация антагонистов рецепторов 5-НТ3 + антагонисты рецепторов NK1 + dex) следует добавить оланзапин.
Взрослым пациентам, получающим карбоплатин содержащую химиотерапию, а также детям, получающим высокоэметогенную химиотерапию, антагонисты рецепторов NK1 должны быть добавлены к стандартному антиэметическому режиму (комбинация антагонистов рецепторов 5-НТ3 + dex).
Если пациенты получают комбинацию антрациклина и циклофосфамида, прием дексаметазона можно ограничить с первым днем химиотерапии.Экспертная комиссия рекомендует начинать антиэметическую терапию с самой эффективной схемы, подходящей к химио- и радиотерапии, вместо того чтобы оценивать эметический ответ пациента на менее эффективную антиэметическую терапию (13).Таблица 4. Обновленные рекомендации ASCO 2017.
Взрослые пациенты.Группы эметогенного риска Антиэметики Высокий (не АС) 5-НТ3 + DEX* +NK 1+Olanzapine* Высокий (АС) 5-НТ3 + DEX* +NK 1+Olanzapine* Карбоплатин 5-НТ3 + DEX+NK 1 Умеренный (кроме карбоплатина) 5-НТ3 + DEX Низкий 5-НТ3 или DEX или DOP Минимальный Нет рутинной профилактики * — дексаметазон и оланзапин нужно продолжать на 2-4 день
Таблица 5. Рекомендуемые дозы антогонистов серотониновых рецепторов (5-НТ) для острой тошноты и рвоты.
Препарат Путь введения Доза Ондансетрон в/в 8мг или 0,15мг/кг пероральный 16мг* Гранисетрон в/в 1мг или 0,01мг/кг пероральный 2мг (или 1мг**) Трописетрон в/в 5мг пероральный 5мг Палоносетрон в/в 0,25мг пероральный 0,5мг * В рандомизированных исследованиях был протестирован режим 8 мг два раза в день.
** Некоторыми панелистами доза 1 мг более предпочтительнаТаблица 6. Рекомендуемые дозы кортикостероидов (дексаметазон)*
Дексаметазон Дозы и Кратность Высокий риск Острая рвота 20мг однократно (12мг когда используется апрепитант или нетупитант) )** Отсроченная рвота 8мг в течение 3-4 дней (8мг один раз в день когда используется апрепитант или нетупитант ) Умеренный риск Острая рвота 8 мг однократно Отсроченная рвота 8 мг ежедневно в течение 2-3
днейНизкий риск Острая рвота 4-8 мг один раз в день * Несмотря на то, что другие кортикостероиды также являются эффективными антиэметиками, режим дозирования для дексаметазона, как препарата выбора, основан на широком распространении препарата, с несколькими формами дозирования
** Только 12 мг дексаметазона было исследовано с (фос) апрепитантами/нетупитантами в рандомизированных исследованияхТаблица 7. Рекомендуемые дозы антагонистов NK1 рецепторов.
Антагонисты NK1 Рецепторов Дозы и кратность Апрепитант* и фосапрепитант
острая рвотаАпрепитант 125мг внутрь однократно в день химиотерапии*
-или- Фосапрепитант 150 в/в, однократно в день химиотерапииАпрепитант* и фосапрепитант
отсроченная рвотаАпрепитант 80мг внутрь однократно в течении 2-х дней после химиотерапии Ролапитант 180мг внутрь однократно в день химиотерапии Нетупитант 300 мг нетупитант / 0,5 мг палоносетрон перорально один раз в день химиотерапии * Апрепитант 165 мг, одна доза перед химиотерапией (не применяется на 2-3 день). Рекомендовано ЕМА и другими органами.
Рекомендации по профилактики преждевременной тошноты и рвоты
Наилучший подход для профилактики преждевременной рвоты это наилучший контроль над острой и отсроченной рвотой.
Психотерапия, особенно прогрессивное обучение мышечной релаксации, систематическая десенситизация и гипноз, могут быть использованы для лечения преждевременной тошноты и рвоты.
Только бензодиазепины уменьшают частоту преждевременной тошноты и рвоты, но их эффективность имеет тенденцию к снижению при продолжающейся химиотерапии.Кардиотоксичность
Кардиотоксичность возникает в основном при лечении антрациклинами- доксорубицин, фарморубицин, даунорубицин- и редко при использовании других препаратов: циклофосфамид, фторурацил, этопозид, тенипозид, паклитаксел, трастузумаб, лапатиниб. Различные препараты по разному воздействуют на сердечно- сосудистую систему в связи с неодинаковым механизмом кардиотоксичости: препараты, вызывающие снижение сократительной или расслабляющей функции миокарда(антрациклины), препараты, вызыващие или обостряющие ишемию(фторурацил, винкристин, винбластин, цисплатин), препараты, влияющие на проводящую систему, в результате чего возникает аритмия/ блокада проводимости(антрациклины, паклитаксел).
Основной способ предупреждения развития кардиотоксичности I типа(необратимые повреждения) при лечени анрациклинами- соблюдение предельных суммарных доз препаратов(доксорубицин ˃550мг/м2, фарморубицин ˃720мг/м2), использование пегилированного липосомного доксорубиина (келикс ˃900мг /м2). Необходмио раннее выявление кардиотоксичности с помощью Эхо КГ и ЭКГ(для пациентов всех возрастов при планировании системной ХТ препаратами антрациклинового ряда, трастузумабом- перед каждым введением, при назначении препаратов таксанового ряда, циклофосфамид, лапатиниб, этопозид, фторурацил- каждые 3 месяца).
При снижении Фракции выброса до 55-50%, необходима отсрочка введения химиопрепаратов до восстановления ФВ в норму, консультация кардиолога.
При снижении ФВ 50% и менее необходима отсрочка системного лечения до 3 месяцев, проведение коррегирующего лечения по назначению кардиолога.Колониестимулирующая терапия:
Целесообразность назначения Г-КСФ для стимуляции кроветворения и преодоления миелосупрессии при фебрильной нейтропении (ФН) изучалась в нескольких рандомизированных исследованиях. На основании имеющихся данных сделаны следующие выводы относительно роли Г-КСФ в период ФН:- Г-КСФ статистически значимо снижает длительность нейтропении на 1–2 дня;
- Г-КСФ не сокращает продолжительность лихорадки и длительность антибактериальной (АБ) терапии в случае развития ФН;
- Г-КСФ не снижает стоимости лечения одного эпизода ФН.
- Г-КСФ могут применяться в случае высокого риска ФН при состояниях, сопровождающихся повышенной смертностью, таких как гипотония, сепсис, пневмония, инфекции тканей, системная грибковая инфекция, длительная нейтропении (>7 дней) или глубокой нейтропении.
Большинство медицинских онкологических сообществ (NCCN, ASCO, EORTC, RUSSCO) рекомендуют использовать следующие Г-КСФ: липэгфилграстим, эмпэгфилграстим, пэгфилграстим (филграстим, соединенный с полиэтиленгликолем), филграстим (негликозилированный Г-КСФ), ленограстим (гликозилированный Г-КСФ). Липэгфилграстим, эмпэгфилграстим и пэгфилграстим представляют собой препараты пролонгированного действия и вводятся однократно после курса ХТ. Пролонгированное действие обусловлено тем, что препарат не выводится с мочой и дольше циркулирует в крови.
Таблица 8. Перечень препаратов Г-КСФ
МНН Группа КСФ Режим введения Филграстим* Рекомбинантный человеческий негликолизированный Г-КСФ 5 мкг/кг массы тела 1 раз/сут. п/к или в/в ежедневно через 24–72 часа после последнего дня ХТ до необходимого стабильного АЧН Пэгфилграстим* Рекомбинантный пегилированный Г-КСФ (филграстим), конъюгированный с полиэтиленгликолем, пролонгированного действия 6 мг (без учета массы тела) однократно п/к не ранее чем через 24 часа и не позднее 14-ых сут. после курса ХТ Липэгфилграстим* Гликопегилированный Г-КСФ пролонгированного действия 100 мкг/кг или 6 мг (без учета массы тела) п/к однократно через 24 ч после окончания цикла ХТ Эмпэгфилграстим* Ковалентный коньюгат филграстима с одной молекулой полиэтиленгликоля, пролонгированного действия 7,5 мг (без учета массы тела) п/к однократно не ранее чем через 24 часа и не позднее 14-ых сут. после курса ХТ Ленограстим* Рекомбинантный человеческий гликолизированный Г-КСФ 19,2 млн. МЕ (или 150 мкг) на м² поверхности тела (0,64 млн. МЕ или 5 мкг на кг массы тела) в день п/к или в/в ежедневно через 24–72 часа после последнего дня ХТ до достижения необходимого стабильного АЧН Таблица 9. Показания для назначения колониестимулирующих факторов
- при режимах ХТ с высоким риском ФН (≥20%);
- в других ситуациях, ассоциирующихся с высоким риском ФН:
- – небольшой резерв костного мозга (АЧН
- – ВИЧ-инфекция;
- – пациенты в возрасте ≥65 лет, получающие ХТ с целью излечения;
- – для обеспечения оптимальной интенсивности лечения в тех случаях, когда редукция доз цитостатиков может негативно влиять на сроки жизни.
- Вероятность возникновения жизнеугрожающей инфекции во время следующего курса ХТ;
- невозможность изменить протокол лечения (редукция доз цитостатиков ниже порогового уровня или увеличение интервала между курсами ХТ);
- нейтропения, не позволяющая начать ХТ;
- модификация режима лечения (интервал, дозы) может привести к уменьшению эффективности (частоты эффектов, времени без прогрессирования и общей выживаемости).
- на фоне ЛТ; показано только при вероятном или очевидном риске смерти пациента из-за угнетения функции костного мозга на фоне ЛТ, при этом РОД от 3 до 10 Гр.
Коррекция анемии:
Анемия при новообразованиях (В63.0 код по МКБ 10) определяется как снижение концентрации Hb ниже нормального значения (обычно 120 г/л) и может быть обусловлена как наличием самой опухоли, так и ее лечением. Слабая степень анемии представляет собой снижение концентрации Hb в диапазоне от 100 до 119 г/л, анемия средней степени – концентрация Hb от 80 до 99 г/л, тяжелая анемия – концентрация Hb ниже 80 г/л.Таблица 10. Препараты рекомендованные для лечения анемии у онкологических больных
Как не пропустить симптомы рака желудка? Это важно!
Рак желудка является одним из наиболее распространенных и в то же время коварных онкологических заболеваний. По частоте смертных случаев он расположен на втором месте, уступая только раку легких. Причина высокой смертности при данном заболевании кроется в сложности своевременной диагностики. Определить болезнь на ранних стадиях очень непросто, так как симптомы при раке желудка зачастую бывают очень смазаны и больные чаще всего не обращают на них внимания. А на более поздних стадиях это заболевание уже плохо поддается лечению.
Рак желудка и особенности его проявления
Язва, переросшая в рак
При обращении к врачу и диагностировании рака на его ранних стадиях, возможность полного избавления от недуга очень высока, а процент пятилетней выживаемости приближается к 80-90%. Но, в большинстве случаев постановка диагноза «рак желудка» происходит уже на более поздних стадиях, что намного снижает коэффициент пятилетней выживаемости. Поэтому следует знать первые, наиболее часто встречающиеся симптомы рака и при малейших подозрениях проходить более детальное обследование.
Симптомы рака желудка не всегда одинаковы у разных пациентов. В зависимости от места расположения опухоли и ее гистологического типа симптомы могут существенно различаться. На месторасположение опухоли в кардиальном отделе желудка (части, прилегающей к пищеводу) в первую очередь указывают трудности с проглатыванием грубой еды или ее больших кусков, повышенное выделение слюны. С ростом опухоли симптомы становятся все выразительнее. Через некоторое время развиваются и другие признаки опухоли: рвота, чувство тяжести в груди, между лопаток или в области сердца, болезненность.
Если первичная опухоль находится нижней части желудка (так называемом антральном отделе), то и симптомы будут немного другими. В таких случаях больной жалуется на рвоту, ощущение тяжести, неприятный запах с ротовой полости или от рвотных масс. На поражение опухолью тела свидетельствуют общеонкологические проявления: отсутствие аппетита, слабость, головокружение, анемия, похудение и т.д. Ярко выраженных симптомов в случае опухоли средней части желудка не наблюдается.
В зависимости от наличия и характера симптомов, врач может определить необходимость и виды дальнейшей диагностики. Но все-таки симптомов рака желудка существует значительно большее количество, чем описано выше.
Симптомы рака желудка на его начальных стадиях
Наиболее ранние признаки рака настолько смазаны и невыразительны, что лечение в случае их проявления начинают в крайне редких случаях и, как правило, не соответствующе заболеванию. Ведь схожие проявления имеют большинство заболеваний желудочно-кишечного тракта, и диагностировать по ним рак крайне трудно. Но, все-таки, наиболее вероятные симптомы рака выделить можно. К ним относятся:
- Расстройство пищеварительного процесса. Это и изжога, частая отрыжка, метеоризм, вздутие, ощущение тяжести в желудке. Эти симптомы отмечали многие больные, даже на протяжении многих лет своей жизни. Но попадали к врачу-онкологу только при наличии других более серьезных симптомов.
- Дискомфортные ощущения, локализирующиеся в районе грудной клетки. К таким проявлениям относятся боль, чувство распирания , тяжести или любые другие проявления дискомфорта. . Тошнота может преследовать пациента сразу после каждого приема пищи и доставлять неудобство на протяжении длительного времени.
- Трудности при глотании. Этот признак возникает только при образовании опухоли в верхнем отделе желудка. Она может частично препятствовать прохождению пищи, что объясняет этот признак. На ранних этапах трудности возникают только касательно грубой пищи или больших комков. Но с развитием заболевания становится труднее проглатывать даже мягкие и жидкие продукты.
- Рвота. Зачастую только появление таких симптомов как рвота и тошнота приводят пациента на обследование. Рвота может быть единоразовым или периодическим явлением, возникать сразу после еды или вообще не быть связанной с приемом пищи. Наиболее страшным проявлением является рвота с кровью алого или коричневого цвета. В дополнение к небольшим, но стабильно повторяющимся кровотечениям присоединяется анемия, бледность, отдышка , быстрая утомляемость.
- Наличие в кале крови. Это еще один симптом желудочного кровотечения и опухоли желудка. Его можно диагностировать в лабораторных условиях или визуально по цвету кала, который в таком случае дегтярно-черный.
- Болезненные ощущения. Зачастую болезненность ощущается в области грудной клетки, но также боль может распространяться и по направлению к лопатке или к сердцу.
- Общеклинические симптомы. После развития опухоли и возникновения метастаз за пределами желудка могут проявляться и общие для всех онкологических заболеваний симптомы: потеря веса, снижение аппетита, утомляемость, анемия, вялость и т.д.
- Вторичные симптомы. Новые симптомы свидетельствуют о появлении вторичных опухолей. Симптомы могут быть самыми разнообразными и зависеть от направления возникновения метастаз.
Перечень вышеуказанных симптомов является далеко не полным, но именно эти симптомы должны насторожить больного и заставить пройти обследование для начала своевременного лечения.
Диспепсия, как характерный признак рака желудка

Диагностика рака — достаточно сложный процесс
Довольно часто пациент приходит к врачу с весьма обычным симптомом – диспепсией. Диспепсией называют нарушение нормальной работы желудка, расстройство пищеварения. В этом случае задачей врача является проведение полного обследования с целью выявить первопричину такого расстройства. Диспепсия характеризуется следующими симптомами:
- ощущение переполнения желудка;
- снижение или потеря аппетита;
- снижение размера употребляемой порции;
- отвращение к любимой ранее еде, зачастую белковой (мясо, рыба);
- тошнота, рвота;
- отсутствие удовольствия при приеме пищи.
Если проявляется один из вышеперечисленных симптомов, паниковать не стоит, но сочетание нескольких должно насторожить пациента и заставить обратится к соответствующему специалисту для проведения досконального обследования.
Диагностика рака желудка в лабораторных условиях
У большинства пациентов (60-85 %) наблюдаются симптомы анемии, вызванные хронической кровопотерей и отравляющим воздействием метаболитов опухолевых клеток на красный костный мозг. При проведении исследования на скрытую кровь в каловых массах положительный результат имеется в 50-90 % случаев. Также исследуют содержимое желудка на уровень кислотности и увеличение активности бета-глукуронидазы.
Дифференциальная диагностика
Прежде всего, рак желудка следует разграничить с доброкачественными опухолями желудка и язвенной болезнью. Окончательно подтвердить диагноз «рак желудка» во всех случаях может только прицельная гастробиопсия .
Рак желудка на фоне язвенной болезни
Заподозрить опухоль при наличии язвенной болезни можно по следующим признакам:
- неровность краев язвы, подрытость одного края и возвышение другого;
- нетрадиционная форма язвы ( амебоподобная );
- утолщение слизистой оболочки по окружности язвы, зернистость слизистой;
- ярко-красный цвет краев язвы;
- кровоточащая, бледная, вялая слизистая оболочка вокруг язвы;
- дно язвы серого цвета, зернистое, неглубокое, относительно плоское;
- изъязвления краев язвы.
При наличии таких симптомов пациенту следует провести прицельную гастробиопсию , образцы ткани обязательно нужно брать и из дна язвы, и из ее краев.
Рак желудка и полипы
Оперативное вмешательство для лечения рака желудка
Полипозный рак желудка – это опухоль, имеющая значительные размеры (до 2 см), похожа на узел на ножке с широким основанием. Поверхность полипа по виду схожа с цветной капустой, на верхушке образования могут наблюдаться язвы, эрозии, отеки, некрозы . Если полип имеет небольшой размер, ненарушенную слизистую оболочку, маленькую ножку с узким основанием, то это говорит о доброкачественности опухоли.
Большинство таких полипов гиперпластические . Но не стоит забывать о частых случаях (около 40%) малигнизации (приобретение клетками свойств злокачественной опухоли) аденоматозных полипов. Полипы, имеющие широкое основание и значительный размер всегда подлежат удалению с дальнейшим исследованием их строения
Другие виды опухолей желудка
Другие виды доброкачественных опухолей встречаются крайне редко. Признаки доброкачественности опухоли всегда явные – это ненарушенная слизистая, сохранение складчастости и перистальтики, слизистая оболочка имеет стандартный, неизмененный цвет (только при ксантоме слизистая имеет желтый цвет).
Макроморфология опухолей желудка
Экзофитные опухоли (имеющие вид бляшки, узла, выступающие над поверхностью ткани), как правило, растут в просвет органа и отделены от здоровых тканей. Они характеризуются меньшей злокачественностью и более медленным распространением и метастазированием.
Полиповидная опухоль встречается в 3-10 % случаев и внешне напоминает шляпу гриба с широким основанием цилиндрической формы, или полипа с высокой ножкой темно-красного цвета, на поверхности которого просматриваются эрозии, отложения фибрина. Располагается преимущественно в антральном отделе или теле желудка, чаще на малой кривизне. Изменения слизистой оболочки отсутствуют. Полиповидная опухоль может быть различного размера: как в несколько миллиметров, так и несколько сантиметров и разрастаться в просвет желудка, занимая его полностью.
Блюдцеобразный (чашеобразный) рак встречается в 10-40 % случаях опухолей и являет собой опухоль с широким основанием, в центре которой находится распад, имеющий вид язвы с широкими, приподнятыми краями, похожими на валики. Дно язвы имеет неровную поверхность, покрыто налетом темно-коричневого или грязно-серого цвета. В углублении язвы можно заметить сгустки крови или тромбированные сосуды. Визуально опухоль резко отделена от здоровых тканей. Расположение опухоли на малой кривизне часто характеризуется ее инфильтративным ростом.
Бляшкообразный рак – очень редкая форма рака желудка. Встречается в 1 % случаев. Являет собой утолщения слизистой оболочки желудка белесоватого или сероватого цвета, диаметром 1-2 см, иногда с изъязвлениями.

Симптомов рака желудка очень много
Эндофитная опухоль характеризуется распространением вдоль стенки желудка во все стороны, преимущественно по ее подслизистому слою. Являет собой глубокую язву различного размера с неровным, бугристым дном и нечеткими контурами. Участки, находящиеся вокруг язвы, инфильтрированы опухолевыми клетками, которые проникают во все слои стенки желудка и рядом расположенные органы.
При таком виде опухоли стенка желудка вокруг нее уплотнена, утолщена. Слизистая оболочка, окружающая опухоль, ригидная , атрофирована, складки ее зачастую расправлены. Локализация опухоли происходит чаще всего на выходе из желудка, в субкардиальном отделе и на малой кривизне. Очень рано начинает давать метастазы.
Диффузный фиброзный рак ( скирр ) одна из наиболее часто встречающихся форм рака желудка, диагностируется в 25-30 % случаев и занимает второе место по частоте возникновения. Наиболее часто размещается в выходном отделе желудка, сморщивая его стенки, сужая просвет и постепенно распространяясь на весь желудок. Стенки желудка при этой форме утолщены, складки слизистой оболочки также утолщены, имеют множественные изъязвления. Зачастую развиваются симптомы ракового лимфангита – прорастания раковых клеток по лимфатическим сосудам. Опухолевая ткань может инфильтрироваться в связки желудка, вследствие чего он подтягивается к печени, поджелудочной железе или другим органам.
Диффузный коллоидный рак – очень редко встречающийся вид опухоли, локализирующийся преимущественно в подслизистом слое или между слоями слизистой оболочки. Стенка желудка при этом как бы пропитана слизистыми массами, состоящими из слизеобразующих клеток. Стенка желудка сильно утолщена, сам желудок значительно увеличен в размерах.
Около 10-15 случаев заболевания раком имеют смешанные признаки или признаки, характерные для переходящих форм. Вышеперечисленные симптомы и виды рака желудка являются далеко не полными, но смогут помочь пациентам вовремя обратить внимание и своевременно начать лечение этого коварного заболевания. Это может снизить частоту возникновения поздних стадий рака желудка и значительно повысить процент благоприятного исхода лечения.
Рак желудка — симптомы и лечение
Что такое рак желудка? Причины возникновения, диагностику и методы лечения разберем в статье доктора Елкина Антона Вадимовича, онколога со стажем в 10 лет.
Над статьей доктора Елкина Антона Вадимовича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Рак желудка — это злокачественная опухоль, которая развивается из клеток слизистой оболочки желудка. В мире он занимает четвёртое место по распространённости среди всех онкологических заболеваний и второе место среди причин смертности от злокачественных опухолей [1] . В России рак желудка, по данным на 2017 год, находится на четвёртом месте по распространённости среди всех онкологических заболеваний у мужчин и на шестом месте у женщин [2] .
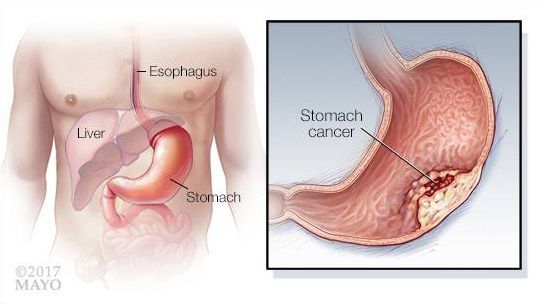
Заболеваемость раком желудка постепенно снижается, но при этом растёт число случаев, когда опухоль выявляют на IV стадии. Зачастую у таких пациентов плохой прогноз. Причина поздней диагностики — длительное бессимптомное течение болезни [1] [3] .
Точные причины развития рака желудка, как и других онкозаболеваний, пока неизвестны. И хотя установлено, что клетка становится злокачественной после определённых мутаций, в каждом конкретном случае сложно сказать, почему они произошли.
С возрастом риск развития рака желудка повышается. Наибольшее число случаев болезни диагностируется в возрасте 50–70 лет. У людей младше 30 лет она встречается крайне редко [4] .
Значимым фактором риска развития рака желудка считается инфекция H. pylori. У хронически инфицированных людей вероятность развития злокачественной опухоли выше в 2-3 раза. Врачи стали более успешно выявлять и лечить хеликобактерную инфекцию. Возможно, именно по этой причине распространённость рака желудка снижается [4] .
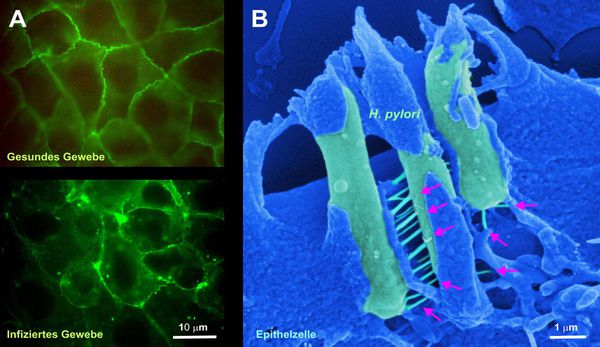
Другие факторы риска:
- Атрофический гастрит и язвенная болезнь желудка. Эти заболевания также связаны с H. pylori.
- Нехватка овощей и фруктов в рационе. В них содержатся вещества, которые, вероятно, защищают слизистую оболочку желудка от злокачественного перерождения: витамины C, E, каротиноиды, селен.
- Обилие солёной пищи. Считается, что именно из-за этого рак желудка часто встречается в некоторых азиатских странах: там вместо заморозки хранят продукты методом засолки.
- Нитраты и нитриты. Из них в желудке образуются канцерогенные соединения, которые могут стимулировать перерождение клеток желудка. Эти вещества, как правило, поступают в организм с овощами, консервированным мясом и питьевой водой.
- Пернициозная анемия — болезнь, связанная с дефицитом витамина B12, который приводит к нарушению кроветворения. Одна из возможных причин — нарушение выработки клетками желудка особого вещества — внутреннего фактора, который необходим для усвоения витамина B12 из пищи. У людей с этим типом анемии повышен риск развития рака желудка. . Его роль в формировании рака желудка пока не до конца ясна. Одни исследования показали, что табачный дым способствует развитию злокачественных опухолей желудка, другие такой связи не обнаружили.
- Вирус Эпштейна — Барр. Некоторые исследователи выделили данный вирус из злокачественных опухолей желудка. Но его роль как фактора риска развития болезни неоднозначна.
- Вторая группа крови (A). По неизвестным причинам рак желудка чаще встречается у людей именно с этой группой крови.
- Некоторые наследственные заболевания. Риск развития заболевания повышается при наследственном раке желудка диффузного типа, синдроме Линча (н аследственном неполипозном раке толстой кишки ), семейном аденоматозном полипозе, синдроме Ли — Фраумени и др. [4][5][6] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы рака желудка
Долгое время рак желудка может не вызывать симптомов. Поэтому раннюю стадию рака диагностируют, как правило, случайно во время гастроскопии, выполненной по другим показаниям.
В некоторых странах, например в Японии, эндоскопическую диагностику используют в качестве скрининга — профилактического обследования здорового населения. Благодаря ранней диагностике смертность от рака в этой стране — одна из самых низких, несмотря на очень высокую распространённость заболевания. В других странах, например в США, такой подход не практикуется. И всё же каждому человеку можно порекомендовать хотя бы раз в жизни, ближе к 50 годам, пройти гастроскопию. Это поможет своевременно выявить изменения на слизистой оболочке желудка.
Первые симптомы рака желудка чаще всего неспецифичны: они напоминают гастрит или язвенную болезнь. Пациента беспокоят дискомфорт, чувство тяжести и распирания в верхней части живота, наступает быстрое насыщение после приёма пищи [6] [7] .
На более поздних стадиях появляются боли в животе, у больного пропадает аппетит, он сильно теряет в весе. При желудочном кровотечении возникает рвота с примесью алой крови или по типу «кофейной гущи». Иногда возникает скрытое кровотечение, которое приводит к анемии. Она проявляется в виде слабости, бледности, головных болей.
Частая упорная рвота может свидетельствовать о том, что опухоль привела к стенозу привратника — перекрыла участок желудка в месте перехода в двенадцатиперстную кишку и нарушает прохождение пищи [6] .
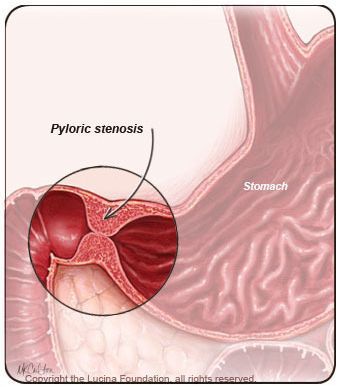
Из-за того, что симптомы возникают на поздних стадиях и маскируются под другие заболевания, у 80 % пациентов рак желудка выявляется на поздних стадиях [6] .
Патогенез рака желудка
Развитие злокачественной опухоли в желудке — длительный и довольно сложный процесс. Ему предшествует каскад предраковых изменений, который обычно протекает на фоне инфекции H. pylori [6] .
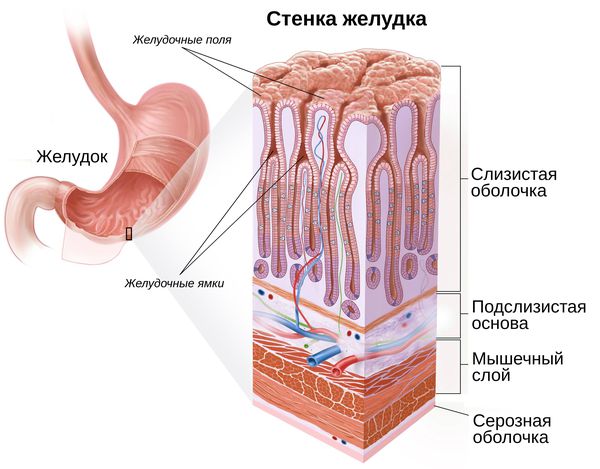
Болезнетворные бактерии вызывают воспаление слизистой оболочки желудка, которое может протекать десятилетиями. В итоге развивается атрофия желёз желудка — так называемый «атрофический гастрит» [6] .
Далее возникает кишечная метаплазия — перерождение ткани. Клетки слизистой оболочки желудка изменяются, и она начинает напоминать слизистую тонкого, а затем толстого кишечника. Это уже предраковое состояние.
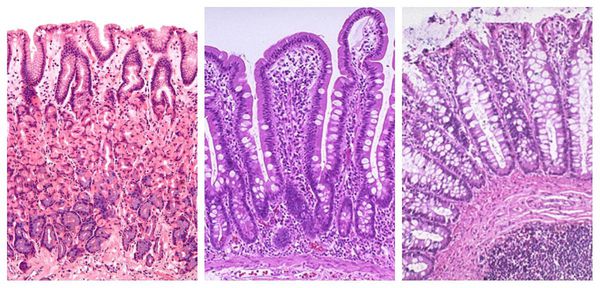
Вслед за кишечной метаплазией развивается дисплазия: клетки приобретают нехарактерный внешний вид (становятся атипичными), быстро размножаются, из-за чего нарушается структура слизистой оболочки [6] .
Выделяют три степени дисплазии слизистой желудка: лёгкую умеренную и тяжёлую. Две первые степени обратимы. Третья степень характеризуется стойкими изменениями, по сути её уже можно рассматривать как злокачественную опухоль.
В конечном итоге дисплазия приводит к развитию рака. Новообразование приобретает классические свойства злокачественных опухолей: оно может прорастать в соседние ткани, метастазировать с образованием вторичных очагов в различных органах [6] .
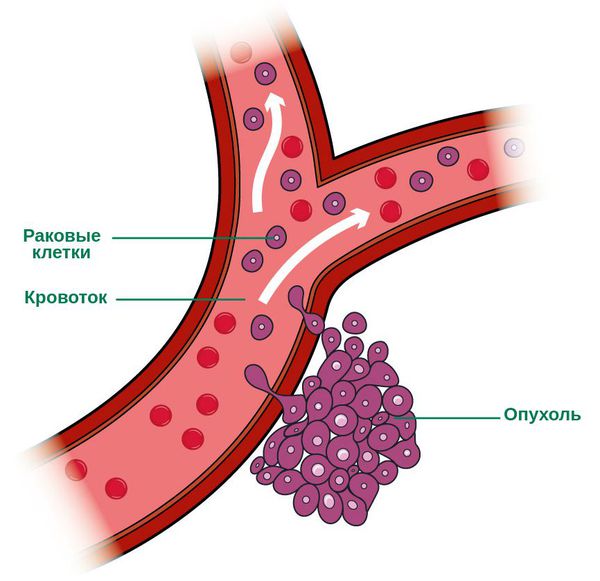
В качестве предраковых заболеваний рассматриваются полипы желудка. Они бывают разных видов, наиболее опасны аденоматозные полипы. Если их обнаружили во время гастроскопии, то необходимо провести полипэктомию — удалить полипы [7] .
К фоновым заболеваниям, при которых обычно развивается рак желудка, относятся:
- хронический атрофический гиперпластический гастрит, аутоиммунный метапластический атрофический гастрит;
- пернициозная анемия;
- перенесённая операция, во время которой была удалена часть желудка;
- аденоматозные полипы;
- болезнь Менетрие [7][8] .
Классификация и стадии развития рака желудка
Рак желудка имеет разное микроскопическое строение. В зависимости от этого выделяют его гистологические типы. Большинство злокачественных опухолей (90-95 %) представлены аденокарциномами. Они развиваются из железистых клеток [9] .
Согласно классификации 2010 года, выделяют четыре основных гистологических типа рака желудка:
- Тубулярные аденокарциномы — наиболее распространённый тип рака. Они выглядят, как полипы или «грибы» на ножке. Под микроскопом в опухоли видны канальцы разных размеров, в которых может находиться слизь.
- Папиллярные карциномы — также довольно распространённый тип опухоли. Как правило, они развиваются в верхнем отделе желудка у пожилых людей. Эти опухоли часто распространяются в лимфоузлы и метастазируют в печень.
- Муцинозные аденокарциномы — составляют около 10 % всех случаев рака желудка. Микроскопически они выглядят, как желе из слизи, в котором находятся опухолевые клетки.
- Перстневидноклеточные аденокарциномы — представлены клетками, внутри которых находится слизь. Она смещает ядро на периферию, из-за чего клетки под микроскопом выглядят, как перстни. Эти опухоли нередко находятся в нижнем отделе желудка, склонны к распространению в двенадцатиперстную кишку [1][10] .
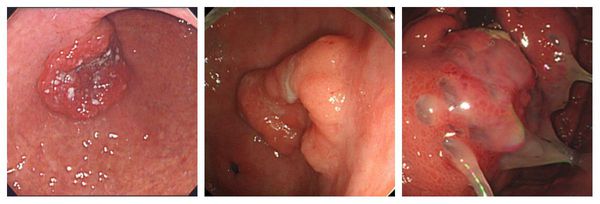
Реже в желудке встречаются другие злокачественные опухоли: лимфомы (новообразования из лимфоидной ткани), гастроинтестинальные стромальные опухоли, карциноидные опухоли (из клеток, вырабатывающих гормоны), плоскоклеточный и мелкоклеточный рак, лейомиосаркомы (злокачественные опухоли из мышечной ткани) [9] .
В зависимости от места расположения выделяют злокачественные опухоли кардии, тела, дна, антрума и привратника желудка, малой и большой кривизны, а также неуточнённой локализации [8] .
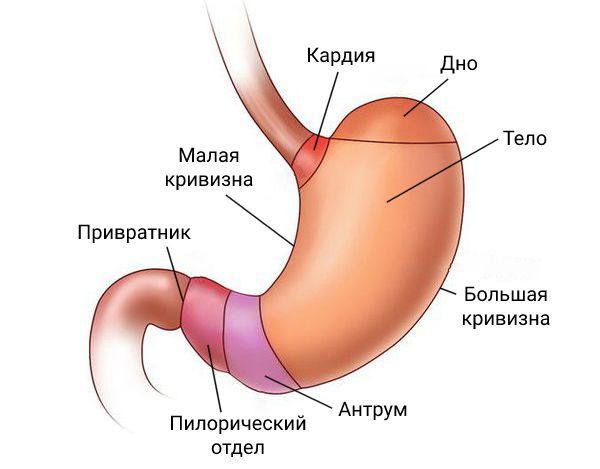
Стадирование рака
Стадию рака желудка определяют согласно общепринятой системе TNM. Буква «T» обозначает признаки первичной опухоли, «N» — распространение в лимфоузлы, «M» — отдалённые метастазы. В зависимости от степени распространения рака в организме каждой букве присваивается числовое обозначение [9] :
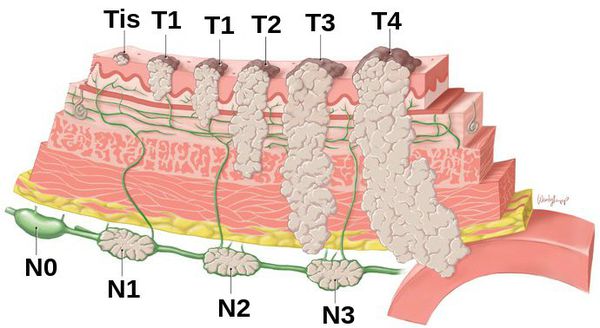
В зависимости от сочетания показателей T, N и M, выделяют четыре стадии рака желудка. В общих чертах их можно охарактеризовать следующим образом:
- Стадия I: опухоль, которая прорастает не глубже мышечного слоя и может распространяться в 1-2 ближайших лимфоузла.
- Стадия II: опухоль, которая прорастает глубже, вплоть до висцеральной брюшины, или распространяется на большее количество ближайших лимфоузлов.
- Стадия III: опухоль, которая прорастает в висцеральную брюшину, соседние органы, или поражает больше лимфоузлов, чем в предыдущих стадиях.
- Стадия IV: обнаружены отдалённые метастазы [8] .
Осложнения рака желудка
Главное осложнение рака желудка — метастазирование. С током крови метастазы (раковые клетки) чаще всего проникают в печень, реже — в лёгкие и кости. Иногда они локализуются в яичниках (опухоль Крукенберга) и лимфатическом узле над ключицей (метастаз Вирхова) [11] [12] .
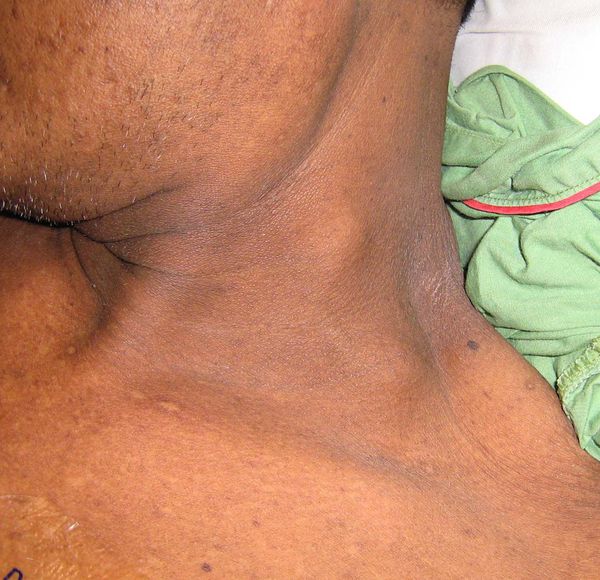
Нередко первые симптомы рака желудка связаны именно с метастазами [6] :
- При поражении печени: боль и дискомфорт под правым ребром, снижение аппетита, тошнота, потеря веса, слабость, повышенная температура и утомляемость, механическая желтуха.
- При поражении лёгких: упорный кашель, одышка, боли в грудной клетке, отхождение мокроты с примесью крови.
- При поражении костей: упорные боли, которые усиливаются во время нагрузок и длительном пребывании в однообразном положении, патологические переломы. Возможно такое серьёзное осложнение, как гиперкальциемия — повышение уровня кальция в крови из-за разрушения костной ткани.
Нередко рак напрямую прорастает в поджелудочную железу, диафрагму, большой сальник, подвздошную и двенадцатиперстную кишку. При проникновении раковых клеток в брюшную полость и распространении по её внутренней оболочке — брюшине — развивается её карциноматоз (обширное поражение метастазами). Прогноз для пациента резко ухудшается: это осложнение может стать причиной асцита (скопления жидкости в брюшной полости) и кишечной непроходимости.
При раке на поздних стадиях развивается непроходимость желудка, места его соединения с пищеводом, двенадцатиперстной кишкой.
Другим распространённым осложнением является желудочное кровотечение [13] . Как правило, оно возникает на III-IV стадии болезни из-за разрыва сосуда, в который проросла опухоль. Может быть скрытым, т. е. обнаружиться только во время диагностики, или проявляться в виде рвоты с примесью крови или дёгтеобразного стула.
Диагностика рака желудка
Наиболее информативный метод диагностики злокачественных опухолей желудка — гастроскопия. Во время этого обследования врач может осмотреть слизистую оболочку, увидеть патологические образования и провести биопсию — получить фрагмент подозрительной ткани и отправить его в лабораторию для гистологического и цитологического исследования [14] .
Современные аппараты для эндоскопической диагностики позволяют выполнить эндоУЗИ (эндосонографию) — ультразвуковое исследование через стенку желудка с помощью миниатюрного датчика. Этот метод помогает оценить глубину прорастания опухоли, её распространение в соседние структуры и лимфоузлы [14] .
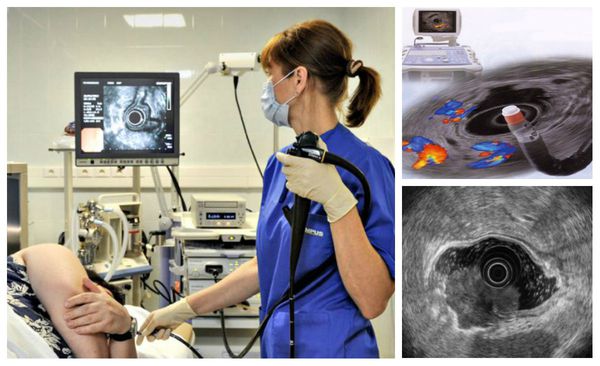
Если результаты биопсии подтвердили злокачественность новообразования, назначают обследование, которое помогает уточнить стадию заболевания и определиться с тактикой лечения:
- Рентгенография с контрастным раствором, который пациенту необходимо выпить. Выявляет поражение пищевода, двенадцатиперстной кишки, степень стеноза (сужение просвета органа).
- УЗИ органов брюшной полости помогает обнаружить метастазы в печени, лимфоузлах, распространение опухоли в соседние органы.
- УЗИ шеи и надключичных областей проводится для исключения метастаза Вирхова.
- Рентгенография грудной клетки позволяет определить наличие метастазов в лёгких.
- Компьютерная томография применяется для поиска метастазов в области груди и живота. Её также можно провести с контрастированием.
- Магнитно-резонансную томографию (МРТ) применяют для оценки распространённости опухоли и поиска метастазов.
- Колоноскопия — эндоскопическое исследование толстой кишки — может быть назначена при подозрении на кишечные осложнения.
- Позитронно-эмиссионная томография (ПЭТ) – современный оптимальный метод поиска отдалённых метастазов. Во время исследования в организм пациента вводят слабый радиоактивный препарат, который накапливается в опухолевых клетках. Затем выполняют снимки с помощью специального аппарата: на них хорошо видны все метастатические очаги.
- Лапароскопия — обследование через небольшой прокол в брюшной полости с помощью лапароскопа — выполняется для оценки распространённости опухоли и возможности её удаления [8][14][15] .
Из лабораторных исследований назначают общий анализ крови для выявления анемии, анализ стула на скрытую кровь, а также биохимический анализ крови, который помогает оценить работу печени и поджелудочной железы [15] .
Лечение рака желудка
Тактика лечения рака желудка в первую очередь зависит от его стадии, общего состояния здоровья пациента и наличия сопутствующих заболеваний.
Радикальный метод лечения рака желудка — удаление опухоли. Существуют разные виды операций. Выбор зависит от того, на какой стадии диагностировано заболевание и какая часть желудка поражена. Радикальное хирургическое вмешательство возможно, если соблюдаются три условия:
- рак желудка резектабелен, т. е. его действительно можно удалить;
- нет отдалённых метастазов;
- состояние здоровья пациента позволяет перенести хирургическое вмешательство [14] .
Если опухоль не успела сильно прорасти в стенку желудка и не распространилась в регионарные лимфоузлы, её можно удалить эндоскопически. Такая операция проводится без разреза на животе, прямо во время гастроскопии. К сожалению, рак желудка редко диагностируют на ранних стадиях, поэтому такие вмешательства показаны немногим больным [14] .
В остальных случаях выполняют один из следующих вариантов операции:
- Дистальная субтотальная резекция желудка — удаление желудка, при котором остаётся лишь 2-3 см его верхней части. Проводится при злокачественных опухолях в нижней части органа — антральном отделе.
- Проксимальная субтотальная резекция — удаление верхней части желудка вместе со сфинктером, который разделяет пищевод и желудок. Показана при поражении данного сфинктера и небольших опухолях в верхней части желудка.
- Гастрэктомию — полное (тотальное) удаление желудка — выполняют во всех остальных случаях.
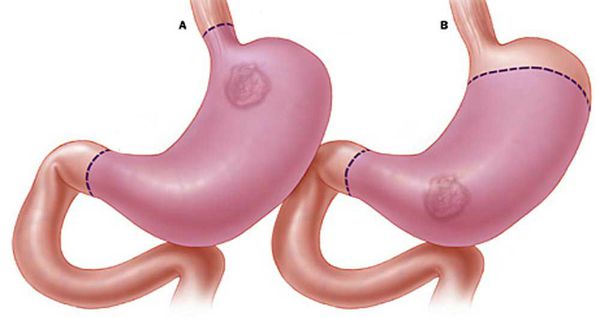
Нередко операцию дополняют лимфодиссекцией — удалением близлежащих лимфатических узлов. Обычно американские хирурги стараются удалять не менее 15 ближайших лимфоузлов, японские — ещё больше. Считается, что объём лимфодиссекции напрямую связан с эффективностью лечения [14] [16] .
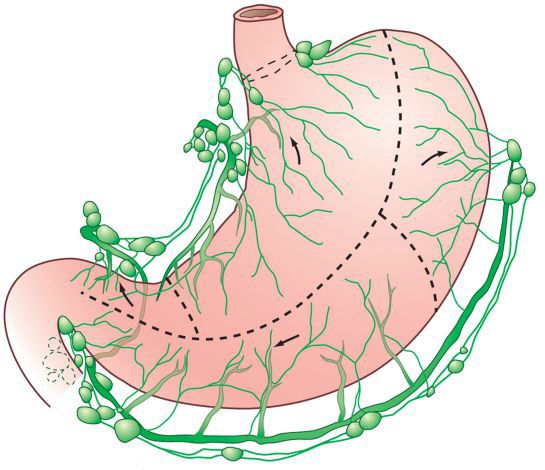
При неоперабельных опухолях прибегают к паллиативным операциям. Они помогают контролировать течение заболевания, купировать некоторые симптомы и справиться с осложнениями:
- Удаление части желудка помогает справиться с кровотечением, устранить стеноз (сужение), вызванный опухолью.
- Если опухоль блокирует нижнюю часть желудка, проводят шунтирование: между желудком и тонкой кишкой создают искусственное отверстие — обходной путь для пищи.
- У людей, которые не могут перенести операцию, для борьбы с кровотечением и стенозом прибегают к эндоскопической аблации: опухолевую ткань разрушают с помощью лазера.
- Стентирование позволяет устранить опухолевый стеноз. Стент — короткую трубку с сетчатой стенкой из металла или пластика — устанавливают в месте сужения. Он обеспечивает нормальную проходимость органа.
- Гастростомию выполняют у пациентов, которые не могут самостоятельно питаться из-за непроходимости соединения пищевода и желудка. Через отверстие из желудка на поверхность кожи выводят трубку. Через неё подают питательные смеси [16] .
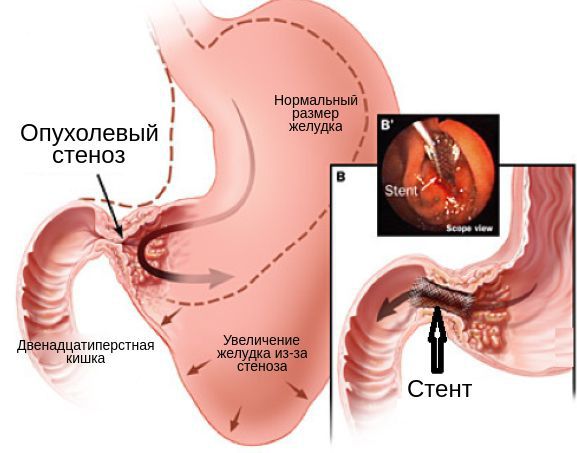
Химиотерапию при раке желудка проводят до операции, чтобы сократить размеры опухоли и облегчить её удаление, а также после, чтобы снизить риск рецидива. При неоперабельном раке она становится одним из основных методов лечения. В таких случаях обычно назначают несколько химиопрепаратов с разными механизмами действия [14] [16] .
Лучевую терапию также назначают до и после операции, а на поздних стадиях проводят в качестве самостоятельного метода лечения. Иногда её сочетают с химиопрепаратами — проводят химиолучевую терапию. Она более эффективно уничтожает опухолевые клетки, но чаще может вызвать серьёзные побочные эффекты [14] [16] .
Примерно у 20 % пациентов с раком желудка повышена активность HER2 — белка-рецептора, который находится на поверхности клеток и стимулирует их размножение. В таких случаях эффективен трастузумаб — таргетный препарат, блокирующий HER2. Его вводят внутривенно раз в 2-3 недели. До начала лечения нужно убедиться, что активность HER2 в опухолевой ткани повышена. Для этого проводят молекулярно-генетические исследования [14] [16] .
При асците проводят лапароцентез — удаление жидкости из брюшной полости через прокол и введение химиопрепаратов. При карциноматозе брюшины у некоторых пациентов может быть выполнена гипертермическая интраперитонеальная («горячая») химиотерапия. Во время вмешательства удаляют все крупные опухолевые узлы в брюшной полости, затем её промывают подогретым раствором химиопрепарата — это помогает уничтожить оставшиеся опухолевые клетки [14] [17] .
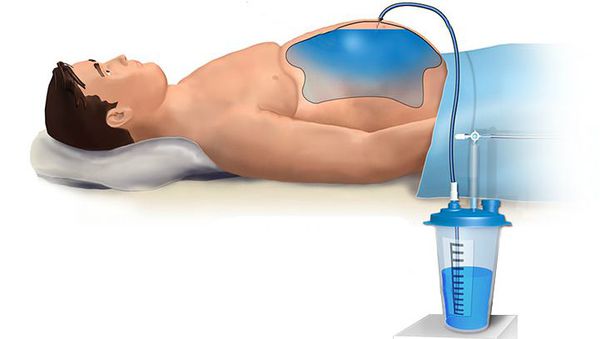
Так как многих пациентов с раком желудка беспокоят мучительные боли, для борьбы с ними применяются разные препараты и методики. Современный оптимальный способ — «лестница обезболивания». Она рекомендована экспертами Всемирной организации здравоохранения. В соответствии с ней, в зависимости от силы боли применяют все более мощные препараты [18] .
Прогноз. Профилактика
Обычно прогноз для онкобольных оценивают по показателю пятилетней выживаемости — проценту пациентов, которые продолжают жить в течение пяти лет с момента постановки диагноза.
Средняя пятилетняя выживаемость при раке желудка составляет 31 %. Она зависит от того, как рано диагностирована злокачественная опухоль:
- на локализованной стадии — когда рак не распространился за пределы желудка — 68 %;
- на местно-распространённой стадии — когда злокачественная опухоль распространилась на соседние органы и ближайшие лимфоузлы — 31 %.
- на распространённой стадии — когда есть отдалённые метастазы — 5 % [19] .
Главные меры профилактики рака желудка:
- своевременная диагностика и лечение инфекции H. Pylori;
- изменение рациона питания — употребление в пищу большого количества овощей, фруктов, ограничение соли.
Люди с предраковыми состояниями — атрофическим гастритом, метаплазией и дисплазией — должны регулярно наблюдаться у врача, проходить гастроскопию [6] .
Источник https://diseases.medelement.com/disease/%D1%80%D0%B0%D0%BA-%D0%B6%D0%B5%D0%BB%D1%83%D0%B4%D0%BA%D0%B0-2018/16063
Источник https://paracels66.ru/info/interesnoe/kak-ne-propustit-simptomy-raka-zheludka-eto-vazhno
Источник https://probolezny.ru/rak-zheludka/