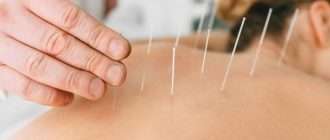
Лечение межпозвоночной грыжи без операции
Сильнейшие боли, сопровождающие грыжу межпозвоночного диска, заставляют больных искать самые быстрые и эффективные способы избавления от них. Казалось бы, операция — это и есть панацея: один раз помучился и избавился от болезни навсегда. Но не все так просто: операция не избавляет от проблем, а иногда даже усугубляет их. Большинство специалистов склоняются к тому, что лучшим вариантом является лечение межпозвоночной грыжи без операции.
Виды операций при межпозвоночной грыже
Чтобы понять, что происходит во время хирургического вмешательства и какие могут быть последствия, нужно знать, что межпозвоночный диск – это амортизатор, позволяющий позвоночнику двигаться без травмирования костной ткани позвонков. Диск состоит из эластичного ядра и окружающего его хрящевого кольца.
При грыже кольцо разрушается, и ядро или отколовшаяся часть диска (секвестр) выпячивается, сдавливая спинной мозг и отходящие от него корешки спинномозговых нервов. Это приводит к появлению характерных симптомов, в том числе боли. Чаще всего такая патология развивается в поясничном отделе позвоночника.
В последнее время некоторые клиники активно рекламируют современные хирургические методы лечения межпозвоночных грыж. Действительно ли они так эффективны и безопасны, как их описывают? Практика показывает, что это далеко не так. Все оперативные вмешательства чреваты осложнениями. К ним относятся кровотечение, инфицирование, травмирование спинного мозга или спинномозговых нервов с непредсказуемыми последствиями. Но самое главное – это то, что хирургическое лечение лишь на время избавляет от болей, но отнюдь не гарантирует, что они не вернутся вместе с рецидивом. Поэтому хирургические методы лечения должны применяться только в крайних случаях, когда все остальные методы оказались недействительными, и состояние больного прогрессивно ухудшается.
Дискэктомия
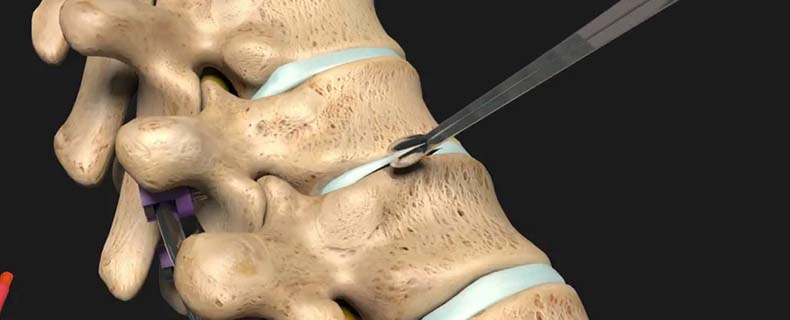
Дискэктомия – полное или частичное удаление диска. Это на определенное время избавляет от тяжелых симптомов. Но если не проводить послеоперационной консервативной реабилитационной терапии, через некоторое время после частичной дискэктомии возможен рецидив грыжи, а после полной начинают травмирваться позвонки. Их костная ткань разрастается, позвонки намертво соединяются между собой, позвоночник перестает двигаться в пораженном отделе – прогрессирующая инвалидизация обеспечена.
Имеет значение и способ проведения дискэктомии. Классический способ с разрезом на коже дает лучшие результаты, но применяется он только при больших выпячиваниях и чаще на поясничном отделе позвоночника. После малотравматичных эндоскопических (с использованием оптической аппаратуры) и микрохирургических (под микроскопом) операций чаще развиваются рецидивы.
Ламинэктомия
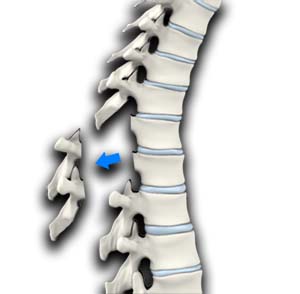
Во время оперативного вмешательства происходит полное или частичное удаление дужек позвонков пораженного отдела позвоночника. Проводится, если дужки сдавливают спинномозговые корешки. При полной ламинэктомии удаляются дужки с обеих сторон и остистый отросток позвонка. Эта операция может сочетаться с созданием неподвижности позвонков или с последующим проведением пластики участком кости пациента или искусственным имплантатом. При поражении только одной стороны позвонка ламинэктомия проводится с одной стороны.
Оперативное вмешательство сложное, проводится под общим наркозом при осложненной патологии, когда не помогают другие методы лечения. Риск осложнений велик, в послеоперационном периоде требуется такая же реабилитация, как после дискэктомии, то есть, длительное консервативное лечение.
Нуклеопластика
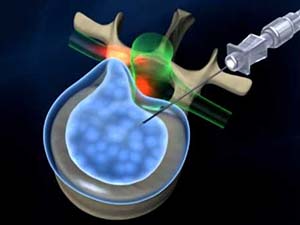
Нуклеопластика проводится при угрозе повреждения ядра диска. Так, при механическом сдавливании ядра оно расплющивается, а при нарушении целостности хрящевого кольца смещается к периферии и выходит за пределы позвоночного столба, ущемляя ткани. Для того, чтобы снизить нагрузку на ядро, его разрушают различными способами или вводят внутрь физраствор с последующим удалением всего содержимого. Самым современным и безопасным способом многие специалисты признают воздействие на ядро холодной плазмой – коблацию.
Нуклеопластика может давать осложнения. И это не всегда связано с действиями хирурга: имеют значение также индивидуальные особенности строения позвоночника пациента. Один из пациентов нашей клиники начал лечение грыжи поясничного отдела с коблации, но потом пожалел об этом: боли уменьшились, но через полгода вернулись вновь. Был поставлен диагноз рецидива заболевания. В этом нет ничего удивительного, ведь нагрузки на позвоночник не уменьшились и диск продолжал разрушаться. После проведения курса реабилитации в клинике Парамита его состояние значительно улучшилось.
Операция при грыже шейного отдела
Это наиболее опасный вид оперативных вмешательств, так как через отверстия в позвонках шейного отдела проходят артерии, питающие головной мозг, где расположены основные жизненно важные центры – сердечно-сосудистый и дыхательный.
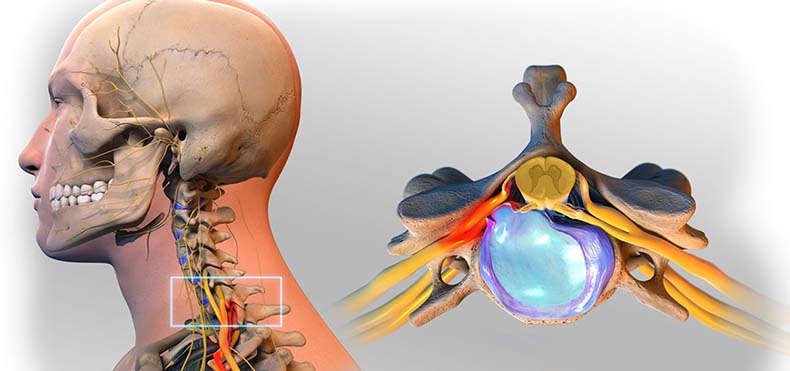
Грыжевые выпячивания шейного отдела позвоночника встречаются не так часто, но протекают тяжело. Хирургическое лечение такой патологии в шейном отделе проводится разными способами, но далеко не всегда проходит удачно. Многие пациенты жалеют, что отказались от консервативной терапии, которую в послеоперационном периоде все равно приходится проводить. Возможные осложнения:
- повреждение спинномозговых корешков шейного отдела; сопровождается усилением боли и онемением в местах прохождения поврежденных нервов; при нарушении целостности нервов развиваются стойкие параличи;
- инфицирование с последующим распространением инфекции на оболочки головного мозга;
- развитие послеоперационных спаек, сдавливающих питающие мозг артерии;
- ранние и поздние рецидивы.
Операции при грыже поясничного отдела
Грыжевое выпячивание поясничного отдела позвоночника встречается часто. Это связано с тем, что на поясничный отдел приходится самая тяжелая нагрузка. Поэтому каким бы способом ни была проведена операция и насколько бы она ни была успешной, остается очень большой риск рецидивов. Поэтому лучше проводить лечение межпозвоночной грыжи поясничного отдела без операции. Ранние и поздние осложнения:
- инфицирование;
- парезы мышц ног, нарушение функции тазовых органов – встречаются редко, но исключить нельзя;
- рецидивы заболевания – очень часто.
Когда операция по удалению межпозвоночной грыжи обязательна?
Большинству больных операция при межпозвоночной грыже диска не требуется. Показаниями к ней могут быть:
- болевой синдром, не снимающийся в течение длительного времени, несмотря на проводимое лечение;
- парезы и параличи конечностей;
- нарушение работы тазовых органов (недержание кала и мочи).
И даже в таких тяжелых случаях следует начать с консервативного лечения. Правильно подобранные безоперационные методики порой более эффективны, чем хирургическое вмешательство.
Можно ли вылечить грыжу без операции?
Не только можно, но и нужно лечить без операции, консервативно. Больному назначается комплексное лечение, в состав которого входят:
- Медикаментозная терапия — лекарства, устраняющие болевой синдром (Дексалгин, Диклофенак, Найз и др.) в виде таблеток, инъекций или мазей. При необходимости проводятся обезболивающие блокады. Также применяются лекарства, способствующие восстановлению межпозвоночных дисков (Глюкозамин, Структум).
- Физиотерапия — при помощи физиотерапевтических методик можно уменьшить боль, улучшить кровообращение, что будет способствовать восстановлению хрящевой ткани диска. Назначаются магнитотерапия, лазеротерапия, электрофорез с лекарственными растворами, фонофорез и другие процедуры. Их подбирают в зависимости от особенностей течения заболевания и общего состояния больного.
- Курсы лечебной физкультуры (ЛФК) — этот вид комплексной терапии один из самых важных, так как улучшает питание пораженных органов и укрепляет мышцы, поддерживающие позвоночник. Начинают процедуры с минимальных нагрузок и постепенно увеличивают их, ориентируясь на состояние больного.
- Массаж — отлично сочетается с ЛФК, улучшает кровообращение, питание и обмен веществ в мышцах спины и хрящевых дисках, активизирует защитные и восстановительные свойства организма.
Уникальные методики безоперационного лечения
В центре Парамита используются все перечисленные стандартные методики лечения. Но они применяются как дополнение к уникальному сочетанию лучших безоперационных методов западной и восточной медицины. Эти методики могут применять только специалисты с большим опытом, прошедшие подготовку на базе ведущих мировых лечебных центров. Наши врачи обучались в европейских и восточных клиниках, они умеют снимать боли и восстанавливать функции позвоночника.
Для каждого больного в клинике назначают следующие комплексы процедур:
- Рефлексотерапия. Наши специалисты прошли хорошую подготовку в Китае и Тибете, поэтому владеют методами диагностики и индивидуального подбора точек акупунктурного воздействия в соответствии с правилами восточной медицины. Рефлекторное воздействие на организм проводится следующими способами:
- – первый же сеанс снимает или значительно уменьшает боль, курс лечения возвращает больного к нормальной жизни, а несколько курсов способствуют восстановлению утерянных функций; – более щадящий, но не менее эффективный способ; – в руках мастера этот простой, казалось бы, способ может творить чудеса; – введением мини-доз лекарств в акупунктурные точки; позволяет успешно снимать боль и лечить заболевания, избегая передозировок лекарств.
- Вытяжение позвоночника – снимает нагрузку, способствует восстановлению нормального кровообращения и хрящевой ткани. – современная европейская методика, направленная на восстановление функций организма; основана на способности тромбоцитов стимулировать регенерацию тканей.
– ручное воздействие на костно-мышечную систему с целью восстановления правильного соотношения позвонков, поддерживающих их мышц и связок. Наши мануалисты способны снять боль за один сеанс. Отличный лечебный эффект оказывает сочетание мануальной терапии с рефлексотерапией. – воздействие щадящего вида гимнастики, направленное на снятие нагрузки с мышц, укрепление мышц спины.
С отзывами пациентов, прошедших курс лечения в клинике Парамита, можно ознакомиться на нашем сайте. Все они хорошо понимают важность систематической консервативной терапии, проходят курсы поддерживающей терапии и живут полной жизнью без болей и нарушений функции позвоночника.
Лечение грыжи межпозвонкового диска требует особого подхода к каждому больному. Лишь немногие пациенты с таким заболеванием нуждаются в операции. Все остальные должны отдавать предпочтение безоперационным способам лечения.
10 главных упражнений для тех, у кого нарушено кровообращение


Самые частые заболевания, связанные с нарушенным кровообращением — гипертония, варикозное расширение вен конечностей, сердечная недостаточность.
Нормальное кровообращение важно для сердца, всех органов и систем без исключения. «Составляющие» организма не могут правильно работать без поступления с кровью полезных веществ и без своевременного удаления лишнего — продуктов обменных процессов, углекислого газа. Застойные явления могут привести к стойким нарушениям функций.
Причиной нарушенного кровообращения выступает изменение тонуса кровеносных сосудов. Их сужение может возникнуть из-за курения, малоподвижного образа жизни, лишнего веса, заболеваний щитовидной и поджелудочной желез, почек, сердца, развития атеросклероза, тромбоза. Недостаточное кровообращение в ногах связано с сидячей работой или долгим пребыванием на ногах.
Признаки проблем с кровообращением
Симптомы хронической недостаточности кровообращения в головном мозге могут не появляться до ситуации, требующей обильного кровоснабжения: стресса, непривычной физической нагрузки, нахождения в непроветриваемой комнате. Они появляются внезапно: головная боль, онемение части лица, нарушение координации движений, шум в ушах.
Хронически могут появляться такие симптомы: частые головокружения, снижение памяти и работоспособности, ухудшение концентрации внимания, сонливость или бессонница.
К признакам нарушения кровотока в конечностях относят перемежающуюся хромоту (боль при ходьбе и ее отсутствие в покое), холодные руки и ноги при любой погоде, образование сосудистых звездочек, тяжесть, усталость, отеки, судороги в мышцах ног.
Как улучшить кровообращение в ногах
Если не следить за кровообращением в ногах, можно упустить начало развития необратимых нарушений. Плохой кровоток приводит к варикозной болезни — стойкому расширению вен. Для того, чтобы обеспечить нормальный ток крови и тонус сосудов, откажитесь от лифтов и отдайте предпочтение ходьбе по ступенькам. Полезно также ходить пешком, кататься на велосипеде/велотренажере.
А эти упражнения можно делать дома ежедневно:
- Встаньте на колени, локти — на полу перед собой. На выдохе выпрямите ноги так, чтобы тело образовало букву «Л» , задержитесь на 10 секунд, вернитесь в исходное положение.
- Лежа на спине имитируйте езду на велосипеде — руки за головой, ноги поднять перпендикулярно туловищу. 30 вращений, количество подходов может варьироваться в зависимости от натренированности мышц.
- В положении сидя прижмите пятки к полу, поднимите носки, затем — наоборот. Повторить 20-30 раз. Идеально подходит в вечернее время тем, кто страдает от судорог икроножных мышц.
- Лежа на спине поднимите одну ногу. Вращайте ей по часовой стрелке 20 раз. Повторите с другой ногой против часовой стрелки.
- Сидя развести прямые ноги в стороны настолько, насколько позволяет растяжка. Наклоняйтесь поочередно в обе стороны по 10 раз.
Как улучшить мозговое кровообращение
Хроническое нарушение мозгового кровообращения — прямой путь к инсульту. Оно чревато и другими неприятными последствиями: нарушениями памяти, ухудшением работоспособности, головокружениями и обмороками, онемением лица.
Вот 5 упражнений для улучшения мозгового кровообращения:
- Березка. Универсальная поза для улучшения кровотока во всем теле, в том числе — в голове. Начинать нужно с минуты, постепенно увеличивая время.
- Наклоны во все стороны и вращения головой. Движения должны быть плавными. Не усердствуйте, если потемнело в глазах или закружилась голова — снизьте амплитуду движений после 5-минутного перерыва.
- Встаньте спиной к стене, сделайте вдох и сильно прижмитесь к ней, напрягая мышцы шеи. Задержитесь на 5 секунд, расслабьтесь.
- Сидя надавите на лоб ладонью и напрягите мышцы шеи, не давая измениться положению головы. Зафиксируйте положение на задержке дыхания на 5-10 секунд, выдохните, расслабьтесь. Достаточно 4-7 повторов.
- Сидя за столом упритесь в него локтем. Ладонь прижмите к виску. Наклоняйте голову в сторону руки, сопротивляйтесь ладонью. Держите мышцы в напряжении 5-10 секунд, после повторить с другой стороной.
Когда нужно немедленно идти к врачу
Симптомы острого нарушения мозгового кровообращения — повод вызвать скорую:
- асимметрия лица, языка;
- онемение, слабость, паралич конечности;
- нарушения речи;
- двоение в глазах, потеря фокусировки зрения;
- рвота;
- сильное нарушение координации движений ( «пьяная» походка);
- спутанность сознания;
- нетипично сильная головная боль.
Медицинская помощь нужна и тогда, когда симптомы хронического нарушения кровообращения не проходят долгое время, а упражнения не помогают вернуть тонус сосудам. Если в течение нескольких дней сохраняется сильное головокружение, головная боль, сонливость, нарушение концентрации внимания, утомляемость, обратитесь к терапевту или неврологу.
Некоторые признаки нарушенного кровообращения в ногах также требуют врачебной помощи. Сосудистые звездочки, выпячивания вен, длительно сохраняющиеся синяки, непроходящие судороги икроножных мышц — повод посетить флеболога.

Рефлексотерапия — один из самых эффективных методов безмедикаментозного лечения. Её история насчитывает…
Почему у одних людей остеохондроз начинается ещё в раннем возрасте, а у других его нет и после 50?
Мануальная терапия — это выполняемый руками комплекс биомеханических приёмов, направленных на устранение…
Рацион опухолевых клеток, или роль питания в терапии рака

Обзор
Авторы
Редакторы
Статья на конкурс «Био/Мол/Текст»: Корректировка диеты часто применяется для лечения и профилактики заболеваний. Онкологические заболевания — не исключение: правильное питание может служить не только профилактической мерой, но и повышать эффективность терапии. Здесь мы предлагаем обсудить «вкусовые предпочтения» раковых клеток и разобраться в том, как отдельные питательные вещества могут помочь бороться с опухолью.

Конкурс «Био/Мол/Текст»-2021/2022
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2021/2022.
Партнер номинации — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.
Генеральный партнер конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Введение: на вкус и цвет товарищей нет
С начала 1980-х годов ведущие организации здравоохранения выпускают рекомендации по питанию и образу жизни, которые позволяют снизить индивидуальный риск развития рака. Данные рекомендации основаны на результатах метаанализов эпидемиологических исследований (иными словами, анализ многолетнего опыта миллионов людей, которые питались тем или иным образом). Эти рекомендации универсальны и просты в исполнении: они не требуют подсчета калорий, строгого контроля состава продуктов, а лишь предлагают общую схему и принцип питания для поддержания здорового веса (рис. 1).
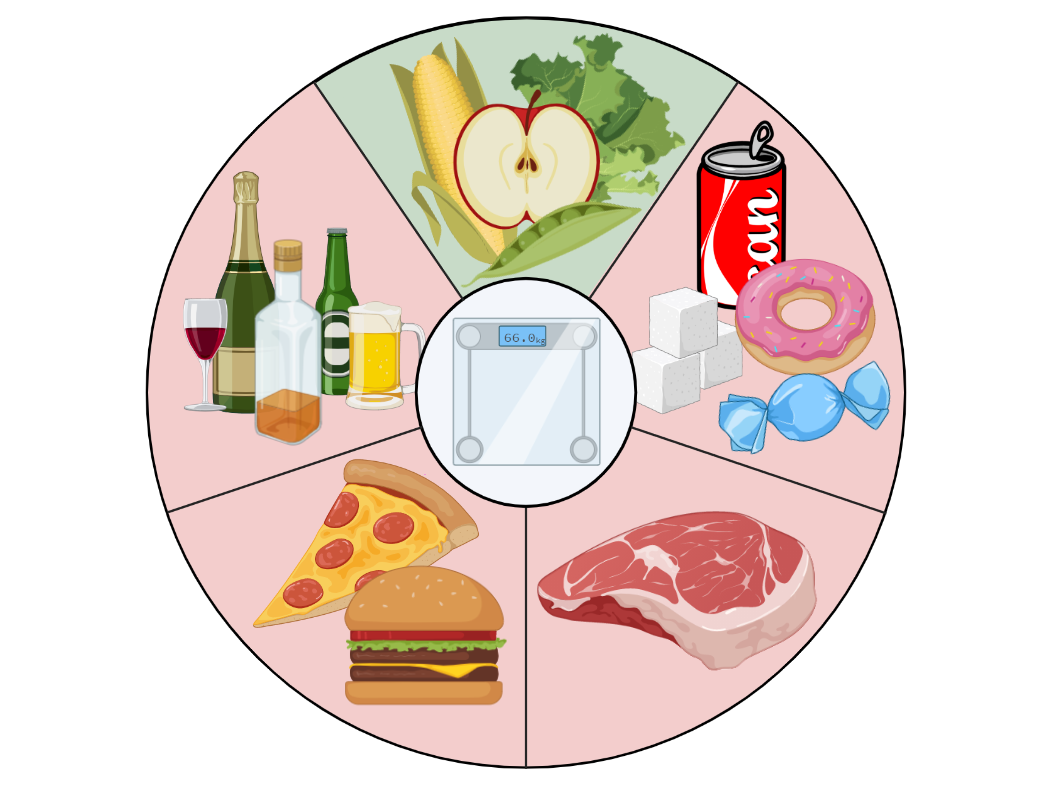
Рисунок 1. Рекомендации по питанию, которые направлены на снижение вероятности возникновения онкологических заболеваний. Ежедневный рацион должен включать фрукты, овощи, бобовые культуры, цельнозерновые крупы. По возможности, необходимо ограничивать употребление красного мяса, сахара, сладких газированных напитков и алкоголя. Следование данным советам позволит поддерживать здоровый вес в течение всей жизни и снизить индивидуальный риск развития рака.
коллаж авторов статьи. Создан с помощью BioRender.com
Подобного рода советы относятся к здоровым людям, тогда как для людей, страдающих онкологическими заболеваниями, стандартных рекомендаций по питанию не существует. В то же время, питание пациентов может сильно влиять на успешность терапии злокачественных образований [1]. Почему для людей, больных раком, нельзя составить универсальные рекомендации по составу пищи? Ответ на этот вопрос следует из принципов, согласно которым развиваются все опухоли [2]. Изначально клетка, которая в будущем даст начало опухоли, ничем не отличается от своих соседей. По мере накопления мутаций нормальные клетки могут постепенно эволюционировать и приобретать черты раковых клеток [3], [4]. В 2000 году среди многочисленных особенностей рака, в легендарном обзоре Hallmarks of cancer [3] были обозначены основные признаки, которые определяют биологию опухолевой клетки (рис. 2).
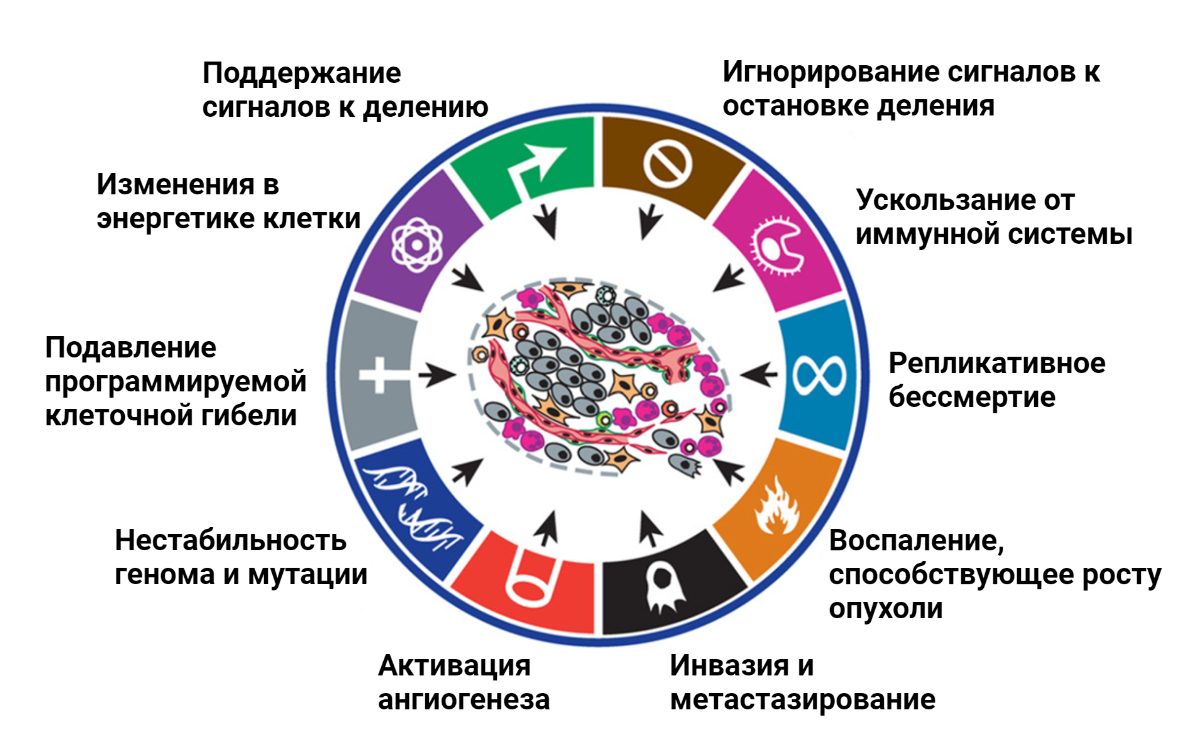
Рисунок 2. Особенности опухолевых клеток (hallmarks of cancer), которые отличают их от нормальных. Были сформулированы в 2000 году [3] и затем дополнены в 2011 [4].
Важнейшей особенностью всех раковых клеток является нестабильность генома, которая приводит к огромному генетическому разнообразию опухолей. Несмотря на ряд свойств, присущих всем раковым клеткам, каждая опухоль обладает уникальным набором мутаций, которые и определяют ее агрессивность, скорость роста, эффективность терапии. Генетическое разнообразие опухолей является основной преградой для составления универсальных рекомендаций по питанию для пациентов.
В последнее время исследователи активно изучают влияние питательных веществ на прогрессию опухоли и эффективность лечения. В основном проводятся экспериментальные работы на животных моделях, но есть и немногочисленные клинические исследования. Мы предлагаем читателям познакомиться поближе с особенностями метаболизма опухолевой клетки. Попытаемся разобраться, как вещества, потребляемые с пищей, могут влиять на опухоль и ее окружение. И, наконец, попробуем ответить на вопрос: может ли диета помочь в борьбе с раком?
Метаболизм
Для того, чтобы разобраться в тонкостях метаболизма раковой клетки, кратко вспомним основные принципы и термины биоэнергетики. Метаболизм — это совокупность химических превращений в клетке, которые направлены на получение энергии и необходимых веществ. Только посмотрите, какое бесчисленное количество реакций включает в себя метаболизм (рис. 3)! Все метаболические пути можно условно разделить на биодеградацию (катаболизм) и биосинтез (анаболизм) [5]. Катаболизм приводит к получению энергии в виде макроэргических соединений (таких как АТФ), а также NADH, NADPH и FADH2 — коферментов, участвующих в окислительно-восстановительных реакциях. Анаболические процессы используют запасенную энергию для синтеза молекул, необходимых для жизни клетки: жиров, нуклеотидов, белков, углеводов.
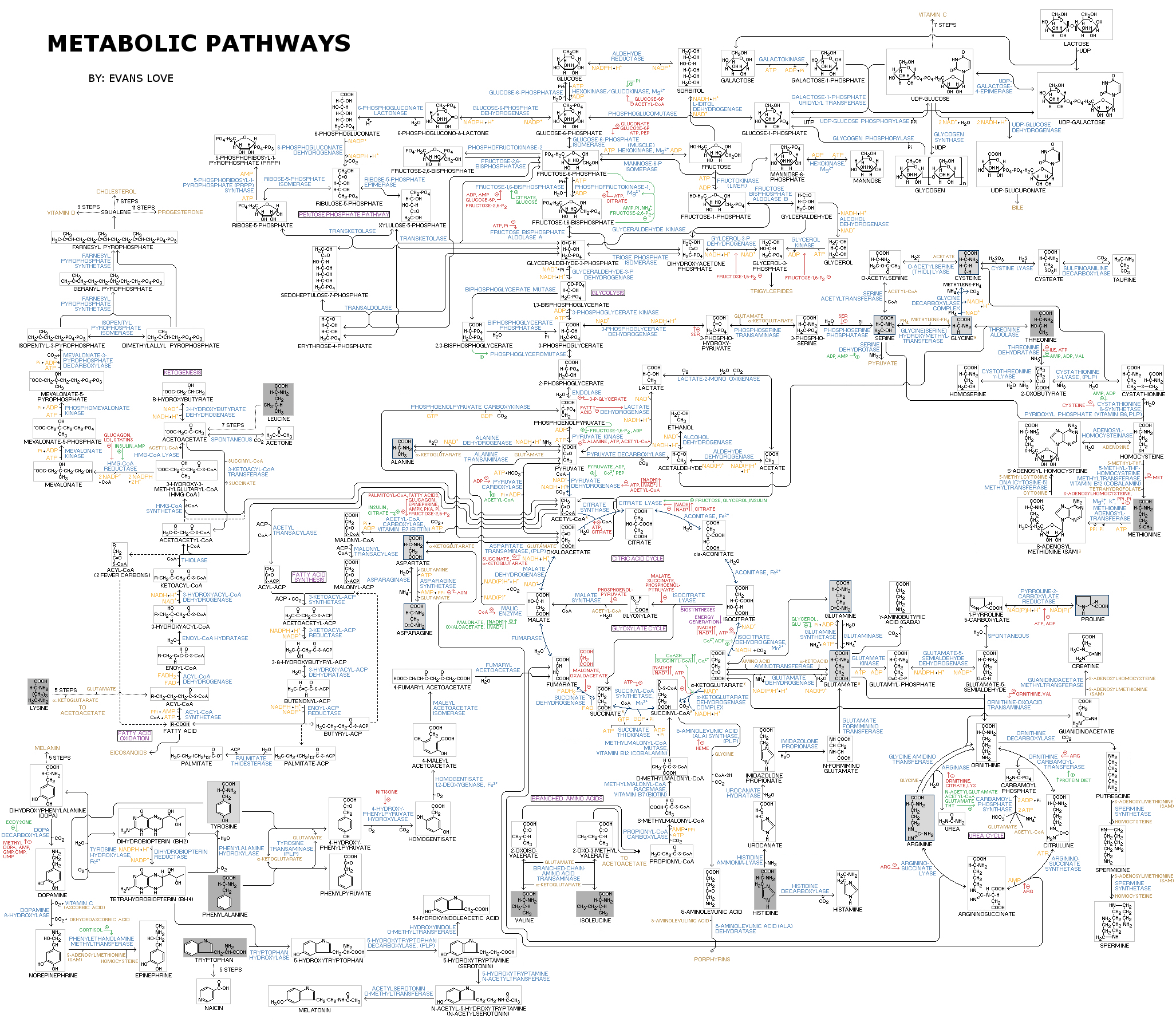
Рисунок 3. Метаболическая карта — схема, объединяющая основные метаболические пути в клетке.
Метаболизм тесно связан с питанием: ежедневно мы потребляем питательные вещества, которые, с одной стороны, участвуют в катаболических реакциях и поставляют энергию клеткам, а с другой — необходимы для синтеза собственных молекул. Углеводы, белки и жиры, которые мы потребляем, разрушаются в пищеварительном тракте до мономерных единиц: углеводы до моносахаридов (глюкоза, фруктоза и др.), жиры до жирных кислот и глицерина, белки до аминокислот. Эти молекулы поступают в клетки организма и принимают участие в метаболических процессах.
В раковой клетке зачастую увеличена активность некоторых метаболических ферментов или целых метаболических путей, а значит, и потребность в питательных веществах у клеток опухоли может отличаться от нормальных клеток [6]. Эти особенности могут быть учтены при лечении опухоли: исключение из рациона пациента определенных компонентов пищи приведет к понижению их содержания в плазме крови, а следовательно, и в окружении раковых клеток, что негативно скажется на их размножении. Кроме этого, некоторые элементы питания могут непосредственно влиять на противоопухолевый иммунитет, что также должно быть учтено при составлении диеты.
Глюкоза
Глюкоза является основным источником энергии для живых организмов. В нормальном рационе человека она встречается как в свободном виде, так и в составе олиго- и полисахаридов (например, в сахарозе, лактозе и мальтозе). Одним из важнейших биоэнергетических путей в клетке является гликолиз — последовательность химических реакций, в результате которых из 1 молекулы глюкозы получается 2 молекулы пировиноградной кислоты, 2 молекулы АТФ и 2 молекулы NADH. Затем пировиноградная кислота может быть вовлечена в цикл трикарбоновых кислот (цикл Кребса) — биохимический процесс, протекающий в митохондриях, который поставляет NADH и FADH2 что, в конечном счете, делает возможным синтез АТФ посредством окислительного фосфорилирования. При этом из 1 молекулы глюкозы можно получить приблизительно 36 молекул АТФ, что гораздо более выгодно с точки зрения энергетики, нежели просто гликолиз. Вследствие этого большинство клеток активно использует цикл трикарбоновых кислот и окислительное фосфорилирование для получения энергии.
Тем не менее, известно множество случаев, когда по разным причинам клетки смещают баланс в сторону гликолиза, используя этот путь в качестве основного источника энергии, ингибируя ферменты цикла трикарбоновых кислот или активируя ферменты гликолиза.
Давно известно, что опухолевые клетки активно используют гликолиз, несмотря на его относительно низкую эффективность с точки зрения энергетической выгоды. Это явление было открыто Отто Генрихом Варбургом в 1924 году. Сам Варбург считал, что нарушение клеточного дыхания — главная причина развития опухоли. Однако оказалось, что клеточное дыхание в большинстве опухолевых клеток не нарушено, а просто подавляется из-за активного гликолиза. Сейчас понятно, что активный гликолиз дает преимущество опухолевым клеткам. Во-первых, гликолиз протекает без кислорода, и, по-видимому, во многом является адаптацией к гипоксии, которая развивается по мере удаления опухолевых клеток от кровеносных сосудов. Частично эта проблема также решается тем, что раковые клетки могут способствовать ангиогенезу — прорастанию сосудов в опухоль за счет продукции ангиогенных факторов, например фактора роста эндотелия сосудов (VEGF, Vascular endothelial growth factor). Во-вторых, активный гликолиз сопряжен с образованием большого количества молочной кислоты, что приводит к закислению среды, тем самым способствуя инвазии опухоли за счет разрушения нормальных популяции клеток и деградации внеклеточного матрикса.
В то же время, нельзя не отметить тот факт, что эффект Варбурга наблюдается не только в опухолевых клетках, но и вообще во всех активно пролиферирующих клетках. Глюкоза — один из основных источников углерода в клетке, и ее полное окисление в цикле трикарбоновых кислот идет вразрез с потребностями пролиферирующей клетки. Некоторая часть глюкозы, а точнее, ее метаболитов, должна быть направлена на пути биосинтеза аминокислот, нуклеотидов и жирных кислот. Важную роль в производстве предшественников нуклеотидов и аминокислот, а также NADPH, необходимого для синтеза жирных кислот, играет пентозофосфатный путь — альтернативный путь окисления глюкозы, который также имеет ключевое значение в поддержании роста раковых клеток.
Итак, глюкоза особенно необходима раковым клеткам в связи с их активным размножением; при этом она служит не только источником энергии, но и важным предшественником для синтеза аминокислот, нуклеотидов и жирных кислот. Однако помимо непосредственной роли глюкозы в клеточном метаболизме, важным физиологическим аспектом также является эффект инсулина на опухолевые клетки.
Как известно, повышение уровня глюкозы в крови вызывает секрецию гормона инсулина бета-клетками поджелудочной железы. Инсулин, в свою очередь, взаимодействует с инсулиновыми рецепторами на поверхностях клеток. Взаимодействие инсулина с его рецептором приводит к активации фосфатидилинозитол-3-киназы (PI3K) — ключевого фермента PI3K/AKT/mTOR сигнального пути: работа PI3K делает возможным фосфорилирование протеинкиназы Akt, что приводит, с одной стороны, к транслокации глюкозных транспортеров на клеточную мембрану (и, как следствие, к увеличению поглощения глюкозы клетками), а с другой стороны — к активации протеинкиназы mTORС1, важнейшего регулятора клеточного метаболизма и роста [1].
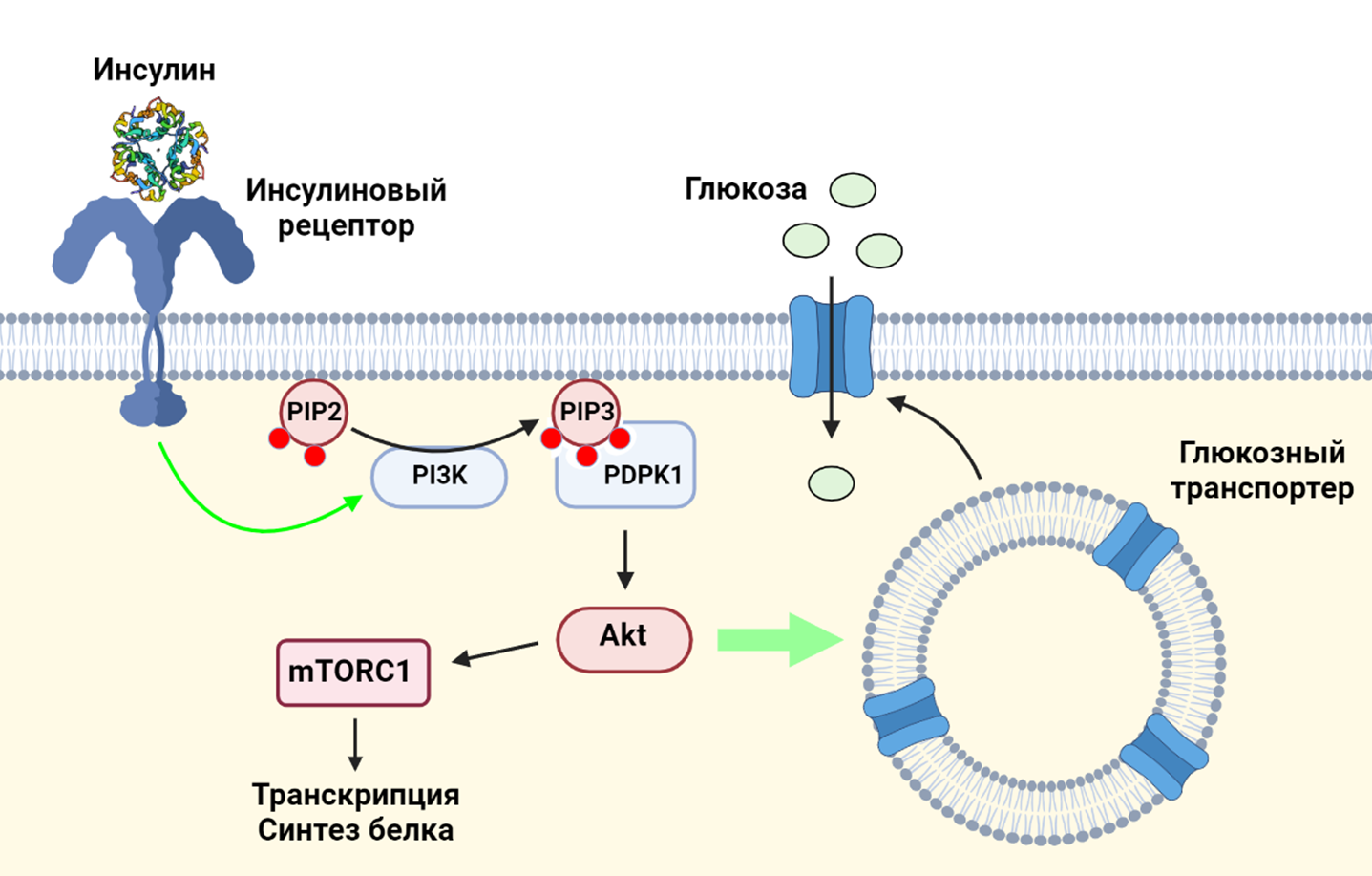
Рисунок 4. Взаимодействие инсулина и его рецептора приводит к активации фосфатидилинозитол-3-киназы (PI3K), которая фосфорилирует фосфатидилинозитолдифосфат (PIP2). Образовавшийся фосфатидилинозитолтрифосфат (PIP3) нужен для того, чтобы фосфоинозитид-зависимая киназа-1 (PDPK1) активировала протеинкиназу Akt. Akt необходима для стыковки внутриклеточных везикул, несущих глюкозный транспортер, с клеточной мембраной. Также Akt активирует mTORC1.
коллаж авторов статьи. Создан с помощью BioRender.com
Сигнальный путь PI3K/AKT/mTOR играет важную роль в раковых клетках, которые могут активно экспрессировать рецепторы к инсулину и, получая сигналы при их стимуляции, увеличивать темпы роста и размножения.
Снижение уровня глюкозы в крови пациентов рассматривается как одна из потенциальных диетических стратегий при терапии рака. Такой подход ограничит доступность глюкозы для раковых клеток и понизит секрецию инсулина бета-клетками поджелудочной железы. Как можно понизить содержание глюкозы в крови пациентов? Конечно, уменьшение калорийности пищи приведет к снижению уровня глюкозы в крови, но такой способ не может быть оптимальным, так как поставит под угрозу общее состояние пациента. Куда более выгодной стратегией может стать кетогенная диета, которая предполагает ограничение потребления углеводов с одновременным увеличением доли жиров в рационе. Действительно, есть данные доклинических исследований и немногочисленные клинические испытания, которые говорят, что такая диета может способствовать благоприятному исходу болезни — например, при глиобластоме [7]. Однако важно отметить, что некоторые типы опухолей, наоборот, зависят от жирных кислот, а значит, диета, богатая жирами, может опосредовать проканцерогенный эффект [1], о чем мы поговорим чуть далее.
А что насчет других углеводов?
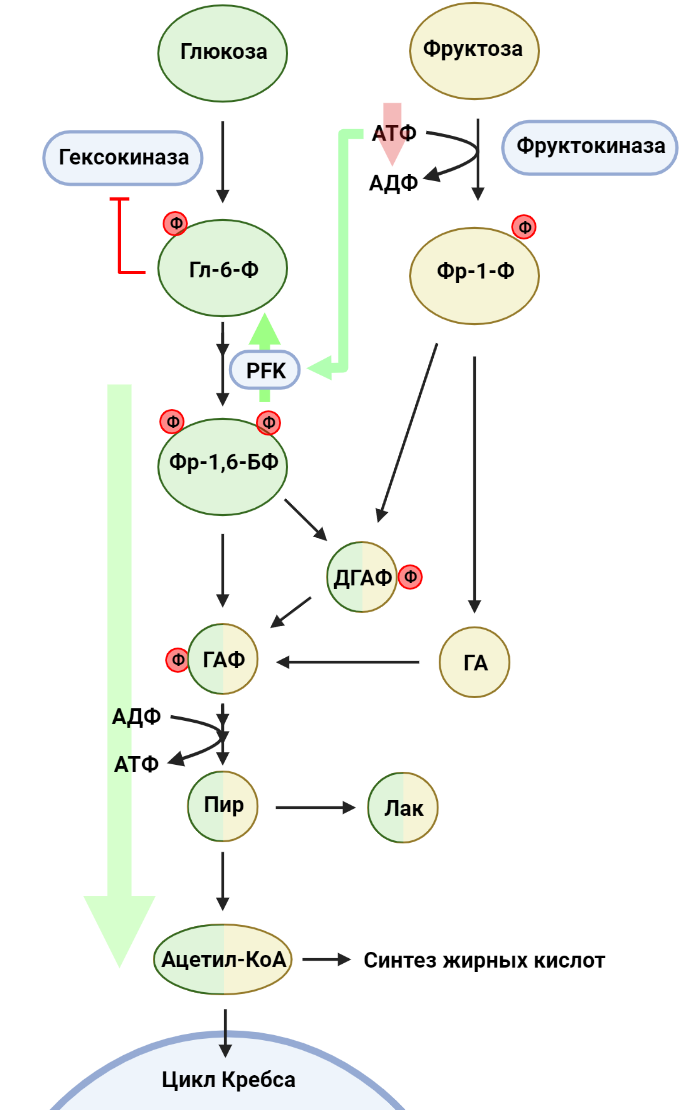
Рисунок 5. Метаболизм фруктозы. В первой стадии гликолиза глюкоза фосфорилируется до глюкозо-6-фосфата (Гл-6-Ф). Параллельно фруктоза фосфорилируется до фруктозо-1-фосфата (Фр-1-Ф). Фруктоза-1,6-бисфосфат (Фр-1,6-БФ), продукт фосфофруктокиназы (PFK), распадается на глицеральдегидфосфат (ГАФ) и дигидроксиацетонфосфат (ДГАФ), а Фр-1,6-БФ расщепляется на ДГАФ и глицеральдегид (ГА). ДГАФ и ГА переходят в ГАФ, который в оставшихся реакциях гликолиза превращается в пируват (ПИР). ПИР может восстановиться до лактата (ЛАК) или подвергаться превращению в ацетил-КоА, соединение, использующееся в многих биохимических процессах.
коллаж авторов статьи. Создан с помощью BioRender.com
Помимо глюкозы, в наш ежедневный рацион входит множество других углеводов. Например, фруктоза, один из наиболее распространенных в природе сахаров, встречается в пище как в свободном виде, так и в составе олигосахаридов, например, сахарозы. Эпидемиологи связывают рост потребления сахаросодержащих напитков с увеличением частоты заболеваемости раком [8]. Более того, оказывается, что даже умеренное потребление фруктозы (эквивалентное одной банке газировки в день) оказывает негативное воздействие и может способствовать росту опухоли, что было отмечено в экспериментах с мышами на примере колоректального рака [9]. Глюкоза эффективно поглощается эпителиальными клетками тонкого кишечника за счет специальных белков, осуществляющих совместный транспорт глюкозы и ионов натрия. При этом транспорт фруктозы опосредуется пассивным транспортером GLUT5 и потому менее эффективен. В результате значительная часть потребляемой фруктозы проходит тонкую кишку и попадает в толстый кишечник. В случае колоректального рака фруктоза становится одним из потенциальных питательных веществ для опухолевых клеток: действительно, раковые клетки в кишечнике активно экспрессируют как GLUT5, так и ферменты, метаболизирующие фруктозу. Глюкоза и фруктоза похожи между собой с точки зрения строения молекул, однако с точки зрения их метаболизма они немного отличаются (рис. 5). Если говорить про глюкозу, то первая стадия гликолиза представляет собой фосфорилирование глюкозы с затратой АТФ и образованием глюкозо-6-фосфата, причем активность гексокиназ (ферментов, осуществляющих эту реакцию) зависит от концентрации глюкозо-6-фосфата в среде: чем больше продукта для фермента, тем менее активно он работает. Это явление — пример отрицательной обратной связи, важного аспекта регуляции активности метаболических путей. Фруктоза же в первую очередь фосфорилируется фруктокиназой до фруктозо-1-фосфата (Фр-1-Ф), также с затратой АТФ, однако в данном случае активность фермента не зависит от концентрации продукта. Это значит, что киназа будет фосфорилировать всю доступную фруктозу, вне зависимости от того, сколько Фр-1-Ф уже было сделано. Следовательно, при повышенной концентрации фруктозы клетка будет тратить много АТФ на ее фосфорилирование. В ответ на понижение уровня АТФ активируется фермент глизолиза фосфофруктокиназа (PFK), а также, помимо этого, продукты расщепления Фр-1-Ф в конечном счете попадают в реакции гликолиза. Таким образом, фруктоза усиливает гликолиз, что на руку раковым клеткам: в случае колоректального рака активация гликолиза способствует индукции синтеза жирных кислот, необходимых для роста опухоли [9].
Надо отметить, что фруктоза, хоть и способствует росту опухолей в случае колоректального рака, для роста и выживания нормальных клеток вовсе не обязательна, так что фармакологическое подавление переносчиков фруктозы и ферментов, участвующих в ее метаболизме (например, фруктокиназы) может препятствовать прогрессии колоректального рака. И конечно же, исключение фруктозы из рациона пациента также может оказывать благотворный эффект на течение болезни. Однако клинических данных, подтверждающих это, пока недостаточно [1].
Еще один любопытный пример связан с маннозой, моносахаридом, который также часто встречается в рационе как в свободном виде, так и в составе полисахаридов. Манноза поглощается теми же транспортерами, что и глюкоза, но затем накапливается в клетках в виде маннозо-6-фосфата и дальше почти не метаболизируется. В то же время, маннозо-6-фосфат ингибирует некоторые ферменты гликолиза (гексокиназу и глюкозоизомеразу), а также глюкозо-6-фосфатдегидрогеназу — первый фермент пентозофосфатного пути, альтернативного способа окисления глюкозы. Таким образом, накопление маннозо-6-фосфат влечет за собой подавление метаболизма глюкозы, что негативно сказывается на жизнеспособности раковых клеток. Однако не все опухоли чувствительны к маннозе. Дело в том, что в клетках есть фермент маннозо-6-фосфат—изомераза (PMI), который катализирует превращение маннозо-6-фосфата в фруктозо-6-фосфат, метаболит гликолиза. Казалось бы, накопление маннозо-6-фосфата перестает быть проблемой для клетки, но дело в том, что разные опухоли имеют разную активность PMI, и если в каких-то опухолевых клетках его активность понижена, то манноза будет подавлять рост опухоли. Оказалось, что колоректальные опухоли обычно имеют очень низкие уровни PMI, и действительно, на мышиной модели колоректального рака было показано, что биодобавки, содержащие маннозу, значительно подавляют рост опухолей и не оказывают отрицательный эффект на здоровье и вес мышей [10]. Возможно, применение маннозы в виде добавок к пище будет повышать эффективность терапии колоректального рака и у людей, но клинических исследований на этот счет еще не проводилось [1].
Жирные кислоты
Жирные кислоты являются важнейшим источником энергии в клетке, особенно для «энергозатратных» тканей вроде скелетной и сердечной мышечных тканей. При окислении жирных кислот (которое в основном происходит в ходе процесса β-окисления) образуются NADH и FADH2, а также ацетил-КоА — вещества, необходимые для синтеза АТФ при окислительном фосфорилировании. Более того, если сравнить между собой жирные кислоты и углеводы, то окажется, что по отношению к своей сухой массе жирные кислоты обеспечивают больше АТФ, чем углеводы, а значит, они лучше подходят на роль запасного питательного вещества (жирные кислоты запасаются в форме триглицеридов в жировой ткани). Разумеется, не могло бы случиться такого, чтобы не нашлось опухолевых клеток, активно использующих жирные кислоты как источник энергии и восстановительных эквивалентов. Действительно, описаны процессы, когда раковая клетка переходит на β-окисление, а также отдельные опухоли, для которых основной источник энергии — это жиры, а не углеводы [1], [11].
Так, было показано, что окисление жирных кислот критично для клеток рака груди при их откреплении от матрикса. Протоки молочных желез выстланы слоем эпителиальных клеток, которые дают начало опухоли. На ранних стадиях развития рака молочной железы опухолевые клетки открепляются от матрикса, покидают свои ниши, начинают пролиферировать в просветах полых железистых структур, заполняя их. Эпителиальные клетки имеют на своей поверхности рецепторы эпидермального фактора роста (epidermal growth factor receptor, EGFR). При стимуляции EGFR, помимо прочего, происходит активация сигнального пути PI3K/AKT/mTOR, что приводит к росту, пролиферации, а также способствует поглощению глюкозы и подавлению апоптоза. Для эпителиальной клетки очень важен контакт с внеклеточным матриксом. Если клетка по какой-либо причине теряет контакт с матриксом, то экспрессия EGFR падает, и, как одно из следствий, клетка начинает испытывать дефицит в глюкозе. В норме эта череда событий непременно приведет к нехватке АТФ, окислительному стрессу, и наконец — к аноикису— гибели клетки, происходящей в ответ на открепление от матрикса. Но опухолевая клетка не так проста и активно пытается спастись от апоптоза. Активность ряда онкогенов в данном случае способствует активации окисления жирных кислот, что обеспечивает клетку энергией и предотвращает гибель [12].
Другой важный пример роли жирных кислот в раковых клетках связан с никотинамидадениндинуклеотидфосфатом (NADPH) — веществом, которое выполняет две основные функции. С одной стороны, он участвует в защите клетки от токсичных активных форм кислорода (АФК), обеспечивая регенерацию антиоксиданта глутатиона (GSH), что особенно важно для выживания раковых клеток в условиях метаболического стресса. С другой стороны, NADPH необходим для синтеза жирных кислот и нуклеотидов, необходимых для поддержания роста и пролиферации клеток, что является неотъемлемой частью биологии опухолевой клетки. Зачастую рост раковой клетки ограничен уровнями NADPH, следовательно, изменения в метаболизме раковой клетки должны учитывать этот важный аспект. Как связаны между собой окисление жирных кислот и производство NADPH? Основным продуктом окисления жиров является ацетил-КоА, который вступает в цикл Кребса и превращается в цитрат. Цитрат может остаться воволеченным в цикл Кребса, а может покинуть митохондрию и выйти в цитоплазму. Там он превратится в изоцитрат, который является субстратом для NADP-зависимой изоцитратдегидрогеназы [13]. Этот фермент окисляет изоцитрат, при этом происходит перенос водорода на NADP+ и образуется NADPH, необходимый раковым клеткам. Например, в клетках глиомы, в которых ингибируется окисление жирных кислот, значительно понижается уровень NADPH, что приводит к накоплению АФК и, как следствие, клеточной гибели [14].
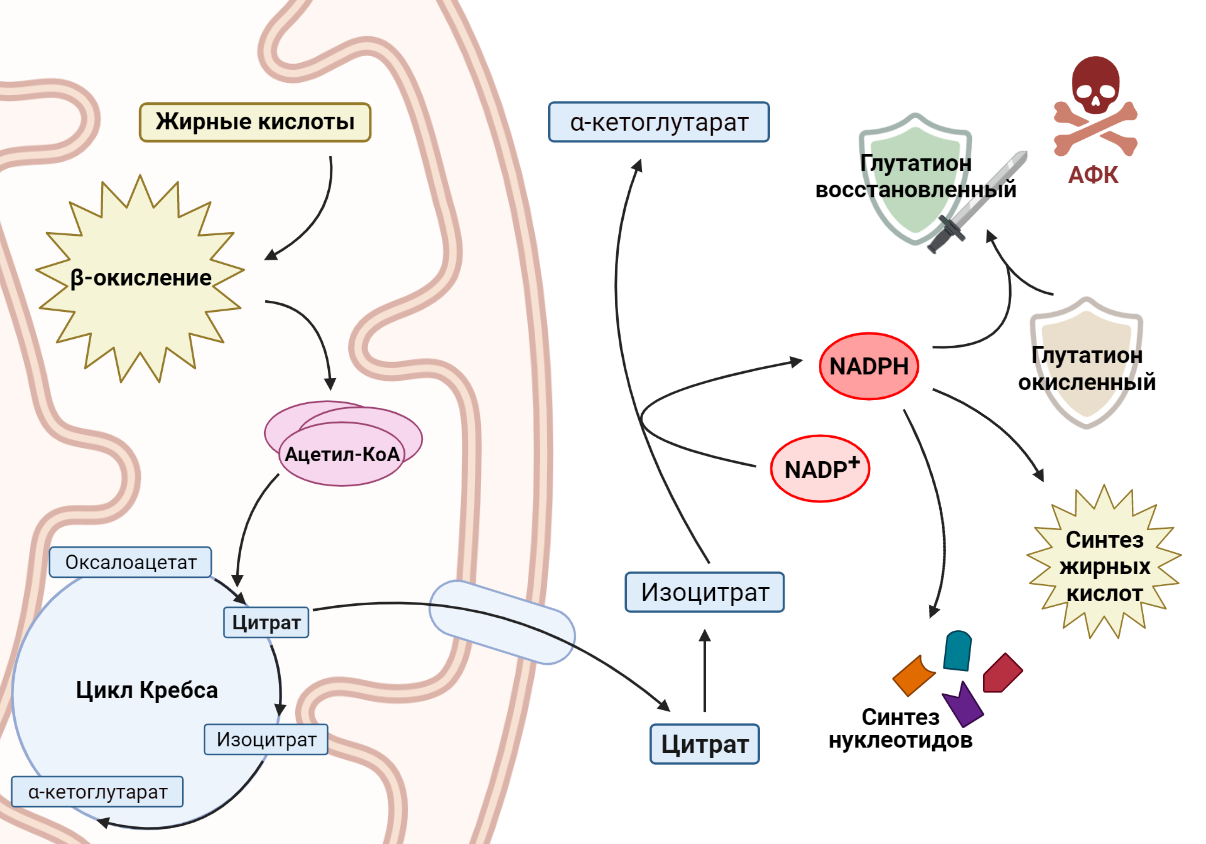
Рисунок 6. Ацетил-КоА, продукт окисления жирных кислот, поступает в цикл Кребса. В то же время цитрат, промежуточное соединение цикла Кребса, покидает митохондрию, где превращается в изоцитрат. При окислении изоцитрата происходит перенос водорода на NADP + , образуется NADPH, необходимый клеткам для множества процессов.
коллаж авторов статьи. Создан с помощью BioRender.com
Из данных примеров мы видим, что в некоторых случаях жирные кислоты способствуют выживанию и метастазированию опухолевых клеток. Это значит, что для отдельных пациентов диета с низким содержанием жиров может оказаться полезной. В то же время, кетогенная диета, которую мы обсуждали в главе про глюкозу, может вызывать непредвиденные проканцерогенные эффекты и способствовать росту опухоли. Таким образом, режим питания пациентов должен подбираться индивидуально с учетом стадии опухоли, ее локализации и особенностей метаболизма.
Аминокислоты
Как известно, белки принимают участие в большинстве клеточных процессов: поддерживают форму клетки, обеспечивают ее подвижность, контролируют работу генов, регулируют метаболические процессы и многое-многое другое. Аминокислоты являются строительными мономерными блоками для белков. Удивительно, что при огромном разнообразии белков, все они построены из довольно ограниченного набора аминокислот (рис. 7).
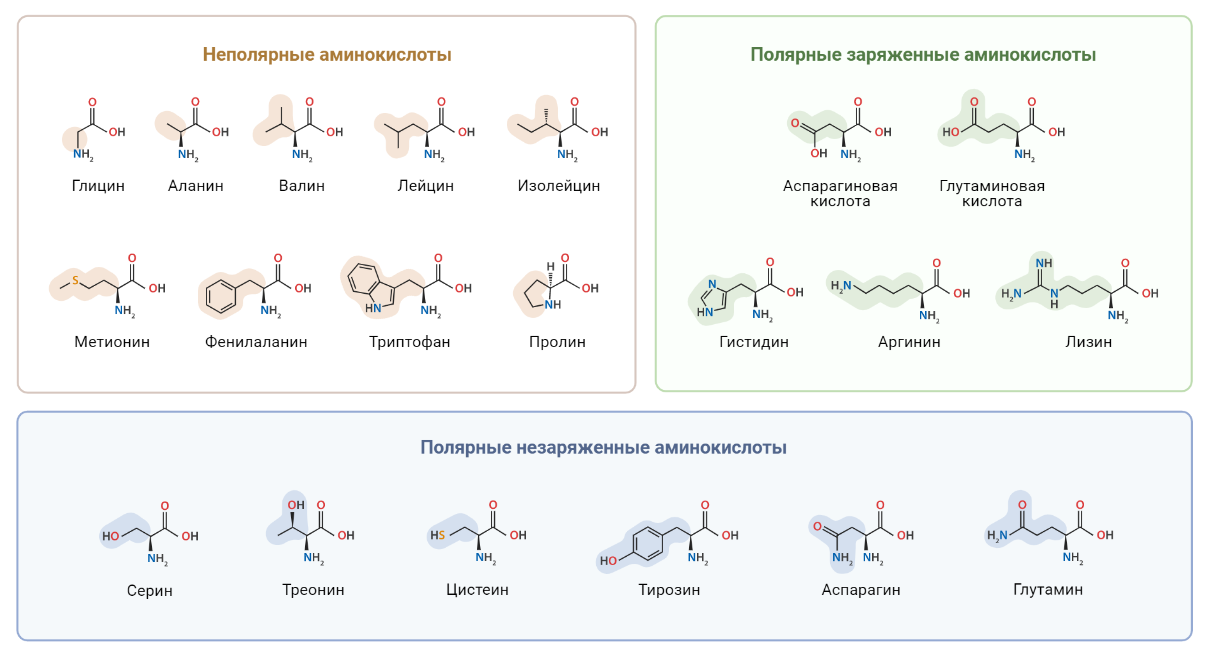
Рисунок 7. 20 классических аминокислот.
С пищей в организм попадают белки, после чего в желудочно-кишечном тракте они деградируют до отдельных аминокислот. Смесь аминокислот всасывается в тонком кишечнике, поступает в кровь и разносится к каждой клетке организма. В клетках аминокислоты используются уже для синтеза собственных белков, которые необходимы для нормального функционирования организма. Важно отметить, что некоторые из аминокислот клетки нашего организма умеют синтезировать сами (так называемые заменимые аминокислоты), а некоторые непременно должны поступать с пищей (незаменимые аминокислоты). Итак, аминокислоты, которые попали в клетку, могут войти в состав белков, но для нас более интересен тот факт, что отдельные аминокислоты могут выполнять специальные метаболические функции. Далее мы будем рассматривать роль конкретных аминокислот в метаболизме раковых клеток, а также возможные диетические стратегии для пациентов с онкологическими заболеваниями, основанные на ограничении или биодобавках данных аминокислот в рационе.
Метионин
Метионин относится к незаменимым аминокислотам для клеток человека. При этом раковые клетки для своего роста требуют бóльшие количества метионина по сравнению с нормальными клетками. Дело в том, что метионин выполняет ряд регуляторных функций. В клетке есть специальные сенсоры, которые в ответ на высокий уровень метионина (а точнее, его производного — S-аденозилметионина) способны активировать протеинкиназу mTORC1. Эта протеинкиназа крайне важна для раковых клеток: она активирует процесс синтеза белка и, как следствие, ускоряет рост и деление клетки [15]. Кроме этого, S-аденозилметионин является главным донором метильной группы в клетке, то есть обеспечивает метилирование. Метилирование ДНК и гистонов (белков, связанных с ДНК) позволяет «включать» и «выключать» определенные гены. Изменения статуса метилирования гистонов и ДНК регулируют экспрессию генов и вносят свой вклад в рост и развитие опухоли [16]. Начиная с 1990 года проводятся исследования на животных, которые демонстрируют, что ограничение потребления метионина улучшает исход лечения опухолей [1], [17]. Совсем недавно было проведено первое клиническое исследование, которое показало, что снижение количества метионина в рационе пациентов позволяет замедлить прогрессирование опухоли [18]. Таким образом, диетическое ограничение метионина у людей, страдающих онкологическими заболеваниями, является весьма многообещающим подходом [1]. Важно уточнить, что диетическое ограничение тех или иных аминокислот можно осуществить только за счет «искусственных» диет, при которых основным источником белковой пищи являются протеиновые напитки/батончики без содержания определенных аминокислот. Именно такой режим питания соблюдали пациенты, принявшие участие в клиническом испытании диеты с низким содержанием метионина: 75% белковой пищи представляли из себя протеиновые напитки без метионина [18].
Серин
Аминокислота серин принимает участие во множестве метаболических процессов: в синтезе нуклеотидов и липидов; она может превращаться в пируват и поступать в цикл Кребса, и так далее. Серин относится к заменимым аминокислотам и может синтезироваться в нормальных клетках из глюкозы и глицина (самой простой аминокислоты). Для раковых клеток, которые активно используют гликолиз и, соответственно, остро нуждаются в глюкозе, синтез серина из глюкозы непременно обернется потерями в количестве АТФ и скорости размножения. Именно поэтому можно сказать, что для опухолевых клеток серин является незаменимой аминокислотой, то есть обязательно должен поступать извне. Путь синтеза серина из глицина для раковых клеток тоже крайне нежелателен, так как глицин принимает непосредственное участие в синтезе нуклеотидов, а значит, превращение глицина в серин опять же ставит под угрозу скорость деления раковых клеток. Таким образом, ограничение потребление серина действительно может помочь в терапии опухолей. Эффективность такой диеты уже была показана в экспериментах на мышах, но клинических исследований пока не проводилось [1].
Аргинин
В нормальных клетках аргинин способен образовываться de novo, то есть является заменимой аминокислотой. В опухолевых клетках меланомы, гепатоцеллюлярной карциномы и рака простаты синтез аргинина сильно снижен. Это связано с низким уровнем фермента аргининосукцинатсинтетазы, участвующем в образовании аргиинина. Выходит, что некоторые раковые опухоли требуют поступление аргинина извне (для клеток этих опухолей аргинин — незаменимая аминокислота). «Аргининовая зависимость» опухолей может быть использована для терапии, причем как в фармакологических подходах, так и в простом диетическом ограничении аргинина. Про фармакологическое снижение аргинина в раковых клетках уже кое-что известно из научных работ: так, например, препараты, снижающие уровень аргинина в плазме крови пациентов, оказались эффективными при лечении гепатоцеллюлярной карциномы и меланомы [19].
Однако аргинин может негативно сказываться на противоопухолевом иммунитете. Важнейшими клетками, участвующими в борьбе с опухолью, являются T-лимфоциты. Аргинин активно поглощается активированными T-клетками, затем метаболизируется, что приводит к увеличению выживаемости клеток и усилению противоопухолевого Т-клеточного ответа. В мышиной модели рака кожи увеличение количества потребляемого с пищей аргинина привело к уменьшению размера опухолей, способствовало выживанию мышей [20].
Не менее важную роль в противоопухолевом иммунитете играют NK-клетки (Natural killer cells, натуральные киллеры) — иммунные клетки, способные уничтожать опухолевые клетки. Исследования показали, что потребление аргинина с пищей увеличивает количество и активность NK-клеток [21], и, наоборот, дефицит аргинина угнетает работу и жизнеспособность натуральных киллеров [22], что может негативно сказаться на борьбе с опухолью.
Таким образом, аргинин необходим как некоторым опухолям для роста, так и иммунным клеткам, сражающимся с опухолью. По-видимому, только масштабные клинические испытания помогут понять, в каких случаях стоит исключать или, наоборот, увеличивать содержание аргинина в пище для достижения максимального эффекта терапии.
Цистин и цистеин
Одна из важнейших функций аминокислоты цистеина в клетке — защита от активных форм кислорода (например, перекиси водорода), которые повреждают ДНК, липиды и белки, вызывая в клетке окислительный стресс. Раковые клетки, по сравнению с нормальными, испытывают сильный окислительный стресс и требуют большого количества цистеина. Действительно, для некоторых опухолевых клеток снижение уровня цистеина губительно: клетки «сгорают» из-за накопленных активных форм кислорода. Цистеин образуется из неклассической аминокислоты цистина, которая поступает в клетку из плазмы крови [1]. Препараты, снижающие уровень цистина в плазме крови, тормозят рост опухолей с мутантным рецептором эпидермального фактора роста (например, немелкоклеточного рака легких) у мышей [23]. Теоретически, достичь снижения уровня цистина в плазме крови пациентов можно при помощи корректировки диеты, без применения препаратов, но такой подход пока не исследован.
Гистидин
При деградации гистидина в клетке тратится тетрагидрофолат — кофактор, который необходим для синтеза нуклеотидов, а значит, определяет скорость деления раковых клеток. Чем больше в раковую клетку поступает гистидина, тем больше тетрагидрофолата тратится на распад гистидина и тем медленнее клетка делится. Применение гистидина вместе с пищей может помочь в терапии некоторых видов опухолей. В частности, такой диетический подход может стать особенно эффективным при лечении рака химиотерапевтическим агентом — метотрексатом (часто применяется для лечения злокачественных заболеваний крови). Метотрексат нарушает синтез тетрагидрофолата, что приводит к остановке синтеза нуклеотидов и к гибели раковых клеток. Оказалось, что эффективность лечения лейкемии метотрексатом заметно увеличивается при добавлении к пище аминокислоты гистидина — это было показано на мышиной модели [24].
Биодобавки фолиевой кислоты
В заключение мы хотим уделить внимание витаминам. Витамины необходимы для протекания многих биохимических реакций и должны поступать в организм с пищей. Существует распространенное заблуждение о том, что прием витаминных биодобавок может послужить защитой от рака и других заболеваний. На самом деле, витамины должны поступать исключительно с пищей, а дополнительный прием витаминов здоровым людям в основном не рекомендован (за некоторыми редкими исключениями). Регулярный прием биодобавок может оказаться не только неэффективными, но и вредным, особенно людям, страдающим онкологическими заболеваниями. Давайте рассмотрим пример того, как дополнительный прием витаминов способствует росту опухоли.
Фолиевая кислота (фолат, витамин B9) является необходимым веществом для синтеза нуклеотидов. Опухолевые клетки быстро делятся и нуждаются в больших количествах нуклеотидов для синтеза ДНК, поэтому активно потребляют фолат. Еще в 1948 году стало известно, что биодобавки фолиевой кислоты способствуют росту некоторых видов опухолей [25]. На сегодняшний день метаболизм фолиевой кислоты является фармакологической мишенью для терапии рака: упоминавшийся ранее химиотерапевтический препарат метотрексат нарушает метаболизм фолата и ингибирует пути синтеза нуклеотидов. Надо подчеркнуть, что антифолиевая терапия рака пока что является сугубо фармакологической и не предполагает корректировки диеты [1].
Однако потенциальные негативные эффекты фолата в опухолевой прогрессии на этом не заканчиваются. Ряд исследований показал, что присутствие в крови неметаболизированной фолиевой кислоты, связанное с ее избыточным потреблением, влекло за собой снижение количества и активности NK-клеток [26-28]. Упоминавшиеся ранее NK-клетки — это иммунные клетки, одна из основных функций которых состоит в защите организма от раковых клеток. Следовательно, снижение числа и подавление активности NK-клеток может повлечь за собой повышенный риск образования и прогрессии рака, хотя конкретных исследований о влиянии высоких доз фолата на противоопухолевый иммунитет не проводилось.
Таким образом, витамины необходимы для поддержания функций организма, однако чрезмерное потребление некоторых из них может привести к негативным последствиям, в том числе и к прогрессии опухоли, как в случае с витамином B9. Возможно, диета с низким содержанием фолата будет полезной для некоторых пациентов.
Заключение
Мы постарались кратко охарактеризовать некоторые особенности метаболизма опухолевых клеток и роль питательных веществ в прогрессии рака. В заключение мы хотели бы еще раз обратить внимание на то, что не существует какой-либо универсальной диеты для людей, страдающих онкологическими заболеваниями. Это связано с тем, что опухоли сильно различаются по своему метаболизму. Перечисленные диетические подходы пока что не могут использоваться повсеместно, так как перед внедрением любого из них для каждого типа рака, его локализации и стадии заболевания должны быть проведены масштабные клинические испытания, подтверждающие безопасность и эффективность нового метода лечения. Однако, ввиду многообещающих результатов исследований, модификации диеты являются перспективным подходом к лечению рака. Мы уверены, что в скором времени контроль состава диеты пациентов станет важной частью терапии онкологических заболеваний и поможет спасти многие жизни. А пока что давайте просто стараться питаться правильно и вести здоровый образ жизни. Будьте здоровы!
Источник https://clinica-paramita.ru/info/557/
Источник https://mz-clinic.ru/articles/10-glavnyh-uprazhnenij-dlja-teh-u-kogo-narusheno-krovoobrashenie.html
Источник https://biomolecula.ru/articles/ratsion-opukholevykh-kletok-ili-rol-pitaniia-v-terapii-raka