Федеральные клинические рекомендации по диагностике и лечению туберкулеза у больных вич-инфекцией
О.Н. Барканова, С.Г. Гагарина, А.А. Калуженина, Н.Л. Попкова
Кафедра фтизиопульмонологии ГБОУ ВПО «Волгоградский государственный медицинский университет» Минздрава РФ, Волгоград
В настоящее время туберкулез и ВИЧ-инфекцию считают закономерными спутниками. В статье подробно рассмотрены вопросы диагностики туберкулеза у больных ВИЧ-инфекцией. Представлены особенности лечения туберкулеза у ВИЧ-инфицированных (противотуберкулезная терапия, хирургическое лечение). Особое внимание уделено антиретровирусной терапии больных ко-инфекцией.
ВИЧ-инфекция – инфекция, вызванная вирусом иммунодефицита человека (human immunodeficiency virus infection – HIV-infection). ВИЧ-инфекция – медленнопрогрессирующее антропонозное заболевание с контактным механизмом передачи, характеризующееся специфическим поражением иммунной системы (преимущественно Т-хелперов), в результате чего организм становится высоковосприимчивым к оппортунистическим инфекциям и опухолям, которые приводят к гибели больного [5].
Диагностика туберкулеза у больных ВИЧ-инфекцией
Подход к диагностике туберкулеза у ВИЧ-инфицированных лиц (взрослых и детей) не отличается от такового у неинфицированных. Однако эффективность такого подхода к лицам, живущим с ВИЧ, имеет ограничения по следующим причинам:
- Клинические проявления, схожие с таковыми туберкулеза легких, могут быть связаны и с другими вторичными заболеваниями, следовательно, менее специфичны для туберкулеза, чем у лиц с ВИЧ-негативным статусом.
- Туберкулиновые кожные пробы у ВИЧ-позитивных лиц при иммуносупрессии обладают меньшей чувствительностью, чем у ВИЧ-негативных.
- ВИЧ-инфицированные лица значительно чаще, чем ВИЧ-негативные, могут иметь заболевания легких, обусловленные несколькими причинами, что может маскировать ответ на противотуберкулезную терапию (ПТТ).
- У ВИЧ-инфицированных лиц рентгенологические изменения в легких при туберкулезе могут быть схожими с другими вторичными оппортунистическими заболеваниями, что затрудняет интерпретацию скиалогической картины специалистами лучевой диагностики.
- Туберкулез, развивающийся у пациентов при значительной иммуносупрессии (уровень CD4+-лимфоцитов менее 200 клеток/мкл), часто носит генерализованный характер с поражением нескольких систем.
- Большинство ВИЧ-инфицирован-ных детей заражаются вирусом перинатально. Поэтому максимальная распространенность ВИЧ-инфекции среди детей приходится на младенцев и детей до 5 лет, которые составляют возрастную группу, где наиболее сложно выяснить причину острого или хронического заболевания легких, в т.ч. и туберкулеза.
- У ВИЧ-инфицированных детей чаще встречаются другие хронические или острые легочные заболевания, чем у ВИЧ-негативных [6].
Все впервые выявленные больные ВИЧ-инфекцией должны быть обследованы на предмет исключения активного туберкулеза и латентной туберкулезной инфекции. Аналогичным образом всем больным туберкулезом должно быть проведено тестирование на ВИЧ.
Процесс диагностики включает несколько этапов [4]:
1. Отбор лиц с клинико-рентгенологическими признаками, подозрительными на туберкулез, осуществляется тремя способами:
1.1. Активно (при проведении планового флюорографического обследования у взрослых и массовой туберкулинодиагностики у детей). Больные ВИЧ-инфекцией являются медицинской группой риска по туберкулезу с показанием проведения подросткам и взрослым флюорографического обследования, а детям туберкулинодиагностики – 2 раза в год [7]. Однако по мере снижения числа CD4+-лимфоцитов (особенно когда их число менее 200 клеток/мкл) активное флюорографическое выявление туберкулеза органов дыхания теряет свою значимость. Это связано с тем, что манифестация и течение туберкулеза у больных ВИЧ-инфекцией значительно отличаются от его начала и течения у лиц с сохранной иммунной системой. Для туберкулеза на фоне ВИЧ-ассоциированной иммуносупрессии характерны пневмониеподобная клиническая картина, нередко острое начало, бурное и быстрое развитие заболевания. Кроме того, пропорционально степени иммунодефицита снижается туберкулиновая чувствительность.
1.2. Активный скрининг четырех клинических симптомов (приоритетное направление в выявлении туберкулеза у людей, живущих с ВИЧ): кашель, лихорадка, ночная потливость и потеря массы тела. Скрининг проводится при каждом обращении пациента за медицинской помощью в любое медицинское учреждение. В отсутствие всех обозначенных клинических симптомов наличие туберкулеза у больного ВИЧ-инфекцией с иммуносупрессией маловероятно. В свою очередь лица с положительными результатами скрининга должны пройти диагностическое обследование для выявления либо активного туберкулеза, либо другого заболевания.
1.3. При обращении за медицинской помощью в учреждения первичной медико-санитарной помощи.
2. Дообследование в учреждениях первичной медико-санитарной помощи:
2.1. Трехкратное исследование мокроты на наличие кислотоустойчивых микобактерий (КУМ).
2.2. Обзорная рентгенография органов грудной клетки.
2.3. Общий анализ крови.
2.4. При подозрении на внелегочную локализацию исследование любого диагностического материала на наличие КУМ.
3. Обследование в учреждениях противотуберкулезной службы. Обязательный диагностический минимум:
3.1. Лучевое рентгенологическое обследование. Рентгенография грудной клетки – цифровая или аналоговая.
Томографическое обследование (спиральная компьютерная томография – СКТ органов грудной клетки или линейные томограммы, необходимость и объем которых определяет рентгенолог с учетом рекомендаций фтизиатра). Проведение СКТ особенно оправданно для больных с глубокой иммуносупрессией (CD4+-лимфоциты менее 100 клеток/мкл) с подозрением на туберкулезный сепсис (в отсутствие изменений на рентгенограмме), а также при наличии диссеминации легочной ткани и внутригрудной лимфаденопатии.
3.2. Ультразвуковое исследование (УЗИ) органов брюшной полости.
3.3. Микроскопия (из 3 проб) и посев мокроты на твердые или жидкие питательные среды (из 2 проб) для выявления микобактерий, ПЦР-(полимеразная цепная реакция)-диагностика с возможностью определения лекарственной чувствительности как минимум к рифампицину, идентификация культуры, выросшей на питательных средах, определение чувствительности микобактерий туберкулеза к противотуберкулезным препаратам (ПТП).
3.4. Исследование числа CD4+-лимфоцитов и РНК ВИЧ (вирусной нагрузки ВИЧ) в крови в начале ПТТ.
3.5. Консультацию врача-инфекциониста для исключения вторичных заболеваний, а также для проведения дифференциальной диагностики туберкулеза с другими заболеваниями проводить как можно раньше.
3.6. Консультацию врача-инфекциониста для назначения или коррекции антиретровирусной терапии (АРВТ) проводить в плановом порядке после получения результатов иммунного статуса и вирусной нагрузки.
3.7. При подозрении на поражение центральной или периферической нервной системы у больного ВИЧ-инфекцией необходимо обеспечить консультацию врача-невролога.
3.8. Консультации других узких специалистов (психиатра, нарколога, ортопеда, окулиста и др.) осуществлять по показаниям, исходя из имеющихся клинико-лабораторных данных.
Если диагноз неясен, необходимо проводить следующие дополнительные методы исследования:
3.9. Инвазивные (по показаниям) для получения биоптата пораженной ткани с проведением комплексного поэтапного изучения биопсийного материала с обязательным проведением цитологического исследования; микроскопической оценки биоптата; гистобактериоскопии с окраской по Цилю–Нильсену. По возможности проводить молекулярно-генетические исследования для выявления ДНК микобактерий туберкулеза (МБТ) в нативном материале и из парафиновых гистологических блоков.
3.10. СКТ или магнитно-резонансная томография (МРТ) головного мозга – показания к назначению определяет врач-невролог.
3.11. СКТ органов брюшной полости – показания к назначению определяет лечащий врач.
3.12. Объем обследования на вторичные заболевания определяет врач-инфекционист.
3.13. Остальные методы лабораторной и инструментальной диагностики (например, УЗИ, эхокардиографию, СКТ/МРТ позвоночника и т.д.) проводят по общим показаниям, исходя из имеющихся клинико-лабораторных данных.
3.14. Пробная противотуберкулезная тест-терапия (еx juvantibus). При подозрении на туберкулез и отсутствии достоверных маркеров специфического воспаления у больных ВИЧ-инфекцией в тяжелом состоянии назначать терапию еx juvantibus с применением четырех ПТП основного ряда с обязательным включением рифампицина или рифабутина. После получения всех результатов обследования представлять на врачебную комиссию для окончательного суждения о диагнозе и лечебной тактике.
Состояние должно быть расценено как «тяжелое» при наличии хотя бы одного из следующих четырех признаков: невозможность передвигаться без посторонней помощи, частота дыхания 30 в минуту и более, пульс 120 в минуту и более, лихорадка 39°С и выше. Тяжесть состояния у таких пациентов оправдывает назначение пробной ПТТ, не дожидаясь выполнения всего комплекса диагностических мероприятий с поиском достоверных признаков туберкулеза и/или альтернативных заболеваний на фоне проводимого лечения.
Лечение пациентов с туберкулезом и ВИЧ-инфекцией
Особенности лечения туберкулеза у больных ВИЧ-инфекцией. Лечение туберкулеза проводится врачом-фтизиатром совместно с врачом-инфекционистом, который назначает и проводит мониторинг (АРВТ), осуществляет консультативную помощь в диагностике и лечении других вторичных заболеваний [1, 2].
К основным принципам лечения туберкулеза у больных ВИЧ-инфекцией добавляются аспекты, имеющие принципиальное значение для успешного ведения этой сложной категории больных:
- совместное ведение больного фтизиатром и инфекционистом;
- своевременное назначение АРВТ;
- по показаниям проведение профилактики других вторичных заболеваний в период лечения туберкулеза;
- своевременная диагностика и адекватная терапия других вторичных заболеваний. Терапия больных сочетанной инфекцией включает ПТТ и АРВТ (назначение последней определяется количеством CD4+-лимфоцитов на момент развития туберкулеза), терапию и профилактику вторичных и сопутствующих заболеваний.
При выборе терапии туберкулеза, сочетанного с ВИЧ-инфекцией, важно оценивать:
- степень иммуносупрессии у больного;
- взаимодействие медикаментов, которые принимает больной, как антиретровирусных, так и противотуберкулезных;
- вероятность возникновения, выявление и коррекцию побочных эффектов;
- вероятность возникновения воспалительного синдрома восстановления иммунной системы – ВСВИС.
Противотуберкулезная терапия больных ВИЧ-инфекцией (режимы химиотерапии). Химиотерапия (ХТ) туберкулеза у больных ВИЧ-инфекцией должна быть начата в максимально ранние сроки после установления диагноза. Эмпирическое назначение ПТП при подозрении на туберкулез у больных ВИЧ-инфекцией оправданно в случае тяжелого состояния пациента.
Выбор режима основывается на данных анамнеза и спектра лекарственной устойчивости выделенного возбудителя [2, 3]. Из анамнеза имеет значение: лечился ли ранее пациент от туберкулеза, результаты теста лекарственной чувствительности (ТЛЧ) в предыдущих случаях лечения, исходы предыдущего лечения, контакт с больным туберкулезом. До получения результатов ТЛЧ важно правильно определить, относится ли пациент к группам высокого риска МЛУ-туберкулеза (туберкулез с множественной лекарственной устойчивостью возбудителя).
Группы высокого риска МЛУ-туберкулеза:
- заболевшие из достоверного контакта с больным МЛУ-туберкулезом;
- больные туберкулезом, ранее получавшие 2 и более неэффективных курсов ХТ туберкулеза;
- больные с рецидивом туберкулеза и другие случаи повторного лечения, если ранее у них была выявлена лекарственная устойчивость к одному из основных препаратов – изониазиду или рифампицину;
- больные с отрицательной клинико-рентгенологической динамикой процесса, а также с сохранением или появлением бактериовыделения на фоне контролируемого лечения по стандартным режимам ХТ;
- дети с остропрогрессирующими формами туберкулеза из контакта с больными, ранее получавшими два и более неэффективных курсов ХТ туберкулеза или умерших от туберкулеза в отсутствие результатов определения лекарственной чувствительности возбудителя.
В настоящее время нет убедительных доказательств, что удлинение сроков терапии более 6 месяцев улучшает результаты лечения больных ВИЧ-инфекцией. Однако ряд исследований показывает, что пролонгированное лечение (до 8–9 месяцев) все же более предпочтительно для этой категории больных. И прежде всего это связано с уменьшением числа рецидивов по сравнению с краткосрочной шестимесячной ХТ.
Не рекомендовано больным ВИЧ-инфекцией использование приема ПТП в интермиттирующем режиме, в т.ч. в фазе продолжения.
Режимы ХТ назначают на основании индивидуальных результатов определения лекарственной устойчивости возбудителя: I – при лекарственной чувствительности, II – при монорезистентности к изониазиду или полирезистентности, III – при эмпирическом назначении ПТП, IV – при МЛУ, V – при широкой лекарственной устойчивости (ШЛУ).
Режимы ХТ и комбинации ПТП Режимы ХТ представлены в таблице.
I режим ХТ назначают больным туберкулезом с лекарственной чувствительностью МБТ. При эмпирической терапии (до получения ТЛЧ МБТ) назначают III режим. Режимы включают 4 препарата первого (основного) ряда: изониазид, рифампицин или рифабутин, пиразинамид, этамбутол. При распространенном и полиорганном туберкулезе в интенсивной фазе к режиму может быть присоединен аминогликозид. Рифабутин назначают вместо рифампицина, если он предпочтителен с точки зрения взаимодействия с АРВТ.
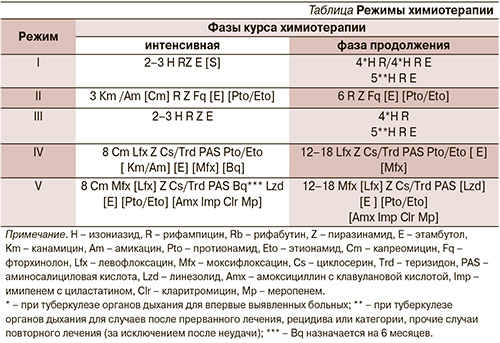
В фазе продолжения терапии назначают три основных препарата с обязательным включением изониазида, рифампицина или рифабутина. Основной курс лечения должен составлять не менее 9 месяцев. У больных туберкулезным менингитом, менингоэнцефалитом, костно-суставным и генерализованным туберкулезом длительность основного курса лечения должна составлять не менее 12 месяцев.
II режим ХТ назначают больным туберкулезом с лекарственной устойчивостью МБТ по крайне мере к изониазиду, но не к сочетанию изониазида и рифампицина по данным ТЛЧ на начало настоящего курса ХТ. Режим включает пять препаратов: рифампицин или рифабутин, пиразинамид, этамбутол, фторхинолон последнего поколения, аминогликозид (канамицин или амикацин) или капреомицин. Препараты, к которым имеется устойчивость микобактерий, больному не назначают, а режим формируется в интенсивной фазе лечения как минимум из четырех, а в фазе продолжения как минимум из трех препаратов, к которым чувствительность возбудителя сохранена. Основной курс лечения должен составлять не менее 12 месяцев.
IV или V режимы ХТ назначают больным туберкулезом при МЛУ или ШЛУ возбудителя. Подходы к терапии с таким видом лекарственной устойчивости практически не отличаются от таковых у больных без ВИЧ-инфекции. Ввиду лекарственных взаимодействий между антиретровирусными препаратами и кларитромицином применение последнего для лечения ШЛУ туберкулеза у больных ВИЧ-инфекцией, получающих АРВТ, не рекомендуется; IV режим ХТ должен состоять как минимум из 5 наиболее эффективных препаратов; IV режим ХТ обязательно должен включать аминогликозид или полипептид, левофлоксацин или моксифлоксацин, пиразинамид.
Длительность ХТ по режиму МЛУ–туберкулез/ВИЧ должна составлять не менее 18 месяцев. Длительность интенсивной фазы по МЛУ–туберкулез/ВИЧ-режиму должна составлять не менее 8 месяцев. IV режим ХТ может быть назначен без лабораторного подтверждения (стандартный), если достоверно известно, что был контакт с больным туберкулезом с МЛУ (множественная устойчивость у вероятного источника заражения должна быть документирована); больным туберкулезом, ранее получавшим 2 и более неэффективных курсов ХТ туберкулеза; больным с рецидивом туберкулеза и в других случаях повторного лечения, если ранее у больного была выявлена лекарственная устойчивость к одному из основных препаратов – изониазиду или рифампицину; больным туберкулезом в отсутствие клинического улучшения при проведении контролируемой ХТ по III режиму в течение 3 недель (при условии исключения ВСВИС).
Коррекция стартового эмпирического режима (III или IV режимы) лечения проводится после получения теста на лекарственную чувствительность. Если на фоне противотуберкулезного лечения в течение месяца по эмпирическому режиму без применения АРВТ наблюдается отрицательная клинико-рентгенологическая динамика, необходимо повторить тест на чувствительность ускоренным молекулярно-генетическим методом.
Дети с ко-инфекцией туберкулез/ВИЧ должны получать терапию, состоящую из комбинации четырех препаратов (изониазид, рифампицин/рифабутин, пиразинамид, этамбутол) в течение минимум 3 месяцев, затем трехкомпонентную терапию (изониазид+рифампицин/рифабутин+этамбутол/пиразинамид) в течение минимум 6 месяцев.
В режиме ПТТ рекомендовано использовать препарат группы рифампицина (рифампицин/рифабутин) весь курс лечения. Поэтому схема АРВТ у детей на период лечения туберкулеза должна быть скорректирована с учетом лекарственных взаимодействий с рифампицином или рифабутином.
При выявлении резистентного туберкулеза или при высоком риске МЛУ–туберкулеза ВИЧ-инфицированным детям и подросткам резервные ПТП могут назначаться по жизненным показаниям независимо от возраста пациента при условии согласия родителей ребенка или законного представителя.
Прогрессирование туберкулезного процесса за первые 3 месяца АРВТ (чаще в первый месяц) может быть связано с ВСВИС. Для дифференциальной диагностики ВСВИС и туберкулеза с МЛУ возбудителя необходимо применение ускоренных молекулярно-генетических методов выявления микобактерий и лекарственной устойчивости.
Хирургическое лечение туберкулеза
у больных ВИЧ-инфекцией. Экстренные и диагностические, а также плановые оперативные вмешательства по поводу туберкулеза и его осложнений проводят исходя из наличия показания, так же как и у больных с ВИЧ-негативным статусом, вне зависимости от степени иммуносупрессии пациента.
Антиретровирусная терапия больных ко-инфекцией
Сочетание ВИЧ-инфекции и туберкулеза обусловливает особый подход к назначению как противотуберкулезной, так и АРВТ. Лечение больных сочетанной патологией ВИЧ/туберкулез довольно сложно, поскольку больному необходимо принимать массу препаратов, между которыми существуют лекарственные взаимодействия.
Основной целью АРВТ служит увеличение продолжительности и сохранение качества жизни пациентов. Приоритетной задачей АРВТ, позволяющей добиваться этих целей, считается максимальное подавление размножения ВИЧ, что выражается в снижении вирусной нагрузки до неопределяемого уровня. Подавление репликации ВИЧ останавливает гибель CD4+-лимфоцитов, что приводит к восстановлению их популяции (рост числа CD4+-лимфоцитов в среднем на 100 клеток в мкл в год) и функциональной активности.
Характеристика схем АРВТ
В настоящее время АРВТ проводится по схемам т.н. высокоактивной терапии, т.е. пациенту одновременно назначают не менее трех антиретровирусных препаратов.
Предпочтительные схемы – схемы с доказанной вирусологической эффективностью, благоприятной переносимостью, экономически обоснованные, назначаемые большинству пациентов.
Альтернативные схемы – схемы с доказанной вирусологической эффективностью, хорошей переносимостью, которые назначают особым категориям пациентов или пациентам при наличии противопоказаний к использованию предпочтительных схем.
Приемлемые схемы – схемы, эффективность которых менее изучена или побочные эффекты выражены в большей степени по сравнению с предпочтительными или альтернативными схемами. Приемлемые схемы могут применяться только при невозможности (например, из-за непереносимости) применения предпочтительных и альтернативных схем.
Основные принципы АРВТ больных ко-инфекцией (ВИЧ-инфекция и туберкулез) практически не отличаются от рекомендаций больным только ВИЧ-инфекцией. Во всех случаях лечение начинают с ПТТ. Сроки начала АРВТ зависят от исходного количества CD4+-лимфоцитов. Больным ВИЧ-инфекцией и туберкулезом с низким числом CD4+-лимфоцитов (
Задержка начала АРВТ может приводить к возникновению новых вторичных заболеваний и даже к смерти больного. При исходном количестве CD4+-лимфоцитов 100–350 клеток/мкл АРВТ присоединяют как можно раньше (в течение первых 2 месяцев после начала ПТТ). При количестве CD4+-лимфоцитов >350 клеток/мкл назначают ПТТ, одновременно проводят контроль количества CD4+-лимфоцитов. Если на фоне лечения туберкулеза число CD4+-лимфоцитов становится < 350 клеток/мкл, назначают АРВТ. Кроме того, при прогрессировании туберкулезного процесса у больных ВИЧ-инфекцией (даже у больных при числе CD4+-лимфоцитов >350 клеток/мкл) целесообразно назначать АРВТ. После завершения терапии туберкулеза АРВТ рекомендуется всем больным ВИЧ-инфекцией (даже при количестве CD4+-лимфоцитов >500 клеток/мкл) с целью профилактики рецидива туберкулеза.
Детям с ко-инфекцией туберкулез/ВИЧ АРВТ назначается вне зависимости от степени иммуносупрессии. Для пациентов с показателем CD4+-лимфоцитов менее 50 клеток/мкл АРВТ должна быть начата в течение 2 недель после начала ПТТ, детям с большим количеством CD4+-клеток – в течение 2 месяцев. При начале АРВТ до развития туберкулеза терапию продолжать.
Лечение активного туберкулеза всегда клинически более важно, чем лечение ВИЧ-инфекции. Несмотря на то что таким больным показано одновременное лечение обеих инфекций, сначала рекомендуется начать лечение туберкулеза и отложить АРВТ хотя бы на 2 недели. Если ПТП хорошо переносятся, можно начинать АРВТ. Такие больные должны находиться под медицинским наблюдением, поскольку для них существует высокий риск развития ВСВИС и тяжелых побочных реакций на комбинированную терапию.
Особые рекомендации по назначению АРВТ имеются при развитии туберкулезного менингита/менингоэнцефалита у больных ВИЧ-инфекцией. Таким больным назначение АРВТ целесообразно отложить хотя бы на 2 месяца после начала ПТТ. Было замечено, что у таких пациентов при немедленно начатой АРВТ наблюдали больше тяжелых побочных эффектов и клиническое ухудшение по сравнению с началом АРВТ через 2 месяца после начала противотуберкулезного лечения. При этом раннее назначение АРВТ не улучшало показатели выживаемости среди больных туберкулезным менингоэнцефалитом.
Помимо показаний к началу АРВТ и сроков ее назначения для больных ВИЧ-инфекцией и туберкулезом серьезной проблемой является выбор оптимальной схемы АРВТ с учетом наличия лекарственных взаимодействий между антиретровирусными и ПТП.
При назначении рифамицинов (рифампицин и рифабутин) вместе с АРВТ необходимо обращать внимание на влияние назначаемых препаратов на ферменты системы цитохрома Р450. Так, рифамицины индуцируют активность ферментов системы цитохрома P450 (в первую очередь изофермента CYP3A4), которые осуществляют метаболизм таких препаратов, как ингибиторы протеазы и в меньшей степени ненуклиозидные ингибиторы обратной транскриптазы (ННИОТ), что приводит к снижению сывороточных концентраций этих АРВП. Индукция рифампицином фермента уридиндифосфат-глюкуронилтрансферазы вызывает снижение концентрации препарата ингибитора интегразы (RAL). В свою очередь ННИОТ, ингибиторы протеазы (ИП) и ингибиторы интегразы через тот же механизм повышают сывороточные концентрации рифампицина. Лекарственные взаимодействия могут приводить к снижению эффективности АРВП и повышению риска гепатотоксических реакций. При этом рифабутин обладает сопоставимой активностью с рифампицином по воздействию на МБТ, поэтому введение его в режим лечения больного ВИЧ-инфекцией более предпочтительно перед рифампицином.
Рекомендации по выбору АРВП для лечения больных ВИЧ-инфекцией, страдающих туберкулезом
Предпочтительная схема: зидовудин (или тенофовир или абакавир)+ламивудин или тенофовир/эмтрицитабин+эфавиренз (в стандартных суточных дозировках) при использовании рифабутина. При использовании рифампицина дозу эфавиренза увеличивают до 800 мг/сут при массе тела пациента >60 кг. Для удобства пациентов и повышения приверженности к лечению рекомендуется назначать комбинированные формы препаратов.
Альтернативные схемы: 3 НИОТ – нуклеозидные ингибиторы обратной трансферазы (зидовудин+ламивудин+абакавир) в стандартных дозах при исходном уровне РНК ВИЧ100 тыс. копий/мл эта схема менее эффективна, чем схема 2 НИОТ+ННИОТ (зидовудин+ламиву-дин+эфавиренз).
Два НИОТ (зидовудин+ламивудин в стандартных дозах)+невирапин 0,2 г 1 раз в сутки в течение 14 дней, далее по 0,2 г 2 раза в сутки (невирапин следует назначать женщинам при числе CD4+-лимфоцитов
В сочетании с рифампицином уро-вень невирапина в крови может быть ниже терапевтического, возможно также усиление гепатотоксичности препаратов.
Тенофовир (зидовудин)+ламивудин (в стандартных дозах)+ралтегравир в стандартных дозах при использо-вании в схеме ПТТ рифабутина и 0,8 г 2 раза в сутки при использовании рифампицина.
Пациентам с предшествующим опытом АРВТ: 2 НИОТ (зидовудин+ламивудин в стандартных дозах) + энфувиртид 90 мкг 2 раза в сутки подкожно или маравирок 0,3 г 2 раза в сутки при использовании в схеме рифабутина и 0,6 г 2 раза в сутки при использовании рифампицина.
При использовании в схеме АРВТ эфавиренза, ралтегравира или маравирока целесообразно заменить рифампицин на рифабутин в среднетерапевтической дозе (300–450 мг/сут).
При назначении в составе АРВТ ИП ВИЧ, усиленного ритонавиром, рифампицин необходимо заменить на рифабутин (150 мг/сут). Не рекомендуется одновременный прием рифампицина и ИП ВИЧ, усиленных или не усиленных стандартной дозой ритонавира.
При необходимости применения в составе схемы ПТТ препарата рифампицин и отсутствия возможности использования других вариантов схемы АРВТ (включающих 3 НИОТ, ННИОТ, ингибитор интегразы или антагонист рецепторов CCR5) в качестве приемлемого режима АРВТ пациенту может быть назначена схема АРВТ, включающая 2 НИОТ+лопинавир/ритонавир в двойной суточной дозе (800/200 мг 2 раза в сутки) или лопинавир/ритонавир в стандартной суточной дозе (400/100 мг 2 раза в сутки) с добавлением ритонавира в дозе 300 мг 2 раза в сутки.
При переключении с режима на основе рифампицина на рифабутин или на режим, не содержащий рифампицина, необходимо отложить не менее чем 2 недели начало АРВТ – так, чтобы эффект от рифампицина не влиял на активность АРВП.
Если необходимо в схеме ПТТ оставить рифампицин (например, для парентерального введения), увеличивают дозу эфавиренза до 800 мг/сут при массе тела пациента >60 кг, ралтегравира до 800 мг 2 раза в сутки (вне зависимости от массы тела), а препарата маравирок – до 600 мг 2 раза в сутки.
Литература
- Рекомендации по лечению туберкулеза. Перевод с англ. ВОЗ, Женева, 2010. 152 с.
- Федеральные клинические рекомендации по диагностике и лечению туберкулеза у ВИЧ-инфицированных. Российское общество фтизиатров. М., 2014. 38 с.
- Федеральные клинические рекомендации по диагностике и лечению туберкулеза органов дыхания с множественной и широкой лекарственной устойчивостью возбудителя. Российское общество фтизиатров. М. 47 с.
- Федеральные клинические рекомендации по диагностике и лечению туберкулеза органов дыхания. Российское общество фтизиатров. М., 2014. 38 с.
- Фтизиатрия: национальное руководство / Под ред. М.И. Перельмана. М., 2010. 506 с.
- Семенова Н.Ю., Чеботарева Т.В., Бог-данова Л.И., Демидов В.И. Клинико-морфологические особенности ВИЧ-инфицированного туберкулеза Эпидемиол. инфекц. болезни. Актуал. вопр. 2014;3: 30–34.
- Кисличкин Н.Н., Фурс С.М., Красильников И.В., Зазимко Л.А. Диагностика туберкулеза. Туберкулин или диаскинтест – что выбрать? Эпидемиол. инфекц. болезни. Актуал. вопр. 2014;5:50–55.
Об авторах / Для корреспонденции
О.Н. Барканова– к.м.н., зав. кафедрой фтизиопульмонологииГБОУ ВПО «Волгоградский государственный медицинский университет» Минздрава РФ, Волгоград; e-mail:barkmed@mail.ru
С.Г. Гагарина –к.м.н., ассистент кафедры фтизиопульмонологии ГБОУ ВПО «Волгоградский государственный медицинский университет» Минздрава РФ, Волгоград; e-mail:s.g.gagarina@mail.ru
А.А. Калуженина– к.м.н., ассистент кафедры фтизиопульмонологияГБОУ ВПО «Волгоградский государственный медицинский университет» Минздрава РФ, Волгоград;e-mail: peace81.81@mail.ru
Н.Л. Попкова – к.м.н., доцент кафедры фтизиопульмонологии. ГБОУ ВПО «Волгоградский государственный медицинский университет» Минздрава РФ, Волгоград
Сочетанная ВИЧ/ТБ инфекция
Сочетанная ВИЧ/туберкулез инфекция – наличие активного туберкулеза у больного ВИЧ-инфекцией.
Название протокола: Сочетанная ВИЧ/ТБ инфекция
Код(ы) МКБ 10:
| МКБ 10 | |
| Код | Название |
| B20 | Болезнь, вызванная вирусом иммунодефицита человека (ВИЧ), проявляющаяся в виде инфекционных и паразитарных болезней. |
| B21 | Болезнь, вызванная вирусом иммунодефицита человека (ВИЧ), проявляющаяся в виде других уточненных болезней. |
| B22 | Болезнь, вызванная вирусом иммунодефицита человека (ВИЧ), проявляющаяся в виде злокачественных новообразований. |
| B23 | Болезнь, вызванная вирусом иммунодефицита человека (ВИЧ), проявляющаяся в виде других состояний. |
| B24 | Болезнь, вызванная вирусом иммунодефицита человека (ВИЧ), неуточненная. |
| A15.0 | Туберкулез органов дыхания, подтвержденный бактериологически и гистологически |
| A16.0 | Туберкулез органов дыхания, не подтвержденный бактериологически или гистологически |
| A17.0 | Туберкулез нервной системы |
| A18.0 | Туберкулез других органов |
| A19.0 | Милиарный туберкулез |
Дата разработки протокола: 2018 год
Пользователи протокола: врачи — инфекционисты, терапевты, врачи общей практики, врачи-лаборанты, фтизиатры, акушер-гинекологи, хирурги.
Категория пациентов: взрослые, беременные женщины, дети.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты, которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных исследований случай-контроль или высококачественное (++) когортное исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование, или мнение экспертов. |
| GPP | Наилучшая клиническая практика. |

Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
— 800 RUB / 5500 KZT / 27 BYN — 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место — 800 RUB / 5500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
[7]: Клинические стадии ВИЧ-инфекции при сочетании с туберкулезом по классификации ВОЗ у взрослых.
Клиническая стадия 3
- туберкулез легких;
- внелегочный туберкулез;
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Подход к диагностике туберкулёза у ВИЧ-инфицированных лиц (взрослых и детей) существенным образом не отличается от такового у неинфицированных. Однако эффективность такого подхода у ЛЖВ может иметь ограничения по следующим причинам:
· клинические проявления, схожие с проявлениями туберкулёза, могут быть связаны и с другими вторичными заболеваниями, и, следовательно, менее специфичны для туберкулёза, чем у лиц с ВИЧ-негативным статусом.
· Иммунологические тесты (ТКП, тест с АТР) у ВИЧ-позитивных лиц (у взрослых и детей) при иммуносупрессии обладают меньшей чувствительностью, чем у ВИЧ-негативных.
· ВИЧ-инфицированные лица значительно чаще, чем ВИЧ-негативные, могут иметь заболевания, обусловленные несколькими причинами, что может маскировать ответ на противотуберкулёзную терапию.
· У ВИЧ-инфицированных лиц рентгенологические изменения в легких при туберкулёзе могут быть схожими с другими вторичными и ассоциированными заболеваниями, что затрудняет интерпретацию скиалогической картины специалистами лучевой диагностики.
· Туберкулёз, развивающийся у пациентов при значительной иммуносупрессии (уровень CD4+лимфоцитов менее 200 клеток/мкл), часто носит генерализованный характер с одновременным поражением нескольких систем и органов.
· Большинство ВИЧ-инфицированных детей заражаются вирусом перинатально. Поэтому максимальная распространенность ВИЧ-инфекции среди детей приходится на младенцев и детей до 5 лет, которые составляют возрастную группу, где наиболее сложно выяснить причину острого или хронического заболевания лёгких, в том числе и туберкулёза.
· У ВИЧ-инфицированных детей чаще встречаются хронические или острые лёгочные заболевания, чем у ВИЧ-негативных.
· Все впервые выявленные больные ВИЧ-инфекцией (взрослые и дети) должны быть обследованы на предмет исключения латентной туберкулёзной инфекции и активного туберкулёза.
· Всем больным туберкулёзом и с подозрением на туберкулез должно быть предложено тестирование на ВИЧ с проведением до — и послетестового консультирования. Повторное тестирование на ВИЧ пациентов с активным туберкулезом проводится каждые 6 месяцев.
Процесс диагностики туберкулёза включает несколько этапов.
1. Отбор лиц с клинико-рентгенологическими признаками, подозрительными на туберкулёз, осуществляется тремя способами:
— при проведении планового флюорографического обследования у взрослых, теста с АТР (или IGRA-тестов) и массовой туберкулинодиагностики у детей. Больные ВИЧ-инфекцией являются медицинской группой риска по туберкулёзу с необходимостью проведения подросткам и взрослым флюорографического обследования, а детям – туберкулинодиагностики 1 раз в год.
Однако по мере снижения количества CD4+лимфоцитов (особенно когда количество CD4+лимфоцитов менее 200 клеток/мкл) активное флюорографическое выявление туберкулёза органов дыхания теряет свою значимость. Манифестация и течение туберкулёза у больных ВИЧ-инфекцией значительно отличаются от его начала и течения у лиц с сохранной иммунной системой. Для туберкулёза на фоне ВИЧ-ассоциированной иммуносупрессии характерна пневмониеподобная клиническая картина, нередко острое начало, бурное и быстрое развитие заболевания. Также пропорционально степени иммунодефицита снижается чувствительность иммунологических тестов;
— по активному скринингу четырех клинических симптомов (приоритетное направление в выявлении туберкулёза у людей, живущих с ВИЧ): кашель, лихорадка, ночная потливость и потеря массы тела. Скрининг должен проводиться при каждом обращении пациента за медицинской помощью в любое медицинское учреждение.
2. При отсутствии всех обозначенных клинических симптомов наличие туберкулёза у больного ВИЧ-инфекцией с иммуносупрессией маловероятно. В свою очередь, лица с положительными результатами скрининга должны пройти диагностическое обследование для выявления либо исключения активного туберкулёза при обращении за медицинской помощью в учреждения первичной медико-санитарной помощи (ПМСП).
3. Людей, живущим с ВИЧ у кого отсутствует любой из четырех симптомов, которые являются показанием для обследования на наличие активного ТБ (длительный кашель, лихорадка, потеря веса и ночная потливость) следует обследовать на наличие латентной ТБ инфекции (ЛТБИ) и/или рассматривать назначение профилактического лечения ТБ, независимо от назначенной АРТ.
4. ЛЖВ у кого был близкий контакт с пациентом с легочным ТБ должны получать лечение от латентной ТБ инфекции независимо от результатов туберкулиновой кожной пробы или IGRA.
5. Лицам, живущим с ВИЧ и принимающим АРТ можно провести рентгенографию грудной клетки, а также назначить профилактическое лечение ТБ тем, у кого отсутствуют симптомы активного ТБ и патологические изменения на рентгенограмме.
Диагностические критерии [3,7,9,13,16,17]
Жалобы: длительный кашель более 2 недель, лихорадка, потеря веса, ночная потливость.
- постепенное начало заболевания;
- на фоне ВИЧ-ассоциированной иммуносупрессии характерна пневмониеподобная клиническая картина, нередко острое начало, бурное и быстрое развитие заболевания;
- контакт пациента с больным туберкулезом;
- данные о вакцинации и ревакцинации БЦЖ;
- материально-бытовые условия жизни;
- характер питания;
- отягощенный семейный и аллергологический анамнез;
- социальный статус.
- измерение массы тела (потеря веса (<10%), сильная потеря веса (>10%), кахексия);
- измерение температуры тела (лихорадка более месяца);
- оценка частоты дыхания (одышка в покое, кашель, хрипы);
- пальпация лимфатических узлов (увеличение лимфатических узлов);
- осмотр грудной клетки (ограничение подвижности одной половины грудной клетки);
- осмотр кожных покровов (бледность).
Общий анализ мочи: анализ мочи у больных туберкулезом практически нормальный. Патологические изменения в моче могут быть при поражении туберкулезом почек или мочевыводящих путей. У больных с хроническими формами туберкулеза легких или костей могут быть выявлены признаки амилоидоза.
Биохимический анализ крови: при острых формах заболевания, а также при обострении и прогрессировании хронических форм туберкулеза уменьшается альбумин-глобулиновый коэффициент. При возникновении в легких фиброзных изменений, возрастает активность ангиотензин-конвертирующего фермента в сыворотке крови. При туберкулезе печени происходит увеличение количество общего билирубина в крови и аминотрансфераз (АСТ и АЛТ). При туберкулезе происходит также увеличение количества содержания холестерина, лизоцима, мочевой кислоты и меди в сыворотке крови.
Выявление возбудителя ТБ: микроскопия, посев и ПЦР как минимум из двух образов мокроты, собранной до начала химиотерапии. Достаточным основанием для этиологического подтверждения диагноза «туберкулёз» может быть выявление микобактерий туберкулёзного комплекса хотя бы в одном образце. При подозрении на туберкулёз внелегочной локализации микроскопия и посев иного диагностического материала (ликвора, экссудата, отделяемого из свища, асцитической жидкости, мочи, кала и др.)
Методы:
· Метод окраски по Цилю-Нильсену (обязательно)
· Люминесцентная микроскопия (в лабораториях при количестве исследований 30 и более в день).
· Культивирование и идентификация M. tuberculosis с использованием как минимум двух разных по составу питательных сред.
· Молекулярно-генетические методы (биочиповая, стриповая, картриджная технологии, ПЦР в режиме реального времени).
· Липоарабинноманнановый (LF-LAM) тест мочи для диагностики ТБ у ЛЖВ взрослых с признаками или симптомами ТБ (легочного и/или внелегочного) с уровнем CD4 клеток ≤100 cells/μL., а также для ЛЖВ в тяжелом состоянии независимо от уровня CD4 или у кого уровень CD4 неизвестен.
· Тест T-SPOT TB
Дифференциация МБТ от НТМБ:
· По особенностям роста культуры (скорость роста, пигментообразование) и биохимическим тестам (обязательно).
· При культивировании на жидких питательных средах проводится тестирование на контаминацию (микроскопия культуры с окраской по Цилю-Нильсену и посев на кровяной агар), а затем принадлежность к микобактериям туберкулёзного комплекса подтверждается молекулярными методами.
· Молекулярные (иммунохроматографический тест, генетические методы ПЦР IS6110, стриповая технология, протеомный масс-спектрометрический анализ).
Определение лекарственной чувствительности (ЛЧ) возбудителя:
Определение лекарственной устойчивости к препаратам резервного ряда проводятся после выявления ЛУ/МЛУ при проведении ТЛЧ к препаратам основного ряда. При двукратном подтверждении устойчивости возбудителя к ПТП любыми методами, в дальнейшем исследование к этим препаратам может не проводиться.
· Фенотипические методы – культивирование МБТ в присутствии противотуберкулёзных препаратов.
· На плотных средах методом абсолютных концентраций по числу выросших колоний.
· На плотных средах методом абсолютных концентраций с применением нитратредуктазного теста.
· На жидких средах – ВАСТЕС MGIT 960 методом пропорций.
· Молекулярно-генетические методы – выявление специфических мутаций, связанных с резистентностью к определенным препаратам.
· Определение лекарственной чувствительности МБТ к препаратам основного ряда (биочиповая, стриповая, картриджная технологии, ПЦР в режиме реального времени).
· Определение лекарственной чувствительности МБТ к препаратам второго ряда (биочиповая, стриповая технологии).
Вместо стандартной микроскопии, культурального исследования и теста на лекарственную чувствительность (ТЛЧ) следует использовать Xpert MTB/RIF в качестве первоначального диагностического теста у взрослых и детей с подозрением на ТБ с множественной лекарственной устойчивостью (МЛУ-ТБ) или ВИЧ-ассоциированный ТБ (взрослые: сильная рекомендация, высокое качество доказательств; дети: очень низкое качество доказательств).
Методу Xpert MTB/RIF следует отдать предпочтение перед стандартной микроскопией и культуральным исследованием как первоначальному диагностическому тесту для образцов спинномозговой жидкости у пациентов с подозрением на ТБ-менингит (сильная рекомендация, очень низкое качество доказательств).
Метод Xpert MTB/RIF можно использовать вместо обычных методов (включая стандартную микроскопию, культуральное или гистопатологическое исследование) при тестировании отдельных нереспираторных образцов (лимфатических узлов и других тканей) у пациентов с подозрением на внелегочный ТБ (условная рекомендация, очень низкое качество доказательств).
| Метод | Показания | УД* |
| Гематологический | Пациенты с клиническими критериями ВИЧ/ТБ-инфекции для определения степени тяжести. | С |
| Биохимический | Пациенты с клиническими критериями ВИЧ/ТБ-инфекции для определения степени тяжести. | С |
| Серологический (ИФА, ИБ) | Пациенты с ТБ для определения ВИЧ-инфекции. | А |
| Молекулярно-генетический (ПЦР) | Пациенты с ВИЧ-инфекцией для диагностики ТБ, и мониторинга АРТ, пациенты с клиническими критериями ВИЧ/ТБ-инфекции для определения лекарственной устойчивости | А |
| Микроскопический | Пациенты с ВИЧ-инфекцией для диагностики ТБ | А |
| Культуральные | Пациенты с клиническими критериями ВИЧ/ТБ-инфекции для определения лекарственной устойчивости и постановки диагноза | А |
Примечание — *уровень доказательности
Инструментальные исследования:
| Метод | Показания | УД* |
| УЗИ органов брюшной полости | Пациенты с клиническими критериями ВИЧ/ТБ-инфекции для определения пораженности органов | В |
| Рентгенография органов грудной клетки | Пациенты с клиническими симптомами ВИЧ-инфекции, аускультативные изменения в легких, при подозрении на туберкулез. | А |
| ФГДС | Пациенты с клиническими критериями ВИЧ/ТБ-инфекции для определения пораженности органов | В |
| МРТ/КТ | Пациенты с клиническими критериями ВИЧ/ТБ-инфекции для определения пораженности органов | В |
| ЭКГ | Пациенты с клиническими симптомами ВИЧ-инфекции, с аускультативными изменениями в сердце для уточнения нарушения функции проведения и трофики ткани сердца. | С |
Примечание — *уровень доказательности
- консультация фтизиатра: при признаках/подозрении на туберкулез, МАК-комплекс;
- консультация невропатолога: при признаках/подозрении на криптококковый менингит, ВИЧ-энцефалопатию, токсоплазмоз ЦНС, ПМЛ, лимфомы головного мозга, периферической полинейропатии;
- консультация психиатра: при признаках/подозрении психического расстройства. ВИЧ-энцефалопатии/деменции, депрессии;
- консультация офтальмолога: при признаках/подозрении на ретинит;
- консультация кардиолога: при признаках/подозрении кардиомиопатии, сердечно-сосудистых заболеваний;
- консультация онколога: при признаках/подозрении на злокачественное новообразование;
- консультация гинеколога: признаках/подозрении на рак шейки матки.
- для взрослых и подростков, живущих с ВИЧ: наличие кашля, лихорадка, потеря веса и ночная потливость.
- для детей, живущих с ВИЧ: плохая прибавка в весе, лихорадка, наличие кашля или контакт с ТБ случаем.

Алгоритм скрининга ЛЖВ для профилактического лечения ЛТБИ и исключения активного туберкулеза
а Необходимо оценить каждого взрослого и подростка для того, чтобы решить подлежит ли он лечению АРТ. Меры инфекционного контроля должны быть приоритетными во всех учреждениях где оказывают медицинскую помощь для предотвращения передачи M. tuberculosis.
б Можно сделать рентгенографию грудной клетки если имеется такая возможность, особенно ЛЖВ на АРТ, но не требуется для классификации пациентов по группам пациенты с ТБ и нет ТБ. В местах с высокой распространенностью ВИЧ и высокой распространенностью ТБ среди ЛЖВ (т.е. >10%), следует уделить серьезное внимание необходимости проведения других более чувствительных методов исследования.
в К противопоказаниям относятся: активный гепатит (острый или хронический), регулярное и чрезмерное потребление алкоголя, и симптомы нейропатии. Туберкулез в анамнезе и наличие беременности не являются противопоказанием для начала профилактического лечения. Хотя обследование на ЛТБИ не требуется для начала профилактического лечения, оно может быть проведено там, где это возможно для того, чтобы определить подлежит ли пациент профилактическому лечению.
Xpert MTB/RIF должен быть использован как первоначальный диагностический тест на ТБ.
г Продолжать регулярный скрининг на ТБ после завершения лечения активного ТБ.
Дифференциальный диагноз
| Заболевание | Сходные симптомы | Отличительные симптомы | Лабораторные тесты |
| Инфекционный мононуклеоз | Лимфоаденопатия, лихорадка | Длительность не более 1 мес., преобладает системное увеличение лимфоузлов. | Положительный тест Пауля-Буннеля. В крови атипичные мононуклеары более 10%. |
| Аденовирусная инфекция | Лихорадка, назофарингит, лимфаденит | Эпиданамнез, острое течение, лимфаденит преимущественно регионарных лимфоузлов | Вирусология, серология с нарастанием титра АТ, иммунофлюоресцентное исследование, гемограмма. |
| Энтеровирусная инфекция | Лихорадка, полиадения, | Герпангина, диарея, лимфаденит менее выражен. | Серология в нарастающем титре. |
| Сепсис | Лихорадка, интоксикация, полиорганность проявлений, экзантема, менингит, отит, синусит, пневмонии. | Наличие первичного очага (кожа, легкие, кишечник и др.) | Выделение возбудителя из крови и др. материала, отрицательный тест на ВИЧ-АТ, гипогаммаглобулинемия, нормальное количество СД-4. |
| Кишечная инфекция, сальмонеллез (генерализованная форма). | потеря массы, лихорадка, интоксикация, наличие очагов в других органах (менингит, пневмония) | Генерализованные формы развиваются только у детей первых месяцев жизни Преморбидный фон отягощен, чаще внутрибольничная инфекция | Посевы кала, крови, серология (РПГА) |
| Бактериальная пневмония (пневмококк, гемофилус, микоплазма) | кашель, субфебрильная температура, постепенно нарастающая одышка при физической нагрузке | Не отличаются | Микроскопия мазков мокроты после их окраски по Цилю — Нильсену, посев мокроты на твёрдую питательную среду Левенштейна–Йенсена «Золотой стандарт диагностики» — бронхо-альвеолярный лаваж с выделением возбудителя до начала антибактериальной терапии |
| Грибковая инфекция (криптококк, гистоплазма) | лихорадка, кашель с мокротой | Одышка, снижение массы тела | Микроскопия, тест латекс-агглютинация, ПЦР для определения ДНК C. Neoformans, посев на питательные среды для грибов, рентгенография, КТ |
| Токсоплазмоз | кашель, одышка, лихорадка | Не отличаются | РИФ и реакция преципитации, Исследование спинномозговой жидкости на ДНК T. gondii у ВИЧ-инфицированных с поражением ЦНС отличается низкой чувствительностью, но высокой специфичностью |
| Эндокардит | гектическая лихорадка обычно 38°С-39°С (при остром эндокардите может быть и выше) с потрясающим ознобом, реже ощущение сильной зябкости (у пожилых и ослабленных пациентов температура может не превышать субфебрильных значений); ночной пот; отсутствие аппетита; рвота; тошнота; быстрое похудание; боли в суставах (полиартралгии у 20% пациентов, могут поражаться мелкие суставы кистей и стоп, но чаще поражаются крупные суставы). | Не отличаются | |
| Лимфома, KS, MCD | кашель и одышка, поражение кожи всегда | Не отличаются | Рентгенография, фибробронхография, сцинтиграфия легких |
| MAK | слабость, утомляемость, лихорадка, похудение, ночная потливость | Не отличаются | микроскопии лимфатического узла, печени, пунктат костного мозга, кал, ИФА с использованием моноклональных антител, ПЦР в реальном времени. Кровь, биоптат лимфатического узла, пунктат костного мозга сеют на среду Левенштейна – Йенсена. |
Если диагноз не ясен, необходимо выполнить дополнительные методы исследования. Дополнительные методы исследования проводят в учреждениях ПМСП или специализированных диагностических отделениях противотуберкулёзных учреждений.
— при подозрении на туберкулёз внелегочной локализации в учреждениях ПМСП проводится обследование, включающее следующие клинические исследования: лучевое (рентгенологическое, томографическое, МСКТ с контрастированием), ультразвуковое, магнитно-резонансное или специальное, (с учетом пораженного органа) инструментальное исследование; осмотр врачом-специалистом с учетом локализации предполагаемого очага туберкулёза;
— инвазивные методы диагностики выполняются с целью получения биоптата пораженной ткани для его комплексного исследования с обязательным проведением следующих исследований: цитологического, микробиологического, молекулярно-генетического, гистологического с проведением гистобактериоскопии с окраской по Цилю-Нильсену;
В учреждениях ПМСП при невозможности проведения полного спектра диагностических мероприятий у больных ВИЧ-инфекцией, находящихся в тяжелом состоянии, с выраженным иммунодефицитом при СD4+ < 100 клеток в мкл, тест-терапия туберкулёза назначается и проводится по решению врачебной комиссии (ВК) медицинской организации с обязательным участием врача-фтизиатра.
Преобладание экссудативного компонента воспаления, практически полное отсутствие продуктивных реакций позволяет оценить результаты тестовой терапии не позднее 10-14 дня от ее начала, основываясь на динамике симптомов интоксикации, в первую очередь, по динамике снижения температуры тела. Начиная с первого дня тест-терапии, проводится ежедневная 3-х кратная термометрия тела, оценивается динамика общего состояния больного. В конце 2 недели проводится контрольная обзорная рентгенография органов грудной клетки. По совокупной оценке, динамики клинических симптомов и сравнению результатов обследования в конце тест-терапии делается решением ВК заключение о наличии туберкулёза.
Лечение
Препараты (действующие вещества), применяющиеся при лечении
| Клофазимин ( Clofazimine) |
| Абакавир (Abacavir) |
| Амикацин (Amikacin) |
| Амоксициллин (Amoxicillin) |
| Долутегравир (Dolutegravir) |
| Зидовудин (Zidovudine) |
| Изониазид (Isoniazid) |
| Канамицин (Kanamycin) |
| Капреомицин (Capreomycin) |
| Клавулановая кислота (Clavulanic acid) |
| Ламивудин (Lamivudine) |
| Левофлоксацин (Levofloxacin) |
| Линезолид (Linezolid) |
| Моксифлоксацин (Moxifloxacin) |
| Невирапин (Nevirapine) |
| Офлоксацин (Ofloxacin) |
| Пара-аминосалициловая кислота (Para-aminosalicylic acid) |
| Пиразинамид (Pyrazinamide) |
| Протионамид (Prothionamide) |
| Ралтегравир (Raltegravir) |
| Рифампицин (Rifampicin) |
| Сульфаметоксазол (Sulphamethoxazole) |
| Тенофовир (Tenofovir) |
| Триметоприм (Trimethoprim) |
| Циклосерин (Cycloserine) |
| Эмтрицитабин (Emtricitabine) |
| Этамбутол (Ethambutol) |
| Этионамид (Ethionamide) |
| Эфавиренз (Efavirenz) |
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ [1-21]
Лечение туберкулеза и антиретровирусную терапию следует начинать как можно быстрее после подтверждения диагноза.
Немедикаментозное лечение:
Режим, диета: зависит от поражения отдельных систем и органов.
Медикаментозное лечение:
Все ЛЖВ с диагностированным туберкулезом нуждаются в лечении ТБ и ВИЧ-инфекции, независимо от числа лимфоцитов CD4 (сильная рекомендация, A).
Первым начинают противотуберкулезное лечение, а затем как можно быстрее (в первые 8 недель лечения) назначают АРТ (сильная рекомендация, A).
Больным ВИЧ/ТБ, имеющим выраженный иммунодефицит (число лимфоцитов CD4 менее 50 клеток/мкл), необходимо начать АРТ немедленно – в течение первых 2 недель после начала лечения ТБ (сильная рекомендация, A).
При наличии туберкулезного менингита начало АРТ следует отложить до завершения фазы интенсивной терапии ТБ (сильная рекомендация, A).
В начале АРТ у больных, получающих противотуберкулезное лечение, предпочтительным ННИОТ является эфавиренз, который назначают вместе с двумя НИОТ (сильная рекомендация, A).
Новых ЛЖВ с ТБ, можно лечить по схеме на основе рифампицина, которая предусматривает ежедневный прием изониазида, рифампицина, пиразинамида и этамбутола в течение первых двух месяцев (фаза интенсивного лечения), а затем изониазид и рифампицин ежедневно в течение четырех месяцев (фаза продолжения лечения). В случаях, когда ежедневный прием лекарств невозможен, приемлемой альтернативной схемой в фазе продолжения лечения является прием изониазида и рифампицина три раза в неделю.
Если туберкулез развивается у ЛЖВ на фоне получения АРТ, ее следует продолжать (если нет признаков неудачи лечения), а схему лечения ТБ выбирать в соответствии с полученными результатами лекарственной чувствительности к противотуберкулезным препаратам.
Лечение чувствительных форм ТБ и ВИЧ
Лечение больных I категории (новых случаев):
1) интенсивная фаза проводится в сроки от двух до четырех месяцев, в зависимости от тяжести и распространенности туберкулезного процесса в ежедневном режиме 7 календарных дней в неделю. Лечение проводится четырьмя противотуберкулезными препаратами: изониазидом (H), рифампицином (R), пиразинамидом (Z) и этамбутолом (E) или стрептомицином (S) в соответствующих весу дозировках, причем приоритет отдается этамбутолу. Стрептомицин используется не более 2 месяцев;
2) поддерживающая фаза проводится в течение четырех месяцев в ежедневном режиме (6 дней в неделю) двумя препаратами – изониазидом (H) и рифампицином (R); при выявлении монорезистентности к изониазиду до начала лечения, поддерживающая фаза проводится с добавлением этамбутола; при тяжелых случаях заболевания поддерживающая фаза продлевается до семи месяцев.
Лечение больных II категории (повторных случаев):
1) интенсивная фаза проводится в сроки от трех до пяти месяцев, в зависимости от тяжести и распространенности туберкулезного процесса в ежедневном режиме 7 календарных дней в неделю. Если интенсивная фаза проводится в амбулаторных условиях – 6 календарных дней в неделю. Лечение проводится пятью противотуберкулезными препаратами в течение двух месяцев: изониазидом (H), рифампицином (R), пиразинамидом (Z), этамбутолом (E) и стрептомицином (S) в соответствующих весу дозировках. Затем лечение продолжается четырьмя противотуберкулезными препаратами: изониазидом (H), рифампицином (R), пиразинамидом (Z), этамбутолом (E);
2) поддерживающая фаза проводится в течение пяти месяцев в ежедневном режиме (6 дней в неделю) тремя противотуберкулезными препаратами – изониазидом (H), рифампицином (R) и этамбутолом (Е).
Рекомендованные схемы АРТ первого ряда у больных ТБ включают препараты группы НИОТ — ламивудин (3TC) или эмтрицитабин (FTC) и тенофовир (TDF) в сочетании с эфавирензем (EFV) из группы ННИОТ, поскольку в этом случае взаимодействие с противотуберкулезными препаратами минимально.
| Схема лечения | Комментарии |
| Рекомендованные схемы АРТ у ЛЖВ с туберкулезом, получающих рифампицин | |
| 3TC (FTC) + TDF + EFV | Два НИОТ + EFV являются предпочтительной схемой стандартной АРТ первой линии у людей, получающих противотуберкулезное лечение с использованием рифампицина |
| 3TC + ZDV + ABC 3TC (FTC) + ZDV + TDF | Три НИОТ являются альтернативной схемой стандартной АРТ первой линии у людей, получающих противотуберкулезное лечение с использованием рифампицина, которые не могут принимать EFV. Эта схема менее эффективна по сравнению с предпочтительной схемой АРТ первой линии |
| 3TC (FTC) + TDF + DTG 3TC (FTC) + ABC + DTG | С рифампицином рекомендуется назначать DTG в дозе 50 мг 2 раза в сутки. |
Перечень основных лекарственных средств (имеющих 100% вероятность применения):
Противотуберкулезные препараты
| Лекарственная группа | Международное непатентованное наименование ЛС | Вес (кг) | Уровень доказательности | |||||
| 33-49 кг | 50-70 кг | >70 кг | ||||||
| Интенсивная фаза – ежедневный прием | ||||||||
| Пероральные противотуберкулезные препараты первого ряда | Изониазид (H) | 10-15 мг/кг | 200-300 | 300 | 400 | А | ||
| Рифампицин (R) | 300 | 450 | 600 | 750 | А | |||
| Пиразинамид (Z) | 30-40 мг/кг | 1000-1500 | 1500-2000 | 2000 | А | |||
| Этамбутол (E) | 25 мг/кг | 800 -1200 | 1200-1600 | 1600-2000 | А | |||
| Инъекционные препараты | Канамицин (Km) (1 г) | 15-20 мг/кг | 500-750 | 1000 | 1000 | А | ||
| Капреомицин (Cm) (1 г) | 15-20 мг/кг | 500-750 | 1000 | 1000 | А | |||
| Амикацин (Am) (1 г) | 15-20 мг/кг | 500-750 | 1000 | 1000 | А | |||
| Препараты из группы фторхинолонов | Офлоксацин (Ofx) | 800 | 800 | 800 | 800-1000 | С | ||
| Левофлоксацин (Lfx) | 500 | 500 | 750-1000 | 1000 | С | |||
| Моксифлоксацин (Mfx) | 400 | 400 | 400 | 400 | С | |||
| Другие противотуберкулезные препараты второго ряда | Этионамид (Eto) | 15-20 мг/кг | 500 | 750 | 1000 | А | ||
| Протионамид (Pto) | 15-20 мг/кг | 500 | 750 | 1000 | А | |||
| Циклосерин (Cs) | 15-20 мг/кг | 500 | 750 | 1000 | А | |||
| Парааминосалициловая кислота (PAS) | 1500 мг/кг | 8000 | 8000 | 8000 | А | |||
| 5 группа | Линезолид (Lzd) | — | 600 | 600 | 600 | А | ||
| Клофазимин (Cfz) * | — | 200* | 200* | 200* | А | |||
| Бедаквилин (Bdq)** | — | 400** | 400** | 400** | А | |||
| Деламанид (Dlm) | — | 200 | 200 | 200 | А | |||
| Амоксициллин-клавуланат (Amx-Clv)*** | При весе до 50 кг – из расчета дозы амоксициллина 35 мг на 1кг массы тела; при весе 50 кг и выше – 2000 мг амоксициллина | |||||||
| Поддерживающая фаза – ежедневный прием | ||||||||
| Пероральные противотуберкулезные препараты первого ряда | Изониазид (H) | 10-15 мг/кг | 300 | 300 | 400 | А | ||
| Рифампицин (R) | 300 | 450 | 600 | 750 | А | |||
| Этамбутол (E) | 25 мг/кг | 800 | 1200 | 1600 | А | |||
| Пиразинамид (Z) | 30-40 мг/кг | 1000-1500 | 1500-2000 | 2000 | А | |||
| Препараты из группы фторхинолонов | Офлоксацин (Ofx) | 600 | 600 | 800 | 800-1000 | С | ||
| Левофлоксацин (Lfx) | 500 | 500 | 750-1000 | 1000 | С | |||
| Моксифлоксацин (Mfx) | 400 | 400 | 400 | 400 | С | |||
| Другие противотуберкулезные препараты второго ряда | Этионамид (Eto) | 15-20 мг/кг | 500 | 750 | 1000 | А | ||
| Протионамид (Pto) | 15-20 мг/кг | 500 | 750 | 1000 | А | |||
| Циклосерин (Cs) | 15-20 мг/кг | 500 | 750 | 1000 | А | |||
| Парааминосалициловая кислота (Pas) | 1500 мг/кг | 8000 | 8000 | 8000 | А | |||
| 5 группа | Линезолид (Lzd) | — | 600 | 600 | 600 | А | ||
| Клофазимин (Cfz)* | — | 100* | 100* | 100* | А | |||
| Бедаквилин (Bdq)** | — | 200** | 200** | 200** | А | |||
| Деламанид (Dlm) | — | 200 | 200 | 200 | А | |||
| Амоксициллин-клавуланат (Amx-Clv)*** | При весе до 50 кг – 1500 мг амоксициллина; При весе 50 кг и выше – 2000 мг амоксициллина | А | ||||||
* Клофазимин назначается в дозе 200 мг ежедневно в течение первых двух месяцев лечения, в последующем в дозе 100 мг ежедневно до окончания лечения.
** Бедаквилин назначается в дозе 400 мг ежедневно в течение первых 14 дней лечения, в последующем в дозе 200 мг три раза в неделю до окончания лечения.
*** Амоксициллин-клавуланат назначается только совместно с Имипенемом-циластатином за 40 минут до его внутривенно-инфузионного введения.
| Лекарственная группа | Международное непатентованное наименование ЛС | Способ применения | Уровень доказательности |
| Нуклеозидные ингибиторы обратной транскриптазы (НИОТ) | Абакавир (ABC) |
Зидовудин (AZT)
Ламивудин (3TC)
| Лекарственная группа | Международное непатентованное наименование ЛС | Способ применения | Уровень доказательности |
| Сульфаметоксазол и Триметоприм | 160 + 800 мг в сутки | А |
Лечение устойчивых форм ТБ и ВИЧ
Всем ЛЖВ, больным МЛУ-ТБ, АРТ необходимо начинать как можно раньше (в течение первых двух недель), независимо от числа лимфоцитов CD4.
Использование краткосрочного режима лечения (КРЛ) длительностью 9-12 месяцев для пациентов с РУ-ТБ/МЛУ-ТБ, включая ЛЖВ, которые соответствуют критериям отбора. (см. Рис.1) Для пациентов, которые не подходят по критериям рекомендуется индивидуальный режим лечения (ИРЛ) с интенсивной фазой в течение 8 месяцев (может быть продлена в зависимости от ответа на лечение) включающей как минимум 5 эффективный ПТП, включая пиразинамид и четыре ключевых препарата второго ряда (см. Рис 2). Продолжительность поддерживающей фазы должна быть как минимум 12 месяцев. Рекомендуется использование новых препаратов, таких как Бедаквилин (Bdq) и Деламанид (Dlm) в течение 6 месяцев, но может быть продлено, если остается менее чем 3 эффективных ПТП, и если переносимость лечения хорошая.
- Не подтверждена устойчивость к ФХ и ИПВР (если ТЛЧ уже доступны)
- Отсутствует контакт с пациентами с устойчивостью к ФХ и/или ИПВР
- Пациент не принимал ПВР ≥ 1 месяц
- Нет непереносимости ПТП, включенных в схему КРЛ
- Отсутствует беременность
- Отсутствует распространенные и осложненные формы ВЛ-ТБ (за исключением лёгких форм)
- Отсутствие факторов риска для безуспешного лечения (распространенные и осложненные формы ТБ, сопутствующие заболевания в фазе декомпенсации, отсутствие минимум одного препарата КРЛ).
- Интенсивная фаза: 4-6 месяцев Cm/Am/Km,Mfx400-800мг,Cfz, Pto(Cs), Z, E, H(высокие дозы);
- Поддерживающая фаза: 5 месяцев Mfx, Cfz, Pto(Cs), Z, E.
- интенсивная фаза – 8-12 месяцев — (Cm/Km/Am+Lfx (Mfx)+Pto+Cs (PAS)+Z+E);
- поддерживающая фаза – 12 месяцев- (Lfx (Mfx)+Pto+Cs(PAS)+Z)
Пошаговый дизайн индивидуальных режимов лечения М/ШЛУ ТБ ([1])
- В случае, если подтверждена ЛУ ко всем ФХ, исключить ФХ из режимa
- В случае, если подтверждена ЛУ ко всем ФХ, исключить ФХ из режимa
Взаимодействие препаратов при лечении ВИЧ и ЛУ-ТБ
Тенофовир (TDF) обычно не назначают при использовании инъекционных препаратов второго ряда (ИПВР) из-за возможного наложения их нефротоксического действия, в случае если используется препарат, то необходимо проводить дополнительный мониторинг функции почек и электролитов.
Бедаквилин (Bdq) метаболизируется CYP3A4. Многие препараты могут либо индуцировать, либо ингибировать CYP3A4, что приводит к лекарственному взаимодействию. Взаимодействие с индукторами CYP3A4 может привести к потере эффективности Bdq (из-за низкой концентрация в крови из-за повышенного метаболизма препарата), и наоборот, взаимодействие с сильными и умеренными ингибиторами CYP3A4 может привести к повышенному содержания (более высокий уровень содержания в крови) Bdq.
Эфавиренз (EFV): одновременное применение с Bdq может привести к снижению содержания Bdq и уменьшению его эффективности, поскольку EFV является умеренным индуктором CYP3A, поэтому он не рекомендуется
Невирапин (NVP): одновременное применение с Bdq у ВИЧ-инфицированных пациентов не имеет клинически значимого эффекта, поэтому его можно использовать.
Лопинавир/ритонавир и другие ингибиторы протеазы (ИП): одновременное применение с Bdq приводит к увеличению концентрации Bdq в плазме, если пациент находится на АРВП второго ряда и нет доступа к ингибиторам интегразы (ИИ), могут использоваться ИП при условии более интенсивного мониторинга ЭКГ и функций печени.
Применение Бедаквилина с АРТ:
Пациенты, которые еще не на АРТ:
Инициировать режим на основе NVP:
• 2 НИОТ + невирапин [т.е., AZT-3TC (или FTC) -NVP]
• ННИОТ, НИОТ + невирапин [т.е., TDF-3TC- (или FTC) -NVP]
• Когда курс Bdq закончен, NVP заменить на EFV.
Пациенты, которые на АРТ:
• Если пациент уже находится на АРТ с EFV, оцените вирусную нагрузку:
• Если ВН не определяется, можно заменить EFV на NVP на весь период лечения с Bdq. Когда курс Bdq будет закончен, вернуться обратно на EFV.
• Если ВН определяется, пациент должен быть переведен на АРТ второго ряда, с использованием ИИ (долутегравир или ралтегравир). Если ИИ недоступны, можно рассматривать ИП (лопинавир/ритонавир) с осторожностью (чаще контролировать ЭКГ и функцию печени).
• Если пациент уже находится на АРТ второго ряда с ИП (лопинавир/ритонавир), оцените ВН:
• Если ВН не определяется, замените лопинавир/ритонавир на долутегравир или ралтегравир на весь период использования Bdq. Как только курс Bdq будет закончен, пациента можно перевести обратно на лопинавир/ритонавир. Если ИИ недоступны, продолжайте использовать лопинавир/ритонавир с осторожностью.
• Если ВН определяется, пациент должен быть переведен на схемы АРТ третьего ряда (с использованием ИИ, таких как долутегравира или ралтегравира).
Деламанид (Dlm) не имеет взаимодействия с АРТ и является предпочтительным для ЛЖВ, которым назначен индивидуальный режим лечения ЛУ-ТБ, содержащие новые препараты.
Исследования лекарственного взаимодействия Dlm и АРТ проводились на здоровых людях без ВИЧ, при этом деламанид (100 мг два раза в день) назначали с АРВП тенофовир (300 мг в день) или лопинавир/ритонавир (400/100 мг в день) или эфавиренц (600 мг в день). Одновременное применение Dlm с лопинавиром/ ритонавиром незначительно повышало содержание Dlm и метаболита деламанида (DM-6705), примерно на 25%. Dlm не оказывал воздействия на тенофовира, лопинавира или ритонавира. Одновременное применение с эфавирензем не влияло на концентрацию как деламанида, так и эфавиренза.
Тактика при побочных эффектах в процессе лечения
Во время первых 2–4 недель лечения больных с сочетанной инфекцией рекомендуется проводить полное клиническое обследование, по крайней мере, 1 раз в неделю. В конце первого месяца необходимо хотя бы один раз определить содержание глутаминовой пируват трансаминазы в сыворотке крови (СГПТ). Признаки гепатотоксичности могут наблюдаться у 13% людей с ТБ и ВИЧ (2,3). Гепатотоксичностью обладают три противотуберкулезных препарата, которые применяются в начальной фазе интенсивного лечения (рифампицин, изониазид и пиразинамид), некоторые лекарства против ВИЧ (ННИОТ) также проявляют гепатотоксичность. Если имеются признаки значительного повреждения печени (уровни СГПТ в пять раз выше нормальных показателей этого теста), все противотуберкулезные и антиретровирусные препараты необходимо заменить менее токсичными, а также принять во внимание возможность взаимодействий между этими лекарствами. Если у пациента имеется тяжелая форма ТБ, и прекращение противотуберкулезного лечения может оказаться небезопасным, следует перейти на нетоксичную для печени схему лечения, включающую стрептомицин, этамбутол и фторхинолоновый препарат. Если лечение ТБ было прекращено, то до возобновления приема противотуберкулезных препаратов должны нормализоваться результаты печеночных тестов и исчезнуть клинические симптомы (тошнота и боли в животе). После разрешения лекарственного гепатита прием лекарств возобновляют по одному. Если после возобновления лечения ТБ симптомы гепатотоксичности возобновятся или снова станут ненормальными результаты функциональных проб печени, следует прекратить прием того препарата, который был добавлен последним. Рифампицин приводит к развитию гепатотоксичности гораздо в меньшей степени, чем изониазид или пиразинамид, и является самым эффективным препаратом, поэтому начинать применять этот препарат необходимо как можно позже.
Нередким побочным эффектом комбинированной противотуберкулезной и антиретровирусной терапии является также сыпь на коже. Рекомендуется, приступив к симптоматическому лечению антигистаминными препаратами и используя местно увлажняющие кремы, продолжить лечение ТБ, тщательно наблюдая за больным. Однако если будет замечено ухудшение со стороны кожных покровов, необходимо прекратить прием всех противотуберкулезных и антиретровирусных препаратов. После исчезновения кожной сыпи можно будет возобновить прием противотуберкулезных лекарств, добавляя их по одному, а затем и антиретровирусных препаратов.
Возможные перекрестная и дополнительная токсичность при лечении ЛУ-ТБ и ВИЧ
| Токсические проявления | ПТП | АРВП | Комментарии |
| Желудочно-кишечные (тошнота, рвота, диарея). | Eto/Pto, PAS, Cfz, H, Z, Bdq, Dlm и другие | ННИОТ-NVP, ИП-RTV, НИОТ-AZT, ddI и d4T | В случае появления диареи необходимо исключить оппортунистические инфекции как вероятную причину. Постоянная рвота может быть вызвана другими причинами (например, гепатитом, лактоацидозом, менингитом, беременностью и т. д.). |
| Боль в животе | Eto/Pto, PAS, Cfz, Lzd | Все АРВП | Боль в животе может быть ранним симптомом тяжелой лекарственной реакции, таких как гепатит, панкреатит или лактоацидоз. |
| Дерматиты (кожная сыпь) | H, R, E, Z, ФХ, Eto/Pto, Cfz | ННИОТ: NVP и EFV; НИОТ: ABC | Не назначайте повторно ABC, т.к. это может привести к угрожающей жизни анафилаксии. Не назначайте повторно с любым препаратом, который может вызвать синдром Стивенса Джонсона. Сульфаметоксазолом+Триметоприм также может вызывать кожную сыпь. |
| Токсическое поражение ЦНС и/или психиатрические симптомы (депрессия, психоз) | Cs, Hh, ФХ, Eto/Pto, Imipenem (Imp)/ Meropenem (Mpn) | Efavirenz (EFV) | Токсическое поражение ЦНС от EFV часто устраняется самостоятельно после первых 2-4 недель лечения. Исключите другие причины. |
| Головная боль | Cs, Bdq | AZT, EFV | Исключите более серьезные причины головной боли, такие как менингит, токсоплазмоз и т. д. |
| Периферическая нейропатия | H, Lzd, (менее часто: ФХ, ИПВР, Cs, Eto/Pto, E) | d4T, ddI | Пациент, получающий Hвд, Cs и / или Lzd, должен получать профилактику пиридоксином (B6). Избегайте использования d4t и ddi с Cs и Lzd. Если периферическая нейропатия обусловлена Lzd и степень ≥ 2 остановить Lzd и не назначать повторно |
| Поражение почек вызванное гипокалиемией | ИПВР (Am, Km, Cm) | TDF | Избегайте одновременное использования TDF и ИПВР, если это возможно. Даже без одновременного использования TDF у ЛЖВ высокий риск токсического поражения почек, вторично к ИПВР. Рекомендуется частый мониторинг уровня креатинина и электролитов. Необходимо откорректировать дозы препаратов, если клиренс |
| Гематологические (Токсические поражения костного мозга) | Lzd | Zidovudine (AZT) | Мониторинг развернутого анализа крови ежемесячно при использовании Lzd. Все пациенты с Lzd должны получать пиридоксин (ВитB6) 100 мг в день. Рассмотрите другие причины как Сульфаметоксазолом+ Триметоприм, ВИЧ инфекция, оппортунистические инфекции. |
| Гепатотоксичность | Z, Hh, Eto/Pto, PAS, Bdq | NVP, EFV, все НИОТ и все ИП | Когда AлT/AсT возрастают > 5 раз необходимо остановить АРВП и ПТП и сначала возобновляют лечение ТБ (см. Главу об управлении нежелательными явлениями). Необходимо исключить другие причины, такие как вирусный гепатит A, B, C и ЦМВ. |
| Панкреатит | Lzd | d4T, ddI | Избегайте совместное использования этих препаратов. Если препарат вызвал панкреатит, прекратите его прием. Рассмотрите другие причины, такие как желчные камни или чрезмерное употребление алкоголя. |
| Лактоацидоз | Lzd | d4T, ddI, AZT | Если препарат вызвал высокий уровень лактата в крови или лактоацидоз, отмените его и замените. |
| Неврит зрительного нерва | E, Lzd | ddI | Отмените препарат, который вызвал неврит зрительного нерва, и замените его. |
| Гипотериоз | Eto/Pto, PAS | d4T | Мониторинг уровня тиреотропного гормона (TТГ) и замените его левотироксином (TТГ> 10 мМЕ / л) при необходимости |
| Дисгликемия | Gfx, Eto/Pto | ИП | Eto/Pto может затруднить контроль глюкозы у пациентов с диабетом. ИП могут вызывать инсулиновую резистентность и гипергликемию. |
| Артралгия | Z (менее часто ФХ и Bdq) | ИП | Артралгия очень распространена при приеме Z, также ФХ, Bdq и ИП. |
| Удлиненный интервал QT | Bdq, Dlm, Mxf, Gfx, Cfz (менее часто с Lfx) | АРТ приводило к удлиненному интервалу QT | Неизвестны данные о дополнительном эффекте комбинации АРТ и ПВР на удлинение интервала QTc. Если QTc удлиняется > 500 мс отмените препараты, удлиняющие интервал QT, но не прекращайте АРТ. |
Особые обстоятельства
Почечная недостаточность
Изониазид, рифампицин и этионамид/протионамид либо почти полностью выводятся с желчью, либо метаболизируются в нетоксичные вещества; следовательно, эти лекарства больным с почечной недостаточностью можно давать в обычных дозировках. У больных с тяжелой почечной недостаточностью, при клиренсе креатинина больше 30 мл/мин или находящихся на гемодиализе, изониазид может провоцировать периферическую нейропатию, развитие которой можно предупредить, назначая больным пиридоксин.
Этамбутол, пиразинамид, циклосерин, парентеральные препараты и фторхинолоны выводятся почками, поэтому больные должны их принимать в уменьшенных дозах или с увеличенными интервалами и при тщательном мониторинге функции почек с помощью ежемесячных проверок уровня креатинина.
Лекарственные формы парааминосалициловой кислоты, не содержащие соли натрия, могут быть использованы без опасения возможной задержки натрия в организме.
Следует избегать применения таких антиретровирусных препаратов, как тенофовир, в связи с их известной нефтотоксичностью.
Формула для оценки клиренса креатинина (CrCI):
Расчетный клиренс =(140 – Возраст) x Вес (кг) x константа
Креатинин сыворотки (ммоль/л)
Константа = 1.23 для мужчин, 1.04 для женщин
Если креатинин указывается в обычных единицах (мг/дл) его можно преобразовать в (ммоль/л) путем умножения на 88,4 (например, креатинин = 1,2 мг/дл эквивалентен: 1,2 х 88,4 = 106,1 мкмоль/л). Нормальные показатели для мужчин от 97 до 137 мл/мин и от 88 до 128 мл/мин для женщин.
Частоту и дозировку ПТП следует регулировать, если клиренс креатинина составляет Некоторые АРВ-препараты следует корректировать, если клиренс креатинина составляет
Корректировка доз для АРТ при почечной недостаточности
| Препараты | СКФ 10 -50 мл/мин | СКФ < 10 мл/мин |
| Abacavir (ABC) Zidovudine (AZT) Lamivudine (3TC) Emtricitabine (FTC) Tenofovir (TDF) | Не требуется Не требуется 150 мг 1 раз в день Не требуется Не назначать | Не требуется 300 мг 1 раз в день 50 мг 1 раз в день Не требуется Не назначать |
| Efavirenz (EFV) Nevirapine (NVP) Etravirine (ETV) Rilpivirine (RPV) | Не требуется Не требуется Не требуется Не требуется | Не требуется Не требуется Не требуется Используйте с осторожностью |
| Dolutegravir (DTG) Raltegravir (RAL) | Не требуется Не требуется | Не требуется Не требуется |
| Lopinavir/ritonavir (LPV/r) Darunavir/ritonavir или cobicistat (DRV/r или k) Atazanavir/ritonavir (ATV/r) | Не требуется Не требуется Не требуется Не требуется | Не требуется Не требуется Не требуется Не требуется |
| Препараты | Рекомендуемая доза и частота для пациентов с клиренсом креатинина |
| Isoniazid | Не требуется |
| Rifampicin | Не требуется |
| Pyrazinamid | 25-35 мг/кг в день, 3 раза в неделю |
| Ethambutol | 12-25 мг/кг в день, 3 раза в неделю |
| ИПВРᵃ | 12-15 г/кг в день, 2 или 3 раза в неделю (не ежедневно) |
| Levofloxacin | 750-1000 мг в день, 3 раза в неделю |
| Moxifloxacin | Не требуется |
| Cyclocerine б | 250 мг 1 раз в день, или 500 мг в день, 3 раза в неделю |
| Pro/Ethionamide | Не требуется |
| Para-aminosalicylic acid в | Не требуется |
| Bedaquiline | Коррекция дозы не требуется у пациентов с легкой или умеренной почечной недостаточностью |
| Delamanid | Коррекция дозы не требуется у пациентов с легкой или умеренной почечной недостаточностью |
| Linezolid | Не требуется |
| Clofazimine | Не требуется |
| Amoxicillin/ clavulanate | При клиренсе креатинина 10-30 мл/мин доза 1000 мг 2 раза в день; при клиренсе креатинина |
| Imipenem/ Cilastatin | При клиренсе креатинина 20-40 мл/мин доза 500 мг каждые 8 часов; при клиренсе креатинина |
| Meropenem | При клиренсе креатинина 20-40 мл/мин доза 750 мг каждые 12 часов; при клиренсе креатинина |
а. Использовать инъекционные препараты с осторожностью у пациентов с нарушенной функцией почек из-за повышенного риска нефротоксичности и ототоксичности. Контролировать креатинин и клиренс креатинина 1 раз в неделю, подумать о том, чтобы прекратить прием инъекционных ПТП в случае ухудшения показателей.
б. Для циклосерина целесообразность назначения доз 250 мг в день не была полностью установлена. Должен быть обеспечен тщательный контроль за симптомами нейротоксичности.
в. PASна основе натриевой соли может приводить к повышению уровня натрия, поэтому следует избегать его использование у пациентов с почечной недостаточностью. В этом случае предпочтительнее PAS не на основе натриевой соли без риска задержки натрия и является предпочтительным для пациентов с почечной недостаточностью.
Поражения печени
Пиразинамид, изониазид и рифампицин или рифабутин могут провоцировать воспалительные процессы в печени. Наибольшей гепатотоксичностью обладает пиразинамид, далее следует изониазид. Рифампицин редко вызывает повреждения клеток печени, хотя его прием может сопровождаться развитием холестаза и желтухи. Из числа противотуберкулезных препаратов второго ряда гепатотоксичностью обладают также этионамид/протионамид и PAS, хотя в меньшей степени, чем любой из препаратов первого ряда. Гепатит редко возникает при лечении фторхинолонами.
Люди, являющиеся носителями вирусов гепатитов или перенесшие острый вирусный гепатит в прошлом, а также употребляющие алкоголь в больших количествах, могут получать противотуберкулезную терапию по обычной схеме. Однако у них при приеме противотуберкулезных препаратов могут чаще наблюдаться гепатотоксические реакции, что это можно было бы ожидать. У людей с нестабильным состоянием печени или с выраженными ее поражениями необходимо, по возможности, проверить функцию печени до начала лечения. Если уровень аланин аминотрансферазы до начала лечения превышает нормальные показатели более чем в три раза, больные могут получать специфическую терапию по схеме без пиразинамида: однако в таких случаях рекомендуется проводить лечение рифампицином, изониазидом и этамбутолом в течение 9 месяцев (только фаза интенсивного лечения). Рекомендован тщательный контроль содержания печеночных ферментов.
Беременные женщины
Использовать те же антиретровирусные препараты первого ряда, что и у небеременных женщин. При отсутствии устойчивости возбудителей ТБ используйте стандартное противотуберкулезное лечение препаратами первого ряда (4).
В случаях устойчивого ТБ — избегайте применения парентеральных противотуберкулезных препаратов, которые обладают высокой токсичностью в отношении развивающегося органа слуха у плода. Прием капреомицина также может сопровождаться риском ототоксичности, однако это лекарство является парентеральным препаратом выбора в случаях, когда нельзя обойтись без инъекционных препаратов.
Избегайте применения этионамида/протионамида, которые могут увеличивать риск возникновения тошноты и рвоты, связанных с беременностью, а также проявлять тератогенное действие.
Лечение ЛУ-ТБ во время грудного вскармливания
Большинство ПВР обнаруживаются в грудном молоке, концентрация обнаруженных препаратов очень низкая и, следовательно, риск минимальный
Исключение составляют Cfz и Bdq, поскольку оба препарата накапливаются в жировой ткани молочной железы и выводятся из организма с грудным молоком. Не следует назначать Cfz беременным женщинам, поскольку наблюдается пигментация кожи у младенцев, но может быть использован, если польза превышает риск.
Лица употребляющие инъекционные наркотики
Взаимодействие наркотиков и заместительной терапии опиоидами с противотуберкулезными и антиретровирусными препаратами приводит к усилению гепатотоксичности. Это требует более осторожного выбора самих противотуберкулезных и антиретровирусных препаратов и их дозировок, а также более тщательного мониторинга функций печени.
У лиц с алкогольной и другими зависимостями циклосерин очень часто вызывает развитие побочных эффектов, включая судороги, поэтому данный препарат не следует включать в схемы лечения МЛУ-ТБ у ЛУИН.
Рифампицин в значительной мере снижает концентрацию и эффективность метадона: доза метадона должна быть скорректирована (увеличена) для поддержания заместительного эффекта. В качестве альтернативы рифампицин можно заменить рифабутином, так как не имеется данных о возможных лекарственных взаимодействиях рифабутина и метадона.
Могут наблюдаться нередкие взаимодействия между антиретровирусными препаратами и метадоном, так как последний оказывает сходное с опиоидами действие на опорожнение желудка и на метаболизм изоферментов 2B6, 3A4 и 2D6 системы цитохрома P450. Это может снижать эффективность одного или обоих видов лечения, вызывая синдром отмены или передозировки, увеличивая токсичность метадона и (или) уменьшая эффективность антиретровирусных препаратов. Эфавиренз, невирапин и лопиновир, усиленный ритонавиром, вызывали существенное снижение уровней метадона. Клинический эффект обычно появляется после семи дней совместного приема этих препаратов и может быть усилен за счет увеличения дозы метадона, обычно на 5-10 мг в день до тех пор, пока не будет достигнут желательный эффект. Профиль лекарственного взаимодействия бупренорфина имеет более благоприятный характер по сравнению с метадоном.
Налтрексон не метаболизируется посредством ферментной системы цитохрома P450, поэтому не следует ожидать его взаимодействия с ИП или с ННИОТ.
Частые коинфекции с вирусным гепатитом C и (или) гепатитом B и взаимодействия с лекарствами, применяемыми для их лечения, требуют специальных подходов. Наличие вирусного гепатита не является противопоказанием для лечения ТБ или ВИЧ-инфекции, но требует более тщательного мониторинга функций печени. Схема лечения сочетанной ВИЧ-инфекции и гепатита В должна включать антиретровирусные препараты тенофовир и эмтрицитабин (или ламивудин). Обычно лечение вирусного гепатита С пегилированным интерфероном и рибавирином должно быть отложено до окончания лечения ТБ, однако при наличии выраженного фиброза или цирроза печени решение о начале лечения должно приниматься индивидуально у каждого больного.
Вирусные гепатиты В и С
Проводить скрининг всех пациентов с ТБ/ВИЧ на гепатиты B и C
Хронический гепатит B
• Использовать схему АРТ с TDF/FTC/EFV в качестве предпочтительной.
• Мониторинг ДНК ВГB каждые 3 — 6 месяцев
• Не прекращать TDF/FTC при переходе на схемы АРТ второго ряда
Хронический гепатит C
Следует избегать одновременного лечения инфекции ВГС и чувствительного ТБ из-за взаимодействия путей метаболизма в печени при использовании рифампицина.
Сначала лечить активный ТБ и внимательно следить за функцией печени.
Очень сложно проводить лечение ВГС, ВИЧ и ЛУ-ТБ одновременно, множественное лекарственное взаимодействие между препаратами и очень мало данных, необходимых для клинического решения по каждому случаю для того, чтобы уменьшить риск дополнительного нежелательного эффекта, лекарственной нагрузки и лекарственного взаимодействия.
Риск реактивации ТБ, если человек, особенно ВИЧ-инфицированный, получает терапию на основе интерферона, так как эта терапия может повысить заболеваемость активным ТБ.
- Клинического ухудшения течения ТБ
- Временной связи с началом АРТ
- Исключения альтернативного диагноза (ЛУ-ТБ) и других ВИЧ-ассоциированных инфекций
- Исключения нежелательных явлений, связанных с лекарствами
- Исключения проблем приверженности, неудачи лечения
Дети
Диагностика (5)
| Рекомендуемый подход к диагностике ТБ у детей | Влияние ВИЧ инфекции | |
| Тщательный анамнез, включая анамнез контактов с ТБ | Особенно важно из-за низкой чувствительности кожного туберкулинового теста для выявления инфекции ТБ | |
| Тщательный анамнез симптомов ТБ | Низкая специфичность: наслоение клинических симптомов ТБ и ВИЧ инфекции | |
| Клинический осмотр, включая оценку роста | Низкая специфичность: недостаточное питание общее для ТБ и ВИЧ | |
| Туберкулиновый кожный тест | Низкая специфичность: позитивность кожного туберкулинового теста снижается с увеличением иммуносупрессии | |
| Бактериологическое подтверждение по возможности | Важно независимо от ВИЧ статуса | |
| Исследования, имеющие отношение при подозрении на легочной и внелегочной туберкулез | Широкий спектр диагностических возможностей из-за ВИЧ связанных заболеваний | |
| Рентгенологические данные грудной клетки | Низкая специфичность: наслоение ВИЧ связанного легочного заболевания | |
Методу Xpert MTB/RIF следует отдать предпочтение перед стандартной микроскопией и культуральным исследованием как первоначальному диагностическому тесту у детей с подозрением на наличии МЛУ-ТБ или ВИЧ-ассоциированного туберкулеза (сильная рекомендация, очень низкое качество доказательств).
Интерферон-гамма-анализ (IGRA) не заменит туберкулиновый кожный тест (TST) для диагностики скрытой туберкулезной инфекции у детей или для диагностической работы с детьми (независимо от ВИЧ-статуса) с подозрением на туберкулез (сильная рекомендация, низкое качество доказательств).
Рутинное тестирование на ВИЧ должно предлагаться всем пациентам, включая детей, с предполагаемым и диагностированным туберкулезом (сильная рекомендация, низкое качество доказательств).
Лечение
Дозировки противотуберкулезных препаратов у детей:
изониазид (H) 10 мг/кг (диапазон 7-15 мг/кг);
максимальная доза 300 мг/день рифампицина (R) 15 мг/кг (диапазон 10-20 мг / кг);
максимальная доза 600 мг/день пиразинамида (Z) 35 мг/кг (диапазон 30-40 мг/кг)
этамбутола (E) 20 мг/кг (диапазон 15-25 мг/кг) (сильная рекомендация, умеренное качество доказательств)
Дети с подозрением на туберкулез или туберкулезный периферический лимфаденит, живущие в условиях высокой распространенности ВИЧ (или с подтвержденной ВИЧ-инфекцией), не должны лечиться с прерывистыми режимами (то есть с двухнедельной или трехнедельной дозой).
Дети, живущие с ВИЧ, которые старше 12 месяцев и при скрининге нет симптомов туберкулеза, а также не имеют контакта с больными туберкулезом:
— следует предлагать 6 месяцев профилактического лечения изониазидом (10 мг/кг в день, диапазон 7-15 мг/кг, максимальная доза 300 мг/сут).
Все дети, живущие с ВИЧ, которые успешно прошли лечение от туберкулеза, должны получать изониазид еще 6 месяцев (6).
Антиретровирусная терапия
Схемы, содержащие цепь нетимидинового нуклеозидного ингибитора обратной транскриптазы (NRTI) (тенофовир дизопроксилфумарат (TDF) или абакавир (ABC) + ламивудин (3TC)) и один ненуклеозидный ингибитор обратной транскриптазы (NNRTI) эфавиренц (EFV) как предпочтительный выбор у подростков и детей старше 3 лет (7)
Для детей в возрасте до 3 лет предпочтительной схемой является ингибитор протеазы (PI) в сочетании с ABC или зидовудином (AZT) (7).
Рекомендуемой схемы АРТ для детей, нуждающихся в лечении ТБ
| Рекомендованные схемы для детей и младенцев, которые во время лечения c ТБ b начали АРТ | ||
| Младше 3 лет | 2 НИОТ + NVP доза составила 200 mg/m 2 или три НИОТ (AZT + 3TC + ABC) d | |
| 3 года и старше | 2 НИОТ + EFV или три НИОТ (AZT + 3TC + ABC) d | |
| Рекомендованные схемы для детей и младенцев, которые во время АРТ начали противотуберкулезное лечение | ||
| Ребенок на основе стандартной схемы ННИОТ (2 НИОТ + EFV или NVP) | Младше 3 лет | Продолжать NVP, чтобы доза составляла 200 mg/m2 или три НИОТ (AZT + 3TC + ABC) d |
| 3 года и старше | Если на EFV, продолжать ту же схему, If on если на NVP, менять на EFV или три НИОТ (AZT + 3TC + ABC) d | |
| Ребенок на основе схемы с ИП (2 НИОТ+ LPV/r) | Младше 3 лет | Три НИОТ (AZT + 3TC + ABC)d или поменять на NVP чтобы доза составляла 200 mg/m2 или продолжить LPV/r и рассмотреть вопрос о добавлении RTV для достижения полной терапевтической дозы e |
| 3 года и старше | Если были неудачи в лечении на схеме с ННИОТ: поменять на EFV или три НИОТ (AZT + 3TC+ ABC)d или продолжить на LPV/r и рассмотреть вопрос о добавлении RTV для достижения полной терапевтической дозы e. Рассмотрите возможность консультаций с экспертами для разработки схемы второй линии . | |
b Обеспечьте оптимизированное дозирование рифампицина на основе новых рекомендаций (глава 4)
c Переключиться на АРВ-терапию, соответствующую возрасту, на основе национального АРТ первой линии при прекращении лечения ТБ.
d Три НИОТ рекомендуется только на время лечения ТБ; соответствующий возрастному режиму на основе ИП или ННИОТ следует возобновить при прекращении терапии рифампицином. Основываясь на результатах исследования ARROW (15), этот режим следует рассматривать как предпочтительный вариант для детей в возрасте до 3 лет в режиме LPV / r при начале лечения туберкулеза. Его также следует рассматривать как предпочтительный режим для детей старше 3 лет с историей неудачи с ННИОТ.
e Увеличьте RTV до той же дозы, что и LPV в мг, в соотношении 1: 1.
f Переход на EFV следует рассматривать как предпочтительный вариант (16), и EFV можно сохранить после прекращения лечения ТБ, чтобы упростить и согласовать режим АРВ-препаратов, используемых у детей старшего возраста.
Профилактика
ВИЧ-инфицированным детям вакцину БЦЖ не следует проводить.
У младенцев с неизвестным ВИЧ-статусом и которые рождаются у ВИЧ-позитивных матерей и отсутствуют симптомы, указывающие на ВИЧ, вакцина БЦЖ следует назначать после изучения местных факторов.
Профилактическое лечение туберкулеза
Дети, живущие с ВИЧ, которые старше 12 месяцев и которые вряд ли заболеют туберкулезом, при скрининге на основе симптомов и не имеют контакта с заболеванием ТБ:
• следует предлагать 6 месяцев ПТИ (10 мг / кг в день, диапазон 7-15 мг / кг, максимальная доза 300 мг / день) в рамках комплексного пакета услуг по профилактике и уходу в связи с ВИЧ, если они живут в условиях с высокой распространенностью ТБ.

Скрининг
Рекомендуемый ВОЗ алгоритм скрининга ТБ и профилактическая терапия изониазидом (ПТИ) у детей старше 12 месяцев и живущих с ВИЧ (8)
a Все дети и младенцы младше одного года должны пройти ПТИ, если у них был контакт с инфекционным заболеванием.
b Плохая прибавка в весе определяется как потеря веса, очень низкий вес (вес по возрасту менее -3 -баллов), недостаточный вес (вес по возрасту менее -2г-баллов), подтвержденная потеря веса (> 5 %) с момента последнего посещения.
c Противопоказания включают: активный гепатит (острый или хронический) и симптомы периферической нейропатии. Туберкулез в прошлом не должен быть противопоказанием для начала ПТИ. Хотя это не требует начала ПТИ, туберкулиновый кожный тест может выполняться как часть необходимой диагностики в некоторых случаях.
d обследования в отношении ТБ должны проводиться в соответствии с существующими национальными протоколами.
Хирургическое вмешательство: нет.
- Диспансерное наблюдение пациентов, получающих АРТ и ПТП осуществляется совместно ПМСП, территориальным центром СПИД и противотуберкулезным учреждением с кратностью посещений не менее 1 раза в 3-6 месяцев;
для оценки результатов АРТ используются показатели — ВН и число лимфоцитов CD4; - вирусная нагрузка определяется перед началом АРТ. В дальнейшем следует измерять ВН первый раз не позднее 3 месяцев, затем 1 раз в 6 месяцев, при достижении неопределяемого уровня ВН;
- в случае отсутствия снижения ВН через 6 месяцев от начала лечения на 1 lоg10 или последовательного двукратного повышения ВН после исходной супрессии, следует провести генотипический тест на определение резистентности ВИЧ к антиретровирусным препаратам;
- число лимфоцитов CD4 нужно измерять через 3 месяца, затем каждые 6 месяцев, при необходимости чаще в течение 1-го года АРТ, далее не реже 1 раз в год (за исключением случаев неэффективности лечения);
- лабораторные исследования необходимо проводить не менее одного раза в 6 месяцев;
- тестирование на носительство аллеля HLA-B*5701 перед назначением схем АРТ, содержащих Абакавир.
| Сроки | |||||
| Перед началом лечения | 2 нед | 4 нед | 12 нед | 24 нед | 48 нед |
| Вирусная нагрузка | X | х | x | x | |
| Число лимфоцитов CD4 | X | х | x | x | |
| Общий анализ крови | X | x | x | x | x |
| Биохимические показатели функции печени b | X | x | |||
х — лабораторное исследование показано независимо от используемых АРВ-препаратов;
x (АРВ-препарат) -исследование показано пациентам, которые получают указанный в скобках препарат.
b Пациентам с хроническими гепатитами биохимические показатели определяют согласно клиническому протоколу диагностики и лечения хронического вирусного гепатита В и С у взрослых в РК.
- консультирование равными консультантами;
- текстовые сообщения на мобильный телефон;
- применение таблетниц;
- когнитивно-поведенческая терапия;
- тренинг поведенческих навыков по повышению приверженности;
- комбинации фиксированных доз и схемы приема препаратов один раз в день.
- мониторинг ВН;
- учет отпуска лекарственных средств;
- самоотчеты;
- подсчет количества таблеток.
- профилактика Сульфаметоксазолом+Триметопримом назначается всем пациентам с активной формой ТБ, независимо от уровня CD4 клеток. Профилактика может быть прекращена у клинически стабильных пациентов (получают АРТ в течение не менее одного года без каких-либо новых явлений, соответствующих клинической стадии 2, 3 или 4) с признаками восстановления иммунитета (CD4>200кл/мкл) и/или вирусной супрессии на фоне АРТ.
- туберкулеза (при исключении у пациента активного туберкулеза) –однократно профилактическое лечение изониазидом (5 мг/кг), но не более 0,3 г в сутки + пиридоксин в дозе 25 мг/сут не менее 6 месяцев;
- инфекции, вызванной МАК — в случае CD4
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ:
смотрите амбулаторный уровень, клинические протоколы по диагностике и лечению туберкулеза.
Индикаторы эффективности лечения и безопасности методов диагностики и лечения, описанных в протоколе:
Критерии эффективности антиретровирусного лечения
| Вирусологические | Иммунологические | Клинические | |||
| Показатель | Вирусная нагрузка | Число CD4 | Клиническая стадия | Переносимость | |
| Сроки а | 24 недели | 48 недель и далее | 24-48 недель и далее | Через 12 недель после начала АРТ клинические проявления должны отсутствовать | Постоянная оценка |
| Цель b | неопределяемый уровень | Повышение от исходного уровня как минимум на 50 клеток/мкл | Стадия 1 или 2 | Через 3 месяца после начала приема АРВ-препарата клинически проявляющиеся побочные эффекты должны отсутствовать (а также субклинические, которые со временем могут проявиться клинически) | |
а Время оценки после начала АРТ указано приблизительно.
b Вирусная нагрузка уменьшается постепенно: у большинства пациентов (за исключением имеющих изначально высокую вирусную нагрузку) через 24 недели АРТ она должна быть
- исчезновение клинических и лабораторных признаков туберкулезного воспаления;
- стойкое прекращение бактериовыделения, подтвержденное микроскопическим и бактериологическим исследованиями;
- регрессия рентгенологических проявлений туберкулеза (очаговых, инфильтративных, деструктивных);
- восстановление функциональных возможностей и трудоспособности.
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ
Показания для плановой госпитализации: смотрите клинические протоколы по диагностике и лечению туберкулеза.
Показания для экстренной госпитализации: смотрите клинические протоколы по диагностике и лечению туберкулеза.
ВИЧ-инфекция — симптомы и лечение
Что такое вич-инфекция? Причины возникновения, диагностику и методы лечения разберем в статье доктора Куракиной Олеси Юрьевны, инфекциониста со стажем в 10 лет.
Над статьей доктора Куракиной Олеси Юрьевны работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
ВИЧ-инфекция — это хроническое инфекционное заболевание, которое провоцирует вирус иммунодефицита человека, поражающий клетки иммунной системы (СD4). При отсутствии лечения закономерно приводит к синдрому приобретённого иммунодефицита (СПИДа). [6]
Вирус иммунодефицита человека принадлежит семейству ретровирусов (Retroviridae), роду Lentivirus. Впервые информация о болезни появилась в 1970 годах. Сам вирус был выделен в 1983 году одновременно во Франции вирусологом Франсуазой Барре-Синусси и в США учёным Робертом Гало, однако название, одобренное Всемирной организацией здравоохранения, получил только через пять лет — в 1987 году. Тогда же впервые был зарегистрирован случай ВИЧ-инфекции в СССР. [1] [2]
В настоящее время выделяют два типа вируса — ВИЧ-1 и ВИЧ-2, которые отличаются по своим структурным характеристикам. На территории России, США, Европы и Центральной Африки распространён вирус первого типа (ВИЧ-1), на территории Индии и Западной Африки эпидемиологическое значение имеет второй тип вируса (ВИЧ-2).
В естественных условиях ВИЧ в высушенном состоянии сохраняет активность на протяжении нескольких часов, в биологических жидкостях — несколько дней, в замороженной сыворотке крови — несколько лет. При нагревании до 70-80°C вирус гибнет через 10 минут, при обработке 70% раствором этилового спирта инактивируется через одну минуту. Также чувствителен к 0,5% раствору гипохлорита натрия, 6% раствору перекиси водорода, 5% раствору лизола, эфира или ацетона. [2]
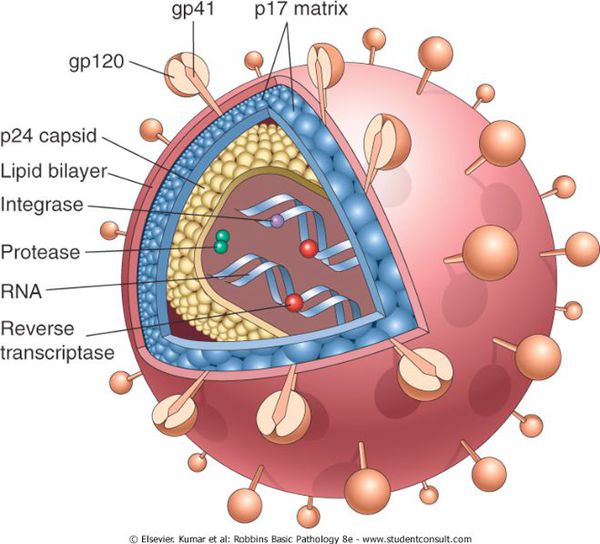
Форма вируса округлая, в центре расположено ядро, содержащее две нити рибонуклеиновой кислоты (РНК) и ферменты, необходимые для размножения — обратную транскриптазу (ревертазу), интегразу, протеазу, РНКазу. Ядро окружено внутренней белковой и наружной липидной оболочкой. Внутренняя оболочка ВИЧ-1 состоит из протеинов p17, p24 и p55. Наружная оболочка «пронизана» гликопротеином gp160, который состоит из фрагментов gp41 и gp120 (так называемых оболочечных белков). Gp41 и gp120 на поверхности вириона образуют отростки, с помощью которых ВИЧ присоединяется к рецепторам клеток-мишеней человека (клеткам организма, которые имеют рецептор — белок CD4). [1] [3]
Как передаётся ВИЧ
Пути передачи инфекции:
- Естественные:
- половой (гетеро- и гомосексуальные контакты);
- вертикальный (от заражённой матери к ребёнку во время беременности, родов или кормления грудью).
- Искусственный — парентеральный (в случае различных воздействий, связанных с нарушением слизистых оболочек и кожных покровов, например, использование нестерильных инструментов при употреблении наркотических веществ, медицинских и немедицинских манипуляциях).
Важно отметить, что при поцелуях, общении, объятиях, рукопожатиях, использовании общей посуды и других предметов быта ВИЧ-инфекция не передаётся.
ВИЧ в России
По данным на 30 июня 2021 года, в России выявлено 1 528 356 человек с подтверждённым диагнозом «ВИЧ-инфекция», в том числе: 1 122 879 пациентов, живущих с ВИЧ, и 405 477 умерших.
ВИЧ-инфекция активно распространяется среди населения. Так, в первом полугодии 2021 года 67,3 % людей заразились при гетеросексуальных контактах, 28,9 % — при употреблении наркотиков и 2,9 % — при гомосексуальных контактах. [7]
Вероятность заразиться ВИЧ
При незащищённом вагинальном контакте женщины заражаются ВИЧ примерно в 8 случаях из 10 000, а мужчины — в 4 случаях. При незащищённом анальном сексе риск заразиться ВИЧ выше: пассивному партнёру вирус передаётся в 138 случаях из 10 000, активному — в 11 случаях. [10]
ВИЧ и беременность
Женщины, которым своевременно назначена антиретровирусная терапия, не передают вирус при беременности и родах. При подавлении вируса роды могут быть проведены естественным путём. Однако грудное вскармливание даже при приёме терапии противопоказано в связи с большим риском заражения ребёнка через грудное молоко. [3] [4] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы вич-инфекции
Инкубационный период ВИЧ длится от четырёх недель до трёх месяцев (в единичных случаях — до года).
Первые признаки ВИЧ
ВИЧ-инфекция не имеет специфических симптомов. Все клинические проявления могут относиться как к другим инфекционным и неинфекционным заболеваниям, так и к проявлениям вторичных заболеваний, которые развиваются на фоне иммунодефицита. Однако можно выделить лишь основные симптомы острой ВИЧ-инфекции, которые проявляются в первые три недели – три месяца от момента инфицирования:
- увеличение лимфатических узлов (чаще всего шейных и подмышечных);
- лихорадка (температура при ВИЧ чаще субфебрильная — от 37,1°C до 38,0°C);
- сыпь;
- воспаление нёбных миндалин и, как следствие, боли в горле;
- слабость, бессонница;
- головные боли.
Вышеперечисленные симптомы ВИЧ могут наблюдаться примерно у 30% заболевших. Ещё у 30-40% острая ВИЧ-инфекция может протекать в более тяжёлой форме (с развитием герпетической инфекции, пневмонии, менингита, энцефалита) и примерно у 30% не наблюдается.
Продолжительность клинических проявлений в случае их возникновения варьируется от нескольких дней до нескольких месяцев. Обычно симптомы ВИЧ длятся около 2-3 недель, после чего все проявления исчезают. Исключение может составлять увеличение лимфоузлов, которое часто сохраняется на протяжении всего заболевания.
Не стоит искать у себя какие-либо симптомы ВИЧ. Единственная возможность узнать о наличии или отсутствии ВИЧ-инфекции — пройти лабораторное исследование крови на антитела к ВИЧ минимум через три месяца после «рискованной» ситуации или на РНК ВИЧ минимум через два месяца.
Патогенез вич-инфекции
Проникнув в организм человека любым из вышеперечисленных способов, вирус с помощью специфического гликопротеида gp120 фиксируется на мембране клеток-мишеней, в которых есть белок CD4. Данный рецептор есть у Т-лимфоцитов (Т4, хелперы), он играет главную роль в иммунном ответе. Также белок CD4 есть у у моноцитов, макрофагов, эндотелиальных и других клеток.
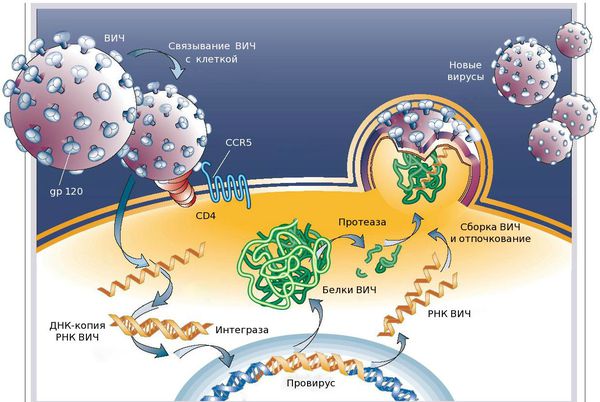
После фиксации на мембране вирус проникает в клетку, там его РНК благодаря ферменту ревертазы синтезирует (создаёт) ДНК, которая встраивается в генетический аппарат здоровой клетки. Там она может существовать в виде провируса в течение всей жизни, при этом оставаясь неактивной. Когда провирус активируется, в заражённой клетке происходит активное накопление новых вирусных частиц, что приводит к разрушению текущей клетки и поражению новых. [3]
Свободный белок gp120 также способен соединяться с рецептором СD4, который присутствует у неинфицированных Т4 лимфоцитов. Вместе они распознаются иммунной системой как чужеродные и разрушаются клетками-киллерами. Ещё одной причиной гибели СD4 клеток являются биологически активные вещества, которые секретируют инфицированные ВИЧ макрофаги. Кроме того, у инфицированных Т-хелперов появляется способность формирования массивных скоплений, в связи с чем их количество резко уменьшается.
Клетки иммунной системы необходимы организму человека для его защиты от бактерий, вирусов, простейших, опухолевых клеток и других чужеродных агентов. Заражённые ВИЧ Т4 клетки не способны осуществлять свою основную функцию, в связи с чем разрушается иммунная система и нарушается нормальная реакция на чужеродные агенты. ВИЧ-инфицированный человек становится беззащитным перед микроорганизмами, даже включая те, которые не представляют опасности для незаражённого человека (оппортунистические инфекции), повышается риск развития онкологических заболеваний.
Также в патологический процесс зачастую вовлекается нервная система. Это становится причиной функциональных, а затем и трофических поражений нейронов и нарушения мозговой деятельности.
Классификация и стадии развития вич-инфекции
Выделяют пять стадий инфицирования:
1) Стадия инкубации — фаза от момента заражения до выработки антител и/или появления реакции, представленных признаками «острой ВИЧ-инфекции». Продолжительность — от четырёх недель до трёх месяцев (в единичных случаях — до года).
В среднем длительность стадии инкубации составляет от 3 до 6 месяцев. В тот период вирус в организме человека активно размножается, но никак себя не проявляет ни клинически, ни при лабораторном исследовании на антитела к ВИЧ. Однако человек в этой стадии уже заразен.
2) Стадия первичных проявлений — этап, который начинается, соответственно, через 3-6, максимум 12 месяцев от момента заражения. В этот период продолжается активное размножение вируса, и появляется первичный ответ в виде выработки антител или клинических проявлений. Поэтому вторую стадию ВИЧ-инфекции можно выявить при сдаче крови на антитела к ВИЧ.
Стадия первичных проявлений может быть бессимптомной (чаще всего), а также проявляться в виде ряда неспецифических признаков ВИЧ:
- субфебрильная температура;
- сыпь;
- увеличение лимфоузлов;
- кандидоз слизистых;
- герпетическая инфекция; ;
- пневмония и другие проявления.
Принято считать, что человек находится в стадии острой ВИЧ-инфекции на протяжении 12 месяцев от появления антител к ВИЧ.
3) Субклиническая, или латентная, стадия ВИЧ — период замедленного размножения вируса, по сравнению с предыдущими стадиями. Антитела к ВИЧ в крови продолжают выявляться. Единственный признак ВИЧ — увеличение лимфатических узлов, которое возникает не всегда. Продолжительность стадии без специфического лечения — от 6 до 7 лет (в отдельных случаях может варьироваться от 2 до 20 лет).
4) Стадия вторичных заболеваний — фаза, в которой продолжается репликация ВИЧ. Она сопровождается активной гибелью CD4-лимфоцитов и, следовательно, истощением иммунной системы. Всё это становится причиной развития вторичных (в том числе оппортунистических) инфекционных и/или онкологических заболеваний:
- туберкулёза;
- кандидоза;
- саркомы Капоши;
- опоясывающего герпеса и других болезней.
Продолжительность данной стадии зависит от заболевания, своевременного принятия мер и индивидуальных свойств иммунной системы.
5) Стадия СПИДа (терминальная стадия) — финальный этап течения ВИЧ-инфекции. Происходит развитие тяжёлых вторичных инфекций, угрожающих жизни, их генерализация (распространение по всему организму), развитие онкологических заболеваний и поражение центральной нервной системы, которое может сопровождаться неврологическими симптомами: растерянностью и забывчивостью, неспособностью сконцентрироваться, изменением поведения, головными болями, расстройствами настроения, нарушением координации и трудностями при ходьбе. [9]
При отсутствии своевременно назначенного специфического лечения стадия СПИДа наступает в среднем через 10-12 лет от момента инфицирования. [4]
Осложнения вич-инфекции
Осложнения ВИЧ-инфекции — это вторичные инфекции, развивающиеся на фоне иммунодефицита. К таким заболеваниям относятся:
- Кандидоз (слизистой ротоглотки, дыхательных путей, пищевода) — одна из разновидностей грибковой инфекции, вызывается микроскопическими дрожжеподобными грибами рода Candida. Основные симптомы — боли в горле, при глотании, белый творожистый налёт на языке и/или миндалинах и твёрдом нёбе, субфебрильная лихорадка.
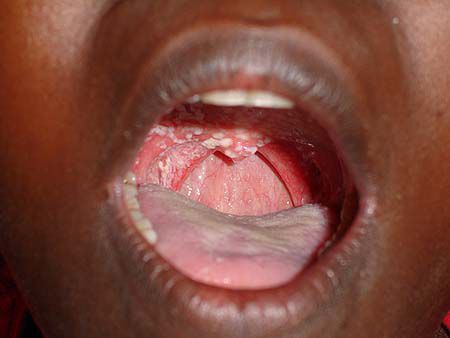
- Опоясывающий герпес — вирусная инфекция, характеризующаяся односторонними герпетиформными высыпаниями на коже (зудящих везикул с жидкостью с их последующим вскрытием и образованием корочек) с сильным болевым синдромом. Возбудитель — Varicella zoster, вирус семейства герпесвирусов, который при первой встрече с организмом (чаще в молодом возрасте) вызывает типичную ветряную оспу. Лечение проводится противогерпетическими препаратами.
- Туберкулёз — инфекционное заболевание, вызываемое различными видами микобактерий группы Mycobacterium. Основные симптомы — лихорадка, кашель, гипергидроз (повышенная потливость, особенно в ночные часы), одышка. Для постановки диагноза необходимо выполнение ФЛГ или КТ лёгких, консультация врача-фтизиатра. У ВИЧ-инфицированных особенностью течения туберкулёза является его частая генерализация, т.е. распространение на другие органы помимо лёгких, что усложняет лечение и, соответственно, ухудшает прогноз.
- Саркома Капоши — многоочаговая опухоль злокачественного характера, поражающая весь организм. Она формируется из эндотелия сосудов, ей свойственно различное клиническое течение. Преимущественно болезнь проявляется новообразованиями кожи, но также она может повлиять на слизистые оболочки, лимфосистему и внутренние органы (прежде всего, на лёгкие и желудочно-кишечный тракт). Лечение должно проводиться совместно с врачом-онкологом.
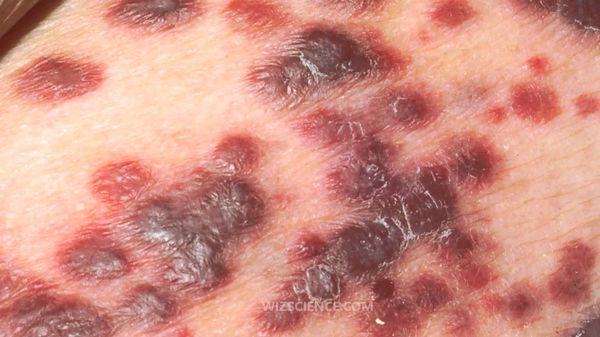
- Пневмоцистная пневмония — атипичная пневмония, характерная для лиц с иммунодефицитом. Основные симптомы — интенсивная одышка и лихорадка. Для постановки диагноза необходимо выполнения КТ лёгких.
- Церебральный токсоплазмоз — паразитарное заболевание, которое также характерно для лиц с выраженным иммунодефицитом, появляющееся образованием многочисленных очагов в головном мозге. Занимает 2-3 место среди оппортунистических инфекций у больных СПИДом. Имеет различную неврологическую симптоматику — головные боли, снижение памяти, эпилептические припадки и другие проявления. Лечение проводится совместно с врачом-неврологом.
Также могут возникнуть другие бактериальные и вирусные инфекции и онкологические заболевания. [4]
Диагностика вич-инфекции
Для диагностики ВИЧ-инфекции применяется специальный иммуноферментный анализ (ИФА) 4-го поколения, который заключается в реакции «антиген-антитело». Он позволяет определить наличие антител к ВИЧ в организме человека. Соответственно, тест на ВИЧ будет достоверным только после завершения периода инкубации, т.е. после того, как организм выработает достаточное количество антител (не ранее четвёртой недели после заражения). У большинства людей тест будет достоверным через три месяца, однако для исключения ВИЧ-инфекции на 100% необходимо сдать анализ через 6 и 12 месяцев.
В случае положительного анализа на ВИЧ тот же образец крови исследуется в лаборатории ещё раз: если результат вновь положительный, то необходим тест другого типа — иммунный блоттинг. Положительный результат иммунного блоттинга (после положительного результата ИФА) достоверен на 99,9%, что является максимально точным для любого медицинского теста. Если же иммуноблот отрицательный, то делается вывод, что первый тест был ложноположительным, и ВИЧ у человека нет.
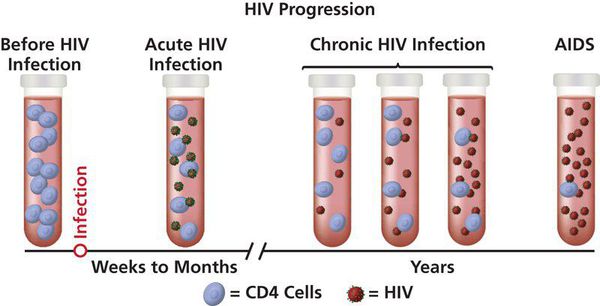
Результат иммуноблота может интерпретироваться как положительный, отрицательный или неопределенный (т.е. наличие в иммуноблоте как минимум одного белка к вирусу). Неопределённый результат может наблюдаться, если анализ сдан в период инкубации: заражение произошло не так давно, поэтому в крови пока находится немного антител к ВИЧ, но спустя некоторое время иммуноблот станет положительным. Также неопределённый результат может возникнуть при отсутствии ВИЧ-инфекции и наличии некоторых хронических заболеваний. В таком случае иммуноблот станет отрицательным, либо будет выявлена причина неопределённого результата.
Как считаю многие, анализ на ВИЧ-инфекцию сдаётся не при любом заборе крови. Однако данное исследование является добровольным для всех, кроме:
- доноров крови;
- иностранцев и лиц без гражданства, которые хотят въехать на территорию Российской Федерации более чем на три месяца;
- медперсонала, работающего с кровью;
- лиц, находящихся в местах лишения свободы.
Люди, не относящиеся ни к одной из перечисленных категорий граждан, не сдают анализ на ВИЧ во время ежегодных профилактических медицинских осмотров, поэтому наличие медицинской книжки также не гарантирует отсутствие ВИЧ-инфекции.
Лечение вич-инфекции
В случае, если ВИЧ-инфекция обнаружена, человек встаёт на учёт в Центре по борьбе со СПИДом, где в дальнейшем наблюдается у врача-инфекциониста.
Лекарственного средства, которое могло бы полностью избавить от ВИЧ, в настоящее время нет. Однако, существуют препараты, значительно продлевающие жизнь и способные предупредить развитие СПИДа. Препараты для лечения показаны всем ВИЧ-инфицированным. Они предоставляются бесплатно после дообследования, назначаемого врачом-инфекционистом.
Препараты для лечения ВИЧ называются антиретровирусными (АРВ). Благодаря АРВ подавляется размножение вируса, в результате чего восстанавливается или не нарушается функция иммунной системы. ВИЧ-инфицированные пациенты, регулярно принимающие данные препараты, не способны передавать вирус даже при незащищённых половых контактах.
Особенность лечения ВИЧ-инфекции заключается в:
- необходимости ежедневного пожизненного приёма препаратов (как правило, не менее трёх);
- контроле эффективности лечения у врача-инфекциониста;
- наблюдении возможных нежелательных явлений, связанных с приёмом препаратов.
Для лечения используются хорошо изученные современные препараты, не оказывающие опасного токсического влияния на другие органы и системы, при условии соблюдения рекомендаций врача и своевременного обследования.
Прогноз. Профилактика
При раннем выявлении и своевременном начале специфического лечения продолжительность жизни ВИЧ-инфицированных людей может не уступать средней продолжительности жизни населения. Поэтому чрезвычайно важно как можно раньше начать наблюдение и лечение у специалиста.
Профилактика ВИЧ
К сожалению, вакцины от данной инфекции пока не существует.
Методами профилактики являются:
- защищённые половые контакты;
- использование стерильных инструментов для проведения различных манипуляций, сопровождающихся нарушением целостности слизистых и кожных покровов;
- тестирование на ВИЧ всего населения не реже 1 раза в год;
- обязательное обследование на ВИЧ при планировании беременности, постановке на учёт в связи с беременностью, а также во время беременности и перед родами;
- обязательный приём препаратов всем ВИЧ-инфицированным женщинам во время беременности;
- приём препаратов всем ВИЧ-инфицированным для снижения вероятности передачи вируса. [4][6]
При положительном результате исследования на антитела к ВИЧ необходимо:
- обратиться в Центр по профилактике и борьбе со СПИДом;
- получить подробную информацию о состоянии своего здоровья, о жизни с ВИЧ и о своих правах и обязанностях;
- начать приём препаратов;
- следовать рекомендациям лечащего врача.
Хотелось бы отдельно отметить, что люди, живущие с ВИЧ, ничем не отличаются от других людей, кроме наличия в их организме вируса.
В последнее время среди ВИЧ-положительных пациентов гомосексуальной ориентации участились случаи развития анального рака под влиянием вируса ВПЧ. Для его профилактики институт СПИДа штата Нью-Йорк рекомендует пациентам проходить скрининг на анальную дисплазию. Он включает:
- сбор анамнеза;
- осмотр и пальцевое ректальное обследование;
- анальный тест Папаниколау — взятие мазка из ануса;
- кольпоскопия [8] .
На развитие анального рака будет указывать боль и зуд в области ануса, кровянистые выделения, недержание кала, шишки и язвочки в перианальной зоне. Чтобы устранить осложнение, следует обратиться к колопроктологу.
Источник https://pharmateca.ru/ru/archive/article/30925
Источник https://diseases.medelement.com/disease/%D1%81%D0%BE%D1%87%D0%B5%D1%82%D0%B0%D0%BD%D0%BD%D0%B0%D1%8F-%D0%B2%D0%B8%D1%87-%D1%82%D0%B1-%D0%B8%D0%BD%D1%84%D0%B5%D0%BA%D1%86%D0%B8%D1%8F-2018/16124
Источник https://probolezny.ru/vich-infekciya/