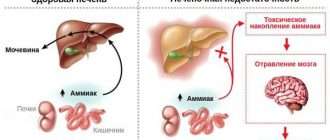
Болезнь Вильсона ( Болезнь Вестфаля-Вильсона-Коновалова , Болезнь Вильсона-Коновалова , Гепатолентикулярная дистрофия , Гепатоцеребральная дистрофия , Лентикулярная прогрессирующая дегенерация )
Болезнь Вильсона — наследственное заболевание, передающееся по аутосомно-рецессивному типу. Возникает в условиях мутаций в гене АТР7В, кодирующем белок медьтраснпортирующей АТФазы печени. Характерный признак болезни Вильсона — накопление меди в различных органах и тканях, в большей степени в печени и базальных ганглиях. Болезнь Вильсона может протекать в брюшной, ригидно-аритмогиперкинетической, дрожательной или экстрапирамидно-корковой форме. Диагностика болезни Вильсона включает офтальмологическое обследование, биохимические анализы мочи и крови, МРТ или КТ головного мозга. Основу патогенетической терапии составляют тиоловые препараты, которые могут приниматься в течении нескольких лет и даже пожизненно.
МКБ-10
Общие сведения
Болезнь Вильсона — наследственное заболевание, передающееся по аутосомно-рецессивному типу. Возникает в условиях мутаций в гене АТР7В, кодирующем белок медьтраснпортирующей АТФ-азы печени. Характерный признак болезни Вильсона — накопление меди в различных органах и тканях, в большей степени в печени и базальных ганглиях. Первооткрыватель заболевания — А.К. Вильсон, описавший заболевание в 1912 году, в отечественной медицине — Н.А. Коновалов. Патогенез болезни Вильсона был выявлен в 1993 году. Понятию «болезнь Вильсона» соответствуют также: болезнь Вильсона-Коновалова, болезнь Вестфаля-Вильсона-Коновалова, дистрофия гепатоцеребральная, дистрофия гепатолентикулярная, дегенерация лентикулярная прогрессирующая.

Причины
Ген АТР7В картирован на длинном плече хромосомы 13 (13q14.3-q21.1). Организм человека содержит около 50-100 мг меди. Суточная потребность меди для человека — 1-2 мг. 95% абсорбированной в кишечнике меди, транспортируется в форме комплекса с церулоплазмином (один из глобулинов сыворотки, синтезируемых печенью) и только 5% в форме комплекса с альбумином. Кроме того, ион меди входит в состав важнейших метаболических ферментов (лизилоксидаза, супероксиддисмутаза, цитохром-С-оксидаза и др.). При болезни Вильсона происходит нарушение двух процессов обмена меди в печени — биосинтез главного медьсвязывающего белка (церулоплазмина) и выведение меди с желчью, следствием чего становится повышение уровня несвязанной меди в крови. Концентрация меди в различных органах (чаще всего в печени, почках, роговице и головном мозге) увеличивается, что приводит к их токсическому поражению.
Классификация
Согласно классификации Н.В. Коновалова различают пять форм болезни Вильсона:
- брюшная
- ригидно-аритмогиперкинетическая
- дрожательно-ригидная
- дрожательная
- экстрапирамидно-корковая
Симптомы
Для болезни Вильсона характерен клинический полиморфизм. Первые проявления заболевания могут появиться в детстве, юношестве, в зрелом возрасте и гораздо реже в зрелом возрасте. В 40-50% случаев Болезнь Вильсона манифестирует с поражения печени, в остальных — с психических и неврологических расстройств. С вовлечением в патологический процесс нервной системы обнаруживается кольцо Кайзера-Флейшера.
Брюшная форма развивается преимущественно до 40 лет. Характерный признак — тяжелое поражение печени по типу цирроза печени, хронического гепатита, фульминантного гепатита.
Ригидно-аритмогиперкинетическая форма манифестирует в детском возрасте. Начальные проявления — мышечная ригидность, амимия, смазанность речи, трудности при выполнении мелких движений, умеренное снижение интеллекта. Для этой формы заболевания характерно прогрессирующее течение, с наличием эпизодов обострения и ремиссии.
Дрожательная форма возникает в возрасте от 10 до 30 лет. Преобладающим симптомом является тремор. Кроме того, могут наблюдаться брадикинезия, брадилалия, тяжелый психоорганический синдром, эпилептические приступы.
Экстрапирамидно-корковая форма встречается весьма редко. Ее начало схоже с началом какой-либо из вышеперечисленных форм. Для нее характерны эпилептические припадки, экстрапирамидные и пирамидные нарушения и выраженный интеллектуальный дефицит.
Диагностика
Офтальмологическое исследование с помощью щелевой лампы выявляет кольцо Кайзера-Флейшера. Биохимические исследования мочи обнаруживают повышенную экскрецию меди в суточной моче, а также снижение концентрации церулоплазмина в крови. С помощью визуализационных методов (КТ и МРТ головного мозга) обнаруживают атрофию полушарий большого мозга и мозжечка, а также базальных ядер.
При диагностике болезни Вильсона неврологу необходимо дифференцировать ее от паркинсонизма, гепатоцеребрального синдрома, болезни Геллервордена-Шпатца. Основным дифференциально-диагностическим признаком этих заболеваний является отсутствие характерных для болезни Вильсона кольца Кайзера-Флейшера и расстройств обмена меди. Для подтверждения болезни Вильсона проводится генодиагностика.
Лечение болезни Вильсона
Основой патогенетического лечения является назначение тиоловых препаратов, в первую очередь — D-пеницилламина либо унитиола. Главное преимущество купренила — низкая токсичность и возможность длительного приема при отсутствии побочных эффектов. Его назначают по 0,15 г (1 капсула) в сутки (только после еды), в дальнейшем, в течение 2,5-3 месяцев дозу увеличивают до 6-10 капсул/сутки (оптимальная доза). Лечение D-пеницилламином проводится годами и даже пожизненно с небольшими перерывами (на 2-3 недели) в случае появления побочных эффектов (тромбоцитопения, лейкопения, обострения язвенной болезни желудка и т. д.).
Унитиол назначают в случае непереносимости (плохой переносимости) D-пеницилламина. Длительность одного курса лечения — 1 месяц, после чего лечение приостанавливают на 2,5-3 месяца. В большинстве случаев наступает улучшение общего состояния пациента, а также регресс неврологических симптомов (скованности, гиперкинезов). В случае доминирования гиперкинезов рекомендовано назначение небольших курсов нейролептиков, при ригидности — леводопы, карбидопы, тригексифенидила.
В случае тяжелого течения болезни Вильсона, при неэффективности консервативного лечения за рубежом прибегают к трансплантации печени. При положительном исходе операции состояние пациента улучшается, восстанавливается обмен меди в организме. В дальнейшем лечение пациента составляет иммуносупрессивная терапия. В России на сегодня постепенно внедряется в клиническую практику метод биогемоперфузии с изолированными живыми клетками селезенки и печени (т. н. аппарат «вспомогательная печень). Немедикаментозное лечение состоит в назначении диеты (стол №5) в целях исключения продуктов богатых медью (кофе, шоколад, бобовые, орехи и т. д.).
Прогноз и профилактика
В случае своевременного диагностирования болезни Вильсона и проведения адекватной медьснижающей терапии возможна нормализация общего состояние пациента и обмена меди в организме. Постоянный прием тиоловых препаратов по схеме, назначенной врачом-специалистом, позволяет поддерживать профессиональную и социальную активность пациента.
Для предотвращения рецидивов болезни Вильсона рекомендовано проведение лабораторных исследований крови и мочи пациента несколько раз в год. Необходим контроль следующих показателей: концентрация меди, церулоплазмина и цинка. Кроме того, рекомендовано проведение биохимического анализа крови, общего анализа крови, а также регулярные консультации у терапевта и невролога.
Болезнь Вильсона — Коновалова — симптомы и лечение
Что такое болезнь Вильсона — Коновалова? Причины возникновения, диагностику и методы лечения разберем в статье доктора Толмачева Алексея Юрьевича, невролога со стажем в 21 год.
Над статьей доктора Толмачева Алексея Юрьевича работали литературный редактор Юлия Липовская , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Болезнь Вильсона-Коновалова — редкое наследственное дистрофическое заболевание, которое развивается из-за избыточного накопления меди в организме. Больше всего металла скапливается в головном мозге, глазах (с образованием характерной пигментации), печени и почках. При этом в органах нарушается обмен веществ и прогрессируют дистрофические изменения [4] .
Заболевание впервые описано в 1912 году английским неврологом Семюэлем Вильсоном. В своём печатном труде он описал симптомы и особенности изменения внутренних органов при этом заболевании. Обычно первые проявления становились заметными в молодом возрасте, позже прогрессировала ригидность, сложности при глотании, снижение двигательной способности мягкого нёба, языка, губ (причина расстройства речи — дизартрии). Развиваются непроизвольные движения, расстройства психики — пониженное или необоснованно повышенное настроение, немотивированная агрессия, которая на поздних стадиях сменяется безучастностью, бредовые идеи, галлюцинации.
Российский невролог Николай Васильевич Коновалов изучал болезнь Вильсона на протяжении многих лет. Это позволило ему создать оригинальную полноценную классификацию различных форм заболевания. За огромный вклад Коновалова в исследование проблемы фамилия учёного навсегда дополнила название болезни.
Частота встречаемости — от 1 до 9 случаев на 100000 населения.
Основная причина возникновения болезни — мутация гена с названием ATP7B, который ответственен за встраивание ионов меди в белок церулоплазмин [14] . Всего описано более 300 мутаций этого гена. База данных мутаций постоянно расширяется новыми вариантами [6] . По международным оценкам, носителем аномального гена является примерно 1 человек из 100. При данном виде наследования заболевание проявляется симптоматикой только в том случае, если патологический ген был унаследован от обоих родителей. Мальчики и девочки болеют с одинаковой частотой [1] [2] [3] [8] [15] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы болезни Вильсона — Коновалова
Симптомы при заболевании подразделяют на четыре группы:
- проявления заболевания, связанные с поражением печени;
- неврологическая симптоматика;
- психическая симптоматика;
- изменения со стороны остальных внутренних органов.
Наиболее значимые проявления заболевания — поражения печени, неврологические и психические симптомы, изменения со стороны глаз.
Симптомы поражения внутренних органов при болезни Вильсона — Коновалова [3] :
Изменения со стороны печени выделяют среди первых симптомов заболевания (часто они проявляются в возрасте 4-5 лет). Иногда болезнь Вильсона — Коновалова проявляется острым или хроническим гепатитом, который можно принять за воспалительное бактериальное или вирусное поражение печени. Патологический процесс начинается с быстрого развития желтухи: кожные покровы и видимые слизистые, белок глаз приобретают жёлтый оттенок. К изменению цвета кожных покровов могут присоединиться симптомы интоксикации и астении (общей слабости, повышенной утомляемости, неустойчивости настроения). Также возможна анорексия — потеря аппетита и отказ отвращение к пище.
Неврологические симптоматика и проявления психических заболеваний при болезни Вильсона — Коновалова встречаются в 35 и 10 % случаев, обычно в возрасте с 10 до 35 лет, хотя встречаются и поздние случаи начала в 55 лет. Неврологические проявления включают нарушение координации с дрожанием конечностей при удержании позы, также возможен тремор в состоянии покоя. Развиваются синдром мышечной дистонии — непроизвольного сокращения мышц с изменением нормального положения тела. Изменения тонуса мышц приводит к нарушению ходьбы. Также из-за уже указанных нарушений работы мышц изменяется речь. Возникает повышенное слюноотделение.
Психиатрическая симптоматика примерно у трети пациентов предшествует всем остальным симптомам. Так как проявления неспецифичны, их обычно не связывают с болезнью Вильсона — Коновалова. У детей отмечается задержка или остановка умственного развития, снижение успеваемости в школе и способности концентрировать внимание. Наблюдается резкая смена настроения — неадекватное чувство счастья и восторга сменяется мимолетным чувством страха и необоснованной тревоги. Возможно вспышки агрессии или сексуальные отклонения. Острые психиатрические нарушения (психозы) случаются редко.
У взрослых пациентов снижается скорость мыслительных процессов при сохранной памяти на прошлые события. По мере развития слабоумия агрессию и депрессию сменяет беспричинная эйфория, а затем эмоциональная тупость и безучастность. Нарастают такие симптомы как беспричинный смех и плач, болезненные рефлексы ротовой мускулатуры, хватательные автоматизмы [10] .
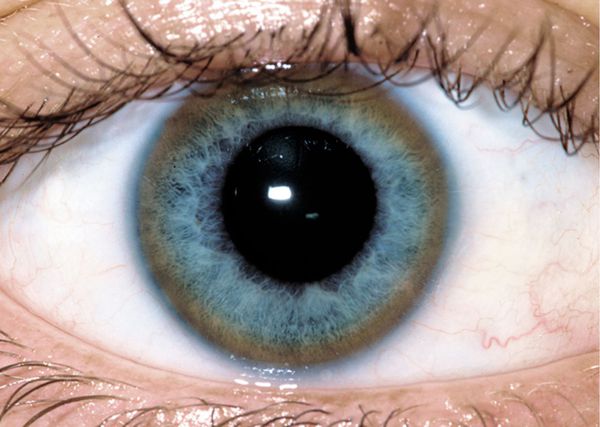
К поражениям глаз при болезни Вильсона относят кольца Кайзера-Флейшера и медную катаракту по типу «подсолнух». Но правильно трактовать эти симптомы может только специалист, так как они встречаются также при отравлении медью. Кольца Кайзера-Флейшера не всегда видны невооруженным глазом, иногда они обнаруживаются только при офтальмологическом осмотре при помощи щелевой лампы [1] [2] [3] [8] [15] .
Патогенез болезни Вильсона — Коновалова
Основной механизм развития болезни Вильсона — Коновалова — это нарушение обменных процессов в организме, в результате которых медь накапливается в различных органах и тканях с прогрессирующим нарушением их функций. Кроме того, за различные симптомы отвечает разнообразие мутаций гена ATP7B, определяющего, как именно проявится заболевание [12] .
Ген ATP7B кодирует белки, ускоряющие химические реакции меди у человека: АТФ-азу 7А и АТФ-азу 7В. Первый фермент способствуют всасыванию меди в кишечнике и её проникновению в головной мозг. Фермент мРНК АТФ-аза 7В обнаружен в клетках печени и сосудах капиллярах мозга. Он способствует выведению меди из головного мозга в кровь и из крови в желчь. Дефицит этого биологически активного вещества вызывает болезнь Вильсона — Коновалова.
Накопление меди в организме вызывает хроническое отравление (интоксикацию). Накапливаясь в печени и мозге, медь способствует гибели клеток этих органов. Это вызывает воспалительную реакцию и разрастание соединительной ткани в печени — фиброз печеночных протоков с нарушением их функций, из-за чего позже формируется цирроз. Гибель нервных клеток и их растворение (лизис) в головном мозге образует полости (кисты). Изменения других органов и тканей, как правило, незначительны.
При выбросе меди из разрушенных клеток в кровь под воздействием внешних факторов (инфекции, интоксикации, реакции на медикаменты) концентрация меди в плазме крови может повыситься в несколько раз. Это вызывает массированный распад эритроцитов, что приводит к тяжелому, чаще смертельному осложнению — фульминантной ( от лат. fulmino — молниеносный, мгновенно и быстро развивающийся) печеночной несостоятельности.
Всё многообразие симптомов болезни Вильсона — Коновалова вызывает не только накопление меди, но и отравление продуктами распада собственных клеток (аутоинтоксикация) [1] [2] [3] [7] [8] [15] .
Классификация и стадии развития болезни Вильсона — Коновалова
В России чаще всего применяется классификация, которая построена на клинических особенностях болезни, сочетания поражения печени и центральной нервной системы. Течение болезни Вилсона — Коновалова подразделяют на:
- бессимптомную форму;
- печеночную форму;
- церебральную форму;
- смешанную форму.
Также применяется классификация Коновалова, которая включает пять форм гепато-церебральной дистрофии:
- Брюшная (абдоминальная) форма — тяжёлое поражение печени, которое проявляется гепатопатией, вильсоновским гепатитом, циррозом печени и фульминарной печёночной несостоятельностью. Может привести к смерти до появления симптомов со стороны нервной системы. Продолжительность от нескольких месяцев до 3-5 лет;.
- Ригидно-аритмогиперкинетическая (ранняя) форма — характеризуется быстрым течением и начинается в детском возрасте. Среди симптомов преобладает мышечная скованность, приводящая к изменениям суставов и их тугоподвижности. Движения замедляются, руки и ноги могут непроизвольно двигаться спирально и червеобразно в сочетании с быстрыми непроизвольными сокращениями мышц. Характерны нарушения речи (дизартрия) и глотания (дисфагия), насильственный, непроизвольный смех и плач, нарушения эмоционального состояния, умеренное снижение интеллекта. Заболевание продолжается 2-3 года, заканчивается смертельным исходом.
- Дрожательно-ригидная форма встречается чаще остальных; начинается в юношеском возрасте, протекает медленно, иногда с периодами полного или неполного восстановления и внезапными ухудшениями, сопровождающиеся повышением температуры тела до 37–38 °C ; характерно одновременное развитие тяжёлой скованности мышц и ритмичного дрожания частотой 2-8 подёргиваний в секунду. Эти симптомы резко усиливаются при движениях и волнении, но исчезают в покое и во сне. Иногда наблюдаются дисфагия и дизартрия. Средняя продолжительность жизни около 6 лет.
- Дрожательная форма проявляется с возраста 20-30 лет, течёт относительно медленно (10-15 лет и более); преобладает дрожание, ригидность появляется лишь в конце болезни, иногда наблюдается пониженный тонус мышц; отмечается отсутствие мимики, медленная монотонная речь, тяжёлые изменения психики, частые эмоциональные вспышки, судорожные припадки.
- Экстрапирамидно-корковая форма встречается реже других. Типичные для гепато-церебральной дистрофии нарушения в дальнейшем осложняются внезапно развивающимися двигательными расстройствами по типу параличей (пирамидными парезами), судорожными (эпилептиформными) припадками и слабоумием тяжёлой степени. Длится 6-8 лет, заканчивается летально.
По течению заболевание можно разделить на две сменяющиеся стадии:
- латентная — характеризуется отсутствием внешних проявлений болезни, характерные изменения определяются только при лабораторном исследовании;
- стадия клинических проявлений — появляются специфические симптомы болезни гепато-церебеллярной дегенерации.
Во время лечения выделяют также стадию отрицательного баланса меди, при которой наблюдается регресс клинической симптоматики и характерных лабораторных изменений [4] .
Осложнения болезни Вильсона — Коновалова
Фульминантная форма гепатита (Вильсоновский криз) — одно из самых опасных осложнений (смертность около 60-95 %). Провоцирующим фактором становятся инфекции или интоксикации. Характерен массовый некроз клеток печени. В дальнейшем медь из поврежденных гепатоцитов обильно выделяется в кровь, что приводит к быстрому разрушению эритроцитов. Свободный гемоглобин из разрушенных эритроцитов дополнительно повреждают печень, замыкая патологический круг тяжелейшей интоксикации и оказывая токсическое действие на почки и другие органы. Характерный симптом — «тающая печень» (печень быстро уменьшается в размерах).
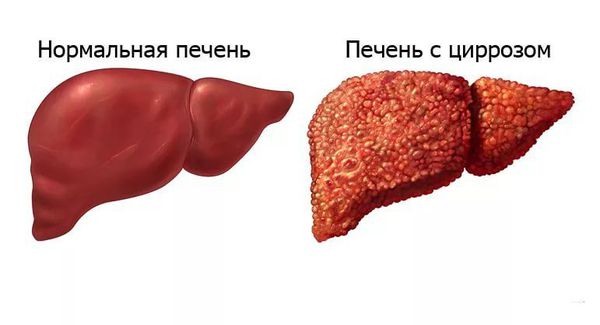
Цирроз — замещение нормальной ткани печени фиброзной (соединительной). Долгое время может прогрессировать без симптоматики, но при неврологических проявлениях болезни Вилсона — Коновалова присутствует у всех пациентов в той или иной степени. Цирроз печени приводит к постепенному нарушению её функций — особенно дезинтоксикации.
Гемолиз — повышенное разрушение красных телец крови (эритроцитов). Приводит к снижению количества эритроцитов и гемоглобина в крови — анемии. Основная функция эритроцитов — это доставка кислорода органам и тканям, поэтому снижение их количества приводит к недостаточному поступление кислорода. Это влечёт за собой нарушение метаболизма, внутренние органы начинают работать неправильно. Данное осложнение может протекать в острой, хронической и рекуррентной форме.
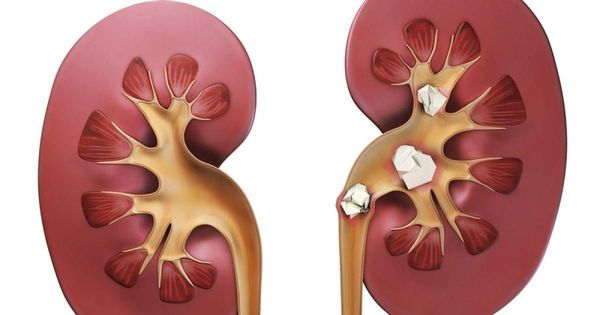
Образование камней в почках происходит из-за нарушения функционирования канальцев почек из-за накопления в почках меди. Камни мешают нормальной работе почек, ухудшают процесс фильтрации и усложняют процесс выделения мочи.
Параноидный бред — психотическое нарушение, чаще выражается в виде идей преследования, уничтожения, обвинения, ущерба или отравления [10] . Бред может быть как преходящим, так и затяжным. Возможно появление галлюцинаций.
Диагностика болезни Вильсона — Коновалова
Диагноз основывается на сочетании клинических симптомов, лабораторных данных и молекулярно-генетического тестирования. Ни один лабораторный тест, за исключением определения болезнетворного гена АТР7В на молекулярном уровне, не обеспечивает 100 % гарантию диагностики заболевания.
Основные диагностические показатели болезни Вильсона — Коновалова:
Суммарные баллы:
- 4 и более — высокая вероятность болезни;
- 2-3 — болезнь вероятна, но требуется дальнейшее обследование пациента;
- 0-1 — болезнь сомнительна.
Для уточнения степени поражения и формы заболевания используются МРТ головного мозга, хотя только на основании МРТ диагноз поставить нельзя. При МРТ исследовании сразу видны характерные очаги и уменьшение объёма головного мозга. Специфичным, но более редко встречающимся симптомом при данном заболевании на МРТ снимке является картина, напоминающая «лицо гигантской панды». КТ- и МРТ-проявления могут опережать клиническую симптоматику.
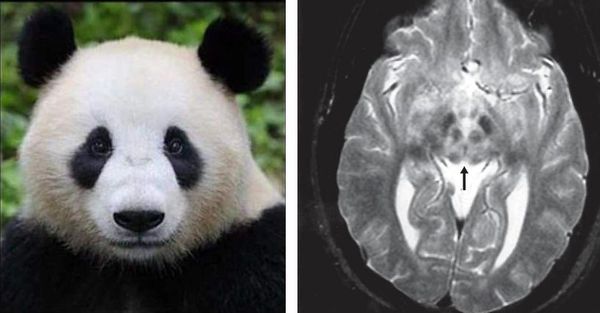
Компьютерная томография (КТ) головного мозга при наличии болезни выявляет увеличение желудочков, атрофию коры и ствола мозга. Однако более важным диагностическим методом при церебральной форме заболевания является именно МРТ.
Для определения очагов скопления меди и нехирургической оценки метаболизма мозга может потребоваться магнитно-резонансная спектроскопия (МРС). Это метод, позволяющий оценить изменения биохимической концентрации веществ при различных заболеваниях в тканях организма.
Также используется позитронно-эмиссионная томография (ПЭТ), позволяющая определить степень обмена и транспорта веществ в организме.
Перспективным методом ранней диагностики является транскраниальное УЗИ головного мозга.
Изменения, определяемые при УЗИ, КТ и МРТ печени и почек определяются и при других болезненных состояниях, поэтому не являются строго специфичными для болезни Вильсона — Коновалова и могут быть использованы только для оценки эффективности лечения.
Новым методом диагностики степени выраженности цирроза (фиброза) печени является эластометрия печени. Исследование использует способность ультразвука проходить с различной скоростью через ткани разной плотности, что позволяет определить изменение нормальной плотности органа [1] [2] [3] [8] [16] .
Лечение болезни Вильсона — Коновалова
Целью лечения при бессимптомной стадии болезни является предотвращение проявления симптомов и нормализация лабораторных показателей. Цель на стадии клинических проявлений — стабилизация и максимально возможная регрессия основных симптомов заболевания, а также нормализация лабораторных показателей. Лечение болезни Вилсона — Коновалова можно разделить на несколько направлений.
Медикаментозное лечение. Включает в себя использование препаратов, выводящих медь из организма (медьэлиминирующая или хелатная терапия), а также использование препаратов, снижающих усвоение меди. Данное лечение назначается пожизненно.
Мировая практика предусматривает применение следующих комплексообразующих препаратов: пеницилламин, триентин, тетратиомолибдат и унитиол. Из таблетированных лекарственных средств в Российской Федерации зарегистрированы препараты d-пеницилламина.
Также при болезни Вилсона — Коновалова используются медикаменты, замедляющие и уменьшающих степень поражения органов мишеней при интоксикации медью (патогенетическая терапия). Кроме того, проводится симптоматическая терапия. Для лечения симптомов заболевания и восстановление поражённых органов используются витамины группы B, С и Е, нейропротективные и нейрометаболические средства, антиконвульсанты для лечения судорожного синдрома, препараты для коррекции психических симптомов заболевания.
Лечение препаратами, содержащими витамины группы В, способно улучшить функционирование нервной ткани, процессы её восстановления и обмен веществ. Наиболее известными комбинированными препаратами этой группы являются мильгамма и комбилипен. Витамин С (аскорбиновая кислота) способствует удалению меди из организма.
Витамин Е (альфа-токоферола-ацетат) является антиоксидантом, способным замедлять процессы окисления в организме и защищать клетки от повреждающего действия и разрушения [5] [7] .
При поражении печени оправдано применение L-орнитина-L-аспартата и других гепатопротекторов. При периферических отёках и осците назначают мочегонные. Также при выраженных отёках возможно использование фуросемида (лазикса). В случае тремора рук и насильственных движениях назначают лоразепам или клоназепам. В случае невротических проявлений (тревожности, депрессии) назначают различные антидепрессаны и анксиолитики [14] .
Диетотерапия. Полное удаление меди из рациона невозможно, так как она содержится во всех продуктах. Однако необходимо исключить из пищи продукты, в которых содержание меди превышает 0,5 мг/100 г: субпродукты, моллюски, орехи, какао-продукты, грибы, бобовые, гречневая и овсяная крупа. Следует сократить потребление сахара, рафинированных углеводов и трансжиров. В целом диету при данном заболевании можно охарактеризовать как молочно-растительную, с достаточным содержанием белка.
Хирургическое лечение. Трансплантация печени при заболевании проводится в следующих случаях:
- при развитии фульминантной (молниеносной) печеночной несостоятельности;
- при безрезультатном лечении препаратами, связывающими медь в течение 3 месяцев;
- пациентам с декомпенсированным циррозом печени – нарастающей симптоматики печёночной недостаточности.
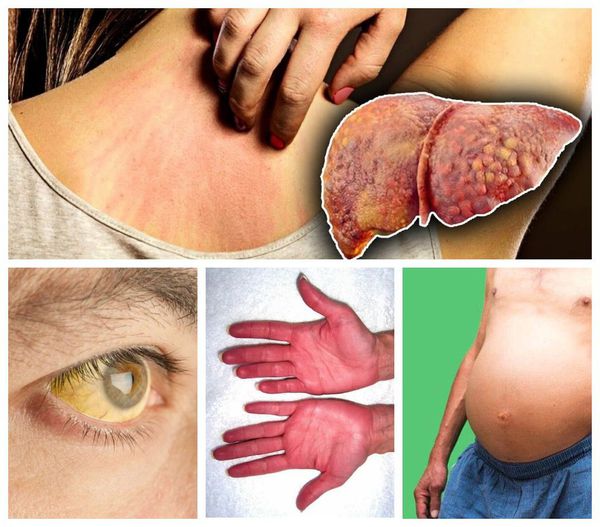
Декомпенированный цирроз печени — это нарушение нормальной работы печени, проявляющееся симптомами грубого нарушения пищеварительной функции. Проявляется следующим образом:
- Желтушность кожных покровов, склер глаз и слизистой рта;.
- Покраснение ладоней (печёночные ладони).
- Зуд кожи из-за накопления токсинов.
- Сосудистые звездочки, а также склонность к кровотечениям и гематомам при малейших повреждениях кожного покрова.
- Потеря аппетита, потеря веса вплоть до истощения;.
- Боли в области правого подреберья, иногда боли в животе без чёткой локализации.
- Накопление жидкости в брюшной полости (асцит).
- Печеночная энцефалопатия — прогрессирующее нарушение функций мозга (памяти, внимания мышления), изменение личности с неадекватным поведением различной выраженности, нарушение сознания (вплоть до комы). При несвоевременном лечении болезнь может привести к летальному исходу.
При трансплантации используется донорская пересадка печени — печень пересаживают целиком или частично. Трансплантация печени обеспечивает улучшение неврологической симптоматики более чем в 50 % случаев. При пересадке печени на стадии декомпенсированного цирроза печени выживание в течение первого года составляет 95 %, через 5 лет – 83 %, через 10 лет – 80%.
Плазмофильтрация и гемосорбция. Для удаления меди из организма также применяются фильтрация крови и плазмы: (плазмофильтрация и гемосорбция). При первой процедуре больного подключают к аппаратуре, благодаря которой кровь из одной руки, пройдя через аппарат, возвращается в другую. Клетки крови возвращаются в кровеносное русло сразу, а плазма проходит сквозь поры особого высокотехнологичного фильтра, где избавляется от продуктов распада и в очищенном виде возвращается в организм. При гемосорюбции цельная кровь пациента пропускается через ёмкость заполненную веществами – сорбентами.
В целом весь период лечения болезнь Вилсона — Коновалова можно разделить на 2 фазы: начальную фазу и фазу поддерживающей терапии. Критерием перехода на поддерживающую терапию является нормализация показателей обмена меди при 2-х последовательных исследованиях, выполненных с интервалом в 3 месяца [1] [2] [3] [8] [17] .
Прогноз. Профилактика
Болезнь Вильсона — Коновалова — это прогрессирующие заболевание, поэтому при отсутствии своевременного лечения больные умирают от цирроза печени или от инфекционно-токсических осложнений (редко). На фоне прогрессирующей неврологической симптоматики пациент может находиться в обездвиженном состоянии. При лечении выводящими медь препаратами и трансплантации печени длительная выживаемость пациентов является нормой.
Факторы, повышающие смертность при болезни Вильсона-Коновалова :
- Поздно установленнй диагноз.
- Самовольный отказ от лечения.
- Связанные с неврологической симптоматикой несчастные случаи.
- Невозможность подобрать эффективное лечение [5] .
Годовая выживаемость после трансплантации печени из-за фульминантной недостаточности достигает 70 %. Без трансплантации — единичные случаи. При декомпенсированном циррозе печени после трансплантации выживаемость пациентов в течение года — 95 %, через 5 лет — 83 %, через 10 лет — 80 %. Обратное развитие неврологической симптоматики после трансплантации отмечается более чем в 50 % случаев.
Восстановление функций печени происходит на 1-2 году лечения и не прогрессирует при полном выполнении всех рекомендаций. При фульминантном течении заболевания эффективно только оперативное лечение.
Специфической профилактики (вакцин, сывороток) для заболевания не существует в связи с его генетической природой.
Пациенты с болезнью Вильсона — Коновалова, которые узнают о диагнозе в результате плановых обследований и не имеют заметных симптомов, не воспринимают медикаментозное лечение как обязательное. В таком случае стоит говорить не о истинной профилактике заболевания, а скорее о профилактике внешних проявлений (клиники) болезни Вильсона — Коновалова и просветительской работе [9] .
Профилактика заболевания включает:
- медико-генетическое консультирование;
- пренатальную (предродовую) диагностику;
- преимплантационную генетическую диагностику.
Скрининг у пациентов, имеющих необъяснимое повышение сывороточных аминотрансфераз, хронический гепатит, цирроз печени и неврологические нарушения неизвестного происхождения должен проводиться в возрасте от 2 до 18 лет. Все родственники по прямой линии больного с диагностированной болезнью должны проходить плановое обследование на наличие у них заболевания.
При беременности, когда имеется риск рождения пациента с болезнью Вильсона — Коновалова, проводится молекулярно-генетический анализ фетальных клеток на 15-18 неделе беременности или ворсинок хориона на 10-12 неделе.
Преимплантационная генетическая диагностика болезни Вильсона — Коновалова заключается в проведении ЭКО, возможности диагностики заболеваний до самого оплодотворения и последующей имплантации оплодотворенного эмбриона в организм женщины. Это может предотвратить зачатие ребенка с генетическими болезнями. Такой метод профилактики может быть выбором в ситуации, когда в семье уже определены мутантные гены, способные вызвать болезнь [1] [2] [3] [15] [17] .
Нарушения обмена меди (болезнь Вильсона) у детей
Болезнь Вильсона (БВ) (синонимы: болезнь Вильсона-Коновалова, гепатолентикулярная дегенерация, гепатоцеребральная дистрофия) — редкое тяжёлое наследственное мультисистемное заболевание, проявляющееся преимущественно печёночными, неврологическими и психиатрическими нарушениями вследствие чрезмерного отложения меди в органах и тканях [1]. Это заболевание относится к числу трудно диагностируемых в связи с длительным латентным течением и полиморфизмом клинической симптоматики. БВ может клинически манифестировать как в детском и подростковом, так и в более старшем возрасте. При отсутствии медь-элиминирующей терапии это заболевание является фатальным.
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем. связанных со здоровьем (МКБ-10)

Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
— 800 RUB / 5500 KZT / 27 BYN — 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место — 800 RUB / 5500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
Клиническая картина БВ характеризуется большим полиморфизмом в отношении как неврологических, так и соматических проявлений. Это нашло своё отражение в различных классификациях заболевания [26, 27]. В настоящее время чаще всего используется классификация БВ, в основе которой лежит клинико-патоморфологический принцип [28]. Выделяют следующие формы БВ.
- Бессимптомная форма (около 10% случаев): клинических проявлений нет, диагноз установлен до проявления симптомов,
- Абдоминальная (печёночная) форма (около 40 % случаев): раннее начало, преимущественно с острой печёночной недостаточности или признаков хронической печёночной недостаточности; фульминантная печёночная недостаточность, цирроз печени.
- Церебральная (неврологическая) форма (около 40-50 % случаев): характерны разнообразные экстрапирамидные нарушения (тремор конечностей и головы, дистония, мозжечковая атаксия, паркинсонизм, нарушение почерка, дизартрия, мышечная ригидность, хорея, атетоз), психические нарушения (депрессия, раздражительность, расторможенность поведения, психотические эпизоды),
- Смешанная форма: сочетание неврологических и печёночных проявлений.
Этиология и патогенез
БВ развивается при наличии у человека патогенных вариантов в компаунд-гетерозиготном (чаще) или гомозиготном (реже) состоянии в гене ATP7B, который располагается на длинном плече 13 хромосомы (13q14.3-q21.1) и состоит из 21 экзона и 20 интронов (общая геномная длина гена составляет около 80 тысяч пар оснований).
Ген АТР7В кодирует одноимённый медь-транспортирующий белок из группы АТФаз Р-типа, который располагается в транс-Гольджи аппарате, обеспечивает транспорт меди через мембраны органелл гепатоцитов, способствуя выведению её с жёлчью, а также включению в молекулу апоцерулоплазмина (церулоплазмин без меди) с образованием голоцерулоплазмина (церулоплазмин с 6 молекулами меди). Наиболее высокая экспрессия гена ATP7B наблюдается в печени, однако он также экспрессируется в почках, плаценте, молочных железах, головном мозге и лёгких.
Тип наследования БВ аутосомно-рецессивный. К настоящему времени в гене АТР7В описано более 700 патогенных вариантов [88], большая часть из которых являются миссенс, однако нонсенс, инсерции/делеции и мутации сайтов сплайсинга также встречаются [13, 14] Наиболее распространённым патогенным вариантом в гене АТР7В среди европеоидной расы является Н1069Q. Около 50-80% пациентов с БВ, проживающих в странах Центральной, Восточной и Северной Европы являются носителями по крайней мере одного аллеля с таким вариантом. По данным ряда исследователей, в России среди пациентов с подтверждённым диагнозом БВ доля больных с вариантом Н1069Q в гетерозиготном состоянии составляет 50 %, а доля пациентов с этим вариантом в гомозиготном состоянии — 26,3 % [17]. В настоящее время чётких корреляций между патогенными вариантами и фенотипами БВ неизвестно.
Медь по своему общему содержанию в теле человека занимает третье место среди переходных металлов, незаменимых для организма. Она выступает в роли кофактора и (или) структурного компонента для нескольких ферментов, участвует во многих физиологических процессах, включая энергетический обмен, антиоксидантную защиту и обмен железа. Физиологическая потребность в меди для взрослых составляет около 1,0 мг/сут, для детей в зависимости от возрастной группы — от 0,5 до 1,0 мг/сут [18]. В организм медь поступает в основном с пищей. Наиболее богаты медью печень, моллюски, крабы, креветки, устрицы, лобстеры, соевые бобы, шоколад, орехи, злаки. Среднее потребление меди у человека составляет 1,5-2,5 мг/сут. Верхний допустимый уровень потребления составляет 5 мг/сут. Всасыванию в проксимальных отделах тонкой кишки подвергается от 20 % (при потреблении более 5 мг/сут) до 50 % (при потреблении менее 1 мг/сут) меди, остальное экскретируется с фекальными массами. В крови всосавшаяся медь связывается с альбумином и транскупреином и
Снижение функции медь-транспортирующей АТФазы в результате патогенных вариантов в гене АТР7В в компаунд-гетерозиготном или гомозиготном состоянии приводит к нарушению гепатобилиарной экскреции меди и нарушению её встраивания в церулоплазмин. Поскольку период полужизни апоцерулоплазмина значительно короче такового у церулоплазмина, нагруженного медью (5 ч против 5,5 сут), при БВ, как правило, в крови наблюдется снижение содержания церулоплазмина. Вместе с тем примерно у трети пациентов с БВ уровень церулоплазмина в крови может быть в пределах нормальных значений. Необходимо отметить, что использование метода определения медь-зависимой оксидазной активности позволяет точнее определить содержания апоцерулоплазмина, в то время как иммунологические тесты могут завышать получаемые значения, т.к. не способны дифференцировать апо- и голоцерулоплазмин.
Основным следствием дефицита медь-транспортирующей АТФазы является накопление меди в различных органах и тканях: первоначально — в печени, а по мере прогрессирования заболевания и при отсутствии лечения, когда способность печени аккумулировать медь исчерпывается, — в головном мозге, роговице глаз и почках. Это обусловливает полиморфизм клинических появлений БВ. Накопление меди в паренхиматозных органах сопровождается снижением содержания общей меди в сыворотке, т.к. в норме около 90 % общей меди составляет медь, связанная с церулоплазмином.
Несмотря на важнейшую роль меди во многих физиологических процессах, её избыток является губительным для организма. Патогенные эффекты избытка меди в клетке опосредованы образованием свободных радикалов с развитием перекисного окисления липидов, повреждением белков, нуклеиновых кислот, митохондрий в сочетании с истощением антиоксидантных систем. Медь может также ингибировать функции многих белков, напрямую связываясь с их тиоловыми и аминогруппами. Кроме того, избыток меди активирует проапоптотические механизмы. Всё это в конечном счёте приводит к разрушению перегруженных медью клеток, преимущественно гепатоцитов. Лизис таких гепатоцитов обусловливает повышение содержания свободной меди в сыворотке и, следовательно, компенсаторному повышению её суточной экскреции с мочой и накоплению в других органах-мишенях [19]. Помимо этого, избыток свободной меди в сыворотке может приводить к гемолитическим кризам [4].
Эпидемиология
Болезнь Вильсона является редким (орфанным) заболеванием, хотя показатели распространённости варьируют в зависимости от исследования. По данным ряда исследований, её распространённость составляет около 1 случая на 7 000-10 000 населения, в то время как частота гетерозиготного носительства патогенных вариантов в АТР7В составляет около 1:40 [20, 21].
Наиболее часто указывается распространённость 1:30,000 [21, 22, 23, 24,140]. Более поздние исследования из Китая [141] и Франции [142] свидетельствуют о более низкой распространенности 1: 56,000 и 1:66,000, соответственно.
По данным анализа федерального регистра орфанных заболеваний, в России в 2014 и 2015 гг. было зарегистрировано всего 572 и 602 пациента с диагнозом БВ, что составило 0,39 и 0,41 на 100 000 населения соответственно (из них детей 16,9%) [25]. Реальная распространенность заболевания предполагается более высокой.
Клиническая картина
Cимптомы, течение
Клиническая картина БВ характеризуется многообразием симптомов и манифестирует в возрасте от 3 до 74 лет (средний возраст 13,2 года), однако до 5-летнего возраста развёрнутая симптоматика развивается редко [29,30,31].
Развёрнутая клиническая картина БВ обусловлена избыточным накоплением меди в различных органах и тканях и преимущественно проявляется симптомами поражения печени, центральной нервной системы, глаз, реже почек, костей, сердца, желёз внутренней секреции.
Неврологическая симптоматика БВ манифестирует позже, чем поражение печени, в большинстве случаев на втором-третьем десятилетии жизни, но может проявляться и в детском возрасте до 10 лет [32, 33]. Наиболее часто клиническая картина включает в себя дистонию (до 69 %), атаксию (до 30 %), постурально-кинетический и интенционный тремор (до 90 %), паркинсонизм (до 62 %), сопровождающиеся на более поздних стадиях слюнотечением, дизартрией и дисфагией; реже наблюдаются хорея (16 %), атетоз (14 %), эпилепсия (6 %) и др. [3,32,89].
Дистония при БВ может затрагивать разные части тела. По мере прогрессирования болезни в случае отсутствия лечения фокальная или сегментарная форма дистонии может переходить в генерализованную [89]. Паркинсонизм при БВ характеризуется брадикинезией, ригидностью и постуральной неустойчивостью, при этом эти явления нередко имеют симметричный характер [90]. Тремор является одним из частых неврологических проявлений БВ. Тремор может быть постуральным, интенционным, отмечаться в покое или иметь все перечисленные условия возникновения (тремор Холмса) [32]. Мозжечковая атаксия наблюдается почти у 30 % пациентов с БВ [91]. Дизартрия является наиболее частым неврологическим симптомом БВ. Основываясь на преобладающей характеристике нарушения речи, можно выделить несколько типов дизартрии при БВ, включая гипокинетическую, псевдобульбарную (спастическую), гиперкинетическую (дистоническую), атактическую и смешанную [34]. Дисфагия, определяемая как затруднение в любой фазе глотания, встречается примерно у 18% пациентов с ВД и у 50% пациентов с неврологическими симптомами [34, 90]. Может быть затронута любая фаза акта глотания, включая пероральный приём, приготовление/жевание, пероральный транзит и само глотание. Дисфагия может возникнуть из-за нарушения мышечного тонуса (например, при орофациальной дистонии), нарушения координации акта глотания, медлительности и слабости мышц. Слюнотечение относится к наиболее заметным и частым симптомам БВ и наблюдается примерно у 70 % пациентов с неврологическими проявлениями заболевания. Очень часто это является следствием дисфагии и (или) неспособности удерживать слюну во рту из-за орофациальной дистонии [34].
У детей ранние неврологические признаки болезни выражаются в поведенческих нарушениях, отставании в учёбе, проблемах при выполнении заданий, требующих сочетанной координации работы рук и глаз, ухудшении мелкой моторики, изменяется почерк.
Психиатрические проявления. Наряду с поведенческими нарушениями психиатрические проявления включают расторможенное поведение, депрессию, тревожность, психотические симптомы. У детей снижается успеваемость в школе, появляется лабильное настроение, неадекватное, агрессивное поведение. У большинства пациентов с неврологической и (или) психиатрической симптоматикой БВ развивается цирроз печени, длительно протекающий бессимптомно [4,31,34].
Симптомы поражения печени при БВ весьма вариабельны. У детей поражение печени развивается раньше, чем неврологическая симптоматика. Клинический дебют БВ может быть в виде фульминантного гепатита (чаще у детей и подростков), проявляющегося коагулопатией, энцефалопатией, Кумбс-негативной гемолитической анемией, печёночной и почечной недостаточностью [3,4,31]. Иногда клинические симптомы крайне напоминают картину острого вирусного гепатита. Этот вариант заболевания без проведения трансплантации печени приводит к практически 100 %-й летальности, поэтому таких пациентов необходимо незамедлительно включать в лист ожидания трансплантации печени.
Клиническая картина хронического гепатита при БВ мало отличима от поражения печени другого генеза и без патогенетической терапии приводит к формированию цирроза, что диктует необходимость исключения БВ у всех пациентов как с острым, так и с хроническим поражением печёночной паренхимы с наличием или без признаков цирроза. Характерной чертой хронического гепатита при БВ является умеренное повышение биохимических маркеров цитолиза, холестаза и уровня билирубина с высоким уровнем структурных изменений печёночной паренхимы при морфологическом исследовании биоптатов печени. БВ может клинически протекать по типу аутоиммунного гепатита с повышением сывороточных иммуноглобулинов и неспецифических аутоантител, в связи с чем у пациентов с аутоиммунным гепатитом при неэффективности кортикостероидной терапии следует также исключать БВ [31].
Поражение органа зрения. Патогномоничным симптомом БВ являются кольца Кайзера-Флейшера — отложение меди в десцеметовой мембране роговицы. У детей с бессимптомным и лёгким печёночным течением БВ они обьино не визуализируются [39]. Кольца Кайзера-Флейшера выявляются у 95 % пациентов с неврологическими симптомами и примерно у половины больных без неврологических нарушений [3]. Для их достоверного определения необходимо проводить осмотр при помощи щелевой лампы [40,92]. Следует учесть, что кольца Кайзера-Флейшера не всегда специфичны для БВ, и могут формироваться у пациентов с хроническими холестатическими заболеваниями или при холестазе новорождённых [41,42]. К другим возможным офтальмологическим проявлениям БВ относится передняя субкапсулярная катаракта (так называемая «медная катаракта») — она тоже выявляется при осмотре при помощи щелевой лампы.
Кумбс-негативная гемолитическая анемия у пациентов с БВ может протекать как единичный острый эпизод или иметь хронический характер. В ряде случаев это может быть единственным симптомом дебюта БВ. Пациенты, у которых в анамнезе отмечалась желтуха до установления диагноза БВ, скорее всего, перенесли ранее нераспознанный гемолиз.
Во время беременности у пациенток с БВ возможно развитие острого гепатита и гемолиза, что требует дифференциальной диагностики с HELLP-синдромом.
— дисфункция почечных канальцев: урикозурия, глюкозурия, аминоацидурия, протеинурия, почечный тубулярный ацидоз [35,36];
Источник https://www.krasotaimedicina.ru/diseases/zabolevanija_neurology/wilsons
Источник https://probolezny.ru/bolezn-vilsona-konovalova/
Источник https://diseases.medelement.com/disease/%D0%BD%D0%B0%D1%80%D1%83%D1%88%D0%B5%D0%BD%D0%B8%D1%8F-%D0%BE%D0%B1%D0%BC%D0%B5%D0%BD%D0%B0-%D0%BC%D0%B5%D0%B4%D0%B8-%D0%B1%D0%BE%D0%BB%D0%B5%D0%B7%D0%BD%D1%8C-%D0%B2%D0%B8%D0%BB%D1%8C%D1%81%D0%BE%D0%BD%D0%B0-%D1%83-%D0%B4%D0%B5%D1%82%D0%B5%D0%B9-%D0%BA%D1%80-%D1%80%D1%84-2021/17054