Гепатит С — симптомы и лечение
Что такое гепатит С? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 15 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Елена Бережная , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина
Определение болезни. Причины заболевания
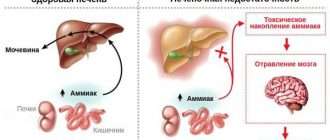
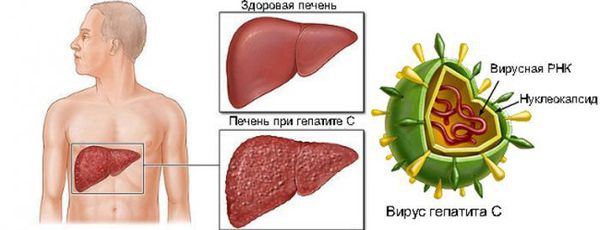
Вирусный гепатит С — острое или хроническое инфекционное заболевание, вызываемое различными типами вируса гепатита С, которые поражают в основном гепатоциты (клетки печени) и вызывают развитие воспалительного процесса в печени. При сочетании ряда факторов, образа жизни и отсутствии адекватного лечения вирусы гепатита С приводят к цирротической перестройке ткани и раку печени (гепатоцеллюлярной карциноме).
Краткое содержание статьи — в видео:
Этиологический агент — вирус гепатита С (ВГС). Вирус был впервые выделен американскими учёными в 1989 году.
Таксономическая структура:
- царство — вирусы
- семейство — Flaviviridae
- род — Hepacivirus
- вид — вирус гепатита С (hepatitis C virus, HCV) — 7 генотипов и 67 подтипов
Этиологические и морфологические свойства вируса
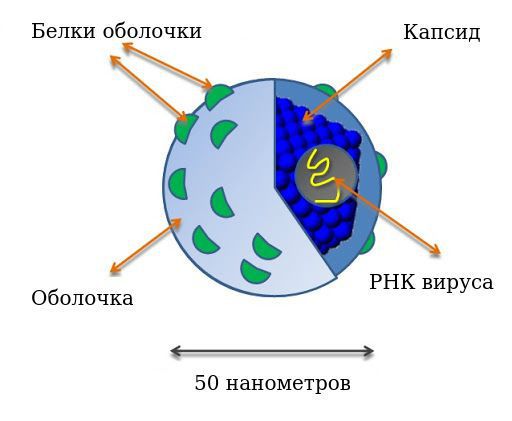
Диаметр вириона (вирусной частицы) — 50 нанометров. Имеет внешнюю белково-липидную оболочку. Оболочка вирусной частицы образуется в том числе за счёт взаимодействия вируса с липопротеидами низкой плотности хозяина, что позволяет ему ускользать из под иммунной атаки и проникать в клетки.
Генетическая структура представляет собой линейную однонитевую молекулу рибонуклеиновой кислоты (РНК), её размер примерно 9400 нуклеотидов. В ней выделяют следующие зоны: шифрующие структурные (Е1 и Е2 белки) и неструктурные (функциональные) белки — NS2, NS3, NS4A, NS4B, NS5A, NS5B, отвечающие за различные функции в жизни вируса. Структурные белки определяют прямой цитопатический эффект (повреждение клеток), полиморфизм (многообразие) вируса, участвуют в эффекте проникновения и выхода из клетки. Неструктурные белки участвуют в процессе развития и размножения вируса, определяют развитие резистентности (устойчивости) к интерферонам (NS5A). Встраивания вирусной РНК в геном клеток человека не замечено.
Вирус неоднороден (есть его различные подвиды — генотипы). Это обусловлено тем, что скорость его репликации огромна (за сутки 10 11 -10 12 ) и в результате возникает большое число ошибок — вирус быстро мутирует. Такие мутации позволяют вирусу ускользать от иммунного ответа человека и длительно находиться в организме, а также сопротивляться воздействию лекарственных препаратов. Основной резервуар вируса — это клетки печени, однако он способен размножаться и в клетках иммунной системы (макрофагах, моноцитах и др.).
В целом вирус малоустойчив в окружающей среде. Под воздействием хлороформа, спирта, хлоргексидина и других дезинфицирующих средств погибает практически мгновенно, инактивируется при температуре 100 °С за 2 минуты, при температуре 60 °С за 30 минут. При комнатной температуре живёт не более четырёх суток, под действием ультрафиолета погибает за 30 минут. В плазме, эритроцитарной массе и др. может сохраняться до года. На культурах клеток не культивируется, не имеет гемагглютинирующей (склеивающей эритроциты) и гемолитической (разрушающей эритроциты) активности [2] [8] [10] [11] .
Передача вируса гепатита С
Передача вируса осуществляется только через кровь. Инфицирующая доза в несколько десятков раз больше, чем при гепатите В, т. е. для заражения нужны видимые следы крови. А вот пути заражения бывают различны:
- употребление наркотиков;
- медицинские манипуляции (в том числе пирсинг, тату и др.);
- половой путь (незащищённый половой контакт, в среднем около 1,5 % в гетеросексуальной семье);
- от матери к ребёнку в родах;
- бытовой путь (использование общих бритв, ножниц, зубных щёток).
При поцелуях, рукопожатиях, через посуду, сухие пятна крови на одежде, через воду, при кашле, чихании, потении, сидении рядом, по воздуху и т. д. гепатит С не передаётся. Заразиться через грудное молоко также нельзя, но заражение возможно при попадании крови матери на повреждённые губы ребёнка. Есть незначительный риск при попадании инфицированной крови в глаза, однако это единичные случаи. Заразиться при переливании крови практически невозможно, т. к. кров ь на гепатит С тестируют методом ПЦР (полимеразной цепной реакции) с высокой чувствительностью.
Нет никаких научных оснований ограничивать выбор профессии, работы и круг общения людей с гепатитом С — передача осуществляется только через кровь, поэтому ограничений в работе (например учителем, врачом, няней), контактах с родственниками и т. п. быть не должно.
Территориальное распределение
Гепатит С распространен во всем мире. Наиболее часто он встречается в Регионе ВОЗ Восточного Средиземноморья и Европейском регионе ВОЗ, где в 2015 г. распространенность HCV, по оценкам, составила соответственно 2,3% и 1,5%. Общее количество больных вирусным гепатитом С в мире не менее 150 млн, в Российской Федерации — неизвестно (по некоторым данным ориентировочное количество больных — не менее 2 млн человек). По состоянию на 2016 год в США было заражено не менее 2,4 млн человек (по другим данным — не менее 4 млн). По самым скромным подсчётам в этой стране в 2018 году от гепатита С умерли не менее 15 тыс. человек. В РФ превалирующее распространение имеют генотипы 1b и За, но частота их выявления может значительно колебаться в зависимости от региона [4] [7] [9] .
В настоящее время вирусный гепатит С распространяется в общей популяции, т. е. заболеванию подвержены люди всех возрастов и социальных слоёв, однако наибольший риск имеют следующие категории:
- потребители инъекционных наркотиков;
- ВИЧ-инфицированные;
- пациенты отделений гемодиализа;
- лица, подвергшиеся трансплантации органов (в настоящее время менее значимо);
- медработники;
- дети, рождённые от матерей с гепатитом С;
- маргинальные слои общества, работники секс-индустрии.
После перенесённого острого вирусного гепатита С примерно 30 % людей самоизлечиваются, т. е. полностью избавляются от вируса, в остальных случаях формируется хронический гепатит. Предикторы (прогностические параметры) самоизлечения — желтуха, высокий уровень АЛТ, молодой возраст, женский пол, 1 генотип вируса, наличие гепатита В с HbsAg (антигеном вируса гепатита В). У каждого 5-25 человека из 100 в течение 10-20 лет от момента инфицирования при хронизации развивается цирроз печени и у них имеется 1-4 % годовой вероятности развития рака печени.
Провоцирующие факторы развития цирроза печени:
- мужской пол;
- возраст более 50 лет;
- злоупотребление алкоголем;
- коинфекция ВИЧ, гепатита В или стеатогепатита;
- иммуносупрессивная терапия.
Гепатитом С можно заразиться после выздоровления от предыдущего случая (даже тем же генотипом), можно заразиться другим генотипом, даже если человек уже имеет гепатит С какого-либо генотипа (суперинфекция). В этом случае наблюдается борьба между генотипами за доминирование. Побеждает, как правило, какой-то один, а другой может сохраняться на минимальных степенях репликации. При этом существует риск ошибки при определении генотипа.
Иммуногенность вируса слабая, т. е. антитела, которые должны вырабатываться в ответ на заражение, появляются медленно (не ранее чем через 3 недели от заражения) и не обладают явным вируснейтрализующим действием [2] [4] [8] [9] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы гепатита С
Скрытый (инкубационный) период гепатита С может составлять от 2 недель до 6 месяцев. В это время может не быть никаких признаков заражения и развивающегося заболевания. Однако коварство гепатита С в том, что даже по прошествии этого времени может не возникнуть никаких явных симптомов и проявлений (большинство больных вообще не имеет симптомов или их нельзя связать с гепатитом). Даже если симптомы и возникают, то зачастую они настолько незначительны, что человек абсолютно не придаёт им значения и не обращается за медицинской помощью до развития осложнений. Чаще всего информация о болезни появляется после прохождения рутинных исследований для операции или донорства крови.
Симптомы вирусного гепатита С в остром и хроническом периоде:
- снижение или отсутствие аппетита;
- общая слабость, ухудшение самочувствия, повышенная утомляемость, депрессия (один из основных симптомов);
- тошнота;
- тяжесть и дискомфорт в правом подреберье;
- боли в животе, небольшое расстройство пищеварения;
- боли в суставах;
- в редких случаях — пожелтение склер глаз, кожи, потемнение мочи или осветление кала.
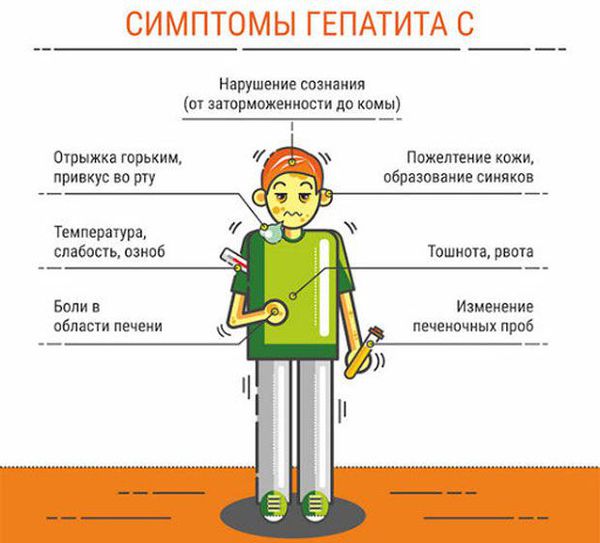
Повышение температуры отмечается редко. Возможен различный характер течения хронического заболевания, в большинстве случаев на протяжении десятков лет больной испытывает незначительную усталость, периодический дискомфорт в правом подреберье, иногда связанный с погрешностями в диете. Примечательно, что чёткого продолжительного периода ухудшения самочувствия обычно нет. Лишь на завершающей стадии заболевания (через несколько десятков лет) человек испытывает резкое ухудшение самочувствия, нарастание отёков, в том числе у него наблюдается накопление жидкости в брюшной полости (асцит), повышенная кровоточивость, похудание, желтуха. Зачастую толчком к этому служит принятие алкоголя на праздники в значительных дозах. В этом коварство вирусного гепатита С — мнимый период благополучия даже при высокоактивном инфекционном процессе («ласковый убийца», как длительное время его называли).
Гепатит С у беременных
Каких-либо значимых различий в течении вирусного гепатита С при беременности нет, как правило, происходит даже минимизация клинических и лабораторных изменений. Риск заражения ребёнка имеется лишь в родах, причём чем выше количество вируса в мл крови (вирусная нагрузка), тем выше риск. Выбор способа родоразрешения может влиять на риск передачи вируса при высокой вирусной нагрузке (свыше 8 х 10^5 МЕ/мл): при естественных родах риск до 8 %, при плановом кесаревом сечении — до 1 % (некоторые исследователи не подтверждают это). При коинфекции ВИЧ у матери риск передачи значительно возрастает — до 15 %.
Гепатит С у детей
После рождения от матерей с гепатитом С у 100 % детей выявляются материнские антитела к вирусу до 18 месяцев в максимальном исчислении (это нормально). Если заражения не произошло, в течение этого срока антитела исчезают и у ребёнка больше не будет никаких следов контакта. Если происходит заражение, то уже через 1-2 месяца в крови будет выявляться вирусная РНК в ПЦР исследовании (требует повторения даже при первичном отрицательном результате). Как правило, течение гепатита у детей малоактивное и не приводит к выраженным изменениям печени и самочувствия до момента возможного современного лечения и выражается только периодическим повышением АЛТ/АСТ [2] [3] [8] [9] .
Патогенез гепатита С
Проникая в организм, вирус гепатита С не оставляет никаких следов в месте внедрения. С током крови он быстро попадает в клетки печени, где оказывает неярко выраженное прямое разрушающее действие на клетки-мишени и в большей степени вызывает иммуноопосредованное поражение клеток на фоне репликации вируса. При использовании одного из исследований — ультрачувствительного ПЦР (полимеразной цепной реакции) — РНК вируса в крови может обнаруживаться уже через 2 недели от момента заражения. Значений, которые выявляются всеми тест-системами, как правило, вирусная нагрузка достигает через 1,5 месяца после заражения.
Нарушается баланс продукции цитокинов (белков, которые оказывают комплексное регулирующее влияние на воспаление и иммунитет):
- усиливается выработка интерлейкинов IL-4 и IL-10 (сигнальных веществ, которые вырабатываются клетками иммунной системы и служат для регуляции активности других клеток);
- снижается образование интерферонов IL-2 (белков с противовирусной и иммуномодулирующей активностью);
- подавляется активация СD4+ лимфоцитов (клеток, которые отражают работу иммунной системы).
Возможность нахождения и размножения вируса в клетках иммунной и нервной систем делает его недоступным для иммунного контроля. Главенствующая частота перехода вирусного гепатита С в хроническую форму (около 70 %) обусловлена не только различными особенностями самого вируса, но и обязательным участием (или вернее неадекватным участием) иммунной системы:
- наличием внепечёночного размножения вируса (главным образом в моноцитарной системе);
- наличием множества генотипов с подтипами и частыми мутациями (перестановками составляющих генома вируса);
- запуском иммунопатологических реакций, которые участвуют и во внепечёночных поражениях при гепатите С, в том числе в клетках эндотелия сосудов головного мозга;
- низкой иммуногенностью вируса;
- участием в патогенезе процессов перекисного окисления липидов.
После заражения и малосимптомного протекания острой фазы заболевания при отсутствии самоизлечения (около 30 %) наступает хронизация инфекции — длительный латентный период (до 10-30 лет, иногда более длительно). В течение этого периода человек ведёт обычный образ жизни, не испытывает никаких явных признаков заболевания, а появляющееся чувство усталости вполне логично списывает на интенсивный современный ритм жизни.
Длительность латентного периода зависит от свойств вируса, его реактивности, развития иммунопатологических реакций иммунной системы, образа жизни человека и других факторов. Однако рано или поздно наступает переломный момент в системе взаимодействия патогенного микроорганизма и восприимчивого человеческого макроорганизма. Несмотря на широкие регенераторные возможности печени происходит нарушение её восстановительных сил. Вследствие постоянного некупируемого воспалительного процесса активная функциональная ткань печени замещается жировой и далее соединительной тканью (рубцовой). При этом нарушается нормальное функционирование органа и по механизму обратной связи происходит прогрессирующее ухудшение работы печени и жизнедеятельности организма в целом [2] [4] [10] [11] .
Классификация и стадии развития гепатита С
Острый вирусный гепатит С
Периоды:
- Инкубационный период — от 3 недель до 4-6 месяцев. Полное отсутствие симптоматики.
- Преджелтушный (продромальный) период — от 4 суток до 3 недель. Симптомы малозаметны, может быть депрессивное настроение, слабость, дискомфорт в животе, неустойчивый стул.
- Период паренхиматозного гепатита (желтушный) — от 1 до 3 недель. Бывает редко, чаще отмечается незначительное желтушное окрашивание склер в совокупности с предыдущими признаками.
- Период выздоровления (реконвалесценции) или переход в малоактивное хроническое течение — от 3 до 6 месяцев.
По (МКБ-10): B17.1 Острый гепатит С.
По клинической форме:
- Манифестная:
- желтушная (типичная);
- безжелтушная.
- Бессимптомная:
- субклиническая (симптомы выражены очень слабо);
- инаппарантная (симптомов нет, возможны лишь лабораторные изменения).
По степени тяжести:
- Лёгкая — незначительная интоксикация до 5 дней, отсутствие или незначительная желтушность до 7 дней, отсутствие лихорадки, нормальные или незначительно увеличенные размеры печени, общий билирубин до 85-100 мкмоль/л, протромбиновый индекс (ПТИ) до 80 %, АЛТ до 500 ед/л.
- Средней тяжести — умеренная интоксикация до 7 дней, умеренная желтушность до 10 дней, субфебрилитет (повышение температуры тела в пределах от 37,1 до 38,0 °С) в начальном периоде до 5 дней, увеличение печени до 4 см, общий билирубин 100-170 мкмоль/л, ПТИ 80-60 %, АЛТ до 1000 ед/л.
- Тяжёлая — резко выраженная интоксикация 15 и более дней, интенсивная желтушность кожи 3 недели и более, фебрильная температура весь начальный и период разгара болезни, тахикардия, увеличение печени на 6 см и резкое её уменьшение в размерах на фоне прогресса болезни, общий билирубин от 170 мкмоль/л, ПТИ менее 60 %, АЛТ более 1000 ед/л.
По длительности течения:
- острый гепатит С (циклический — до 3 месяцев, острый затяжной — 3-6 месяцев);
- хронический гепатит С — продолжительностью более 6 месяцев.
Классификации хронических форм не разработаны, могут применяться различные составляющие на основании выраженности цитолитического синдрома, уровня повышения печёночных ферментов, морфологических изменений печени, наличию осложнений и др. [2] [10] [11] .
Осложнения гепатита С
В остром периоде гепатита С возможно развитие «печёночной комы» — резкого выраженного угнетения функции печени вследствие массивной гибели печёночных клеток и накопления в организме токсичных продуктов обмена различных веществ. Это состояние характеризуется заторможенностью, потерей сознания, нарушением витальных (жизненно важных) функций. Однако встречаемость данного осложнения крайне низкая.
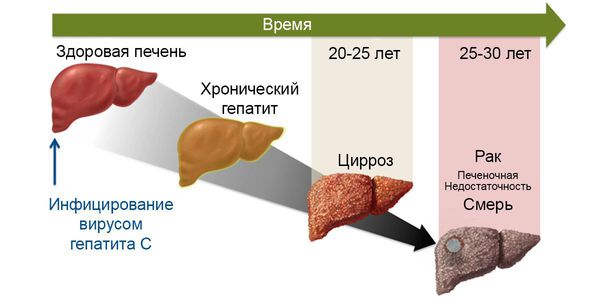
В хронической фазе болезни (или, по мнению части исследователей, конечной фазе заболевания) наиболее частым осложнением является развитие цирроза печени — замещения функционального долькового строения печёночной ткани грубым соединительнотканным образованием, что приводит к неадекватному функционированию органа. Определённое время печень способна выполнять функцию даже на стадии цирроза, но со временем при воздействии вируса наступает декомпенсация работы. Это состояние характеризуется нарушением кровотока в печени, повышением давления в системе воротной вены, расширением вен пищевода и желудка, увеличением селезёночной вены. Прогрессивно снижается уровень выработки белков, факторов свёртывания крови, фильтрационная способность. Появляются отёки, асцит (скопление жидкости в брюшной полости), кровотечения различной интенсивности, ухудшается общее состояние, интеллектуально-мнестические характеристики. В конечном итоге возможен летальный исход из-за массивного кровотечения и полиорганной недостаточности.
Не менее значимое осложнение хронической фазы гепатита С — развитие гепатоцеллюлярной карциномы (опухолевое перерождение). Согласно основной гипотезе, злокачественное перерождение возникает в результате повышенного распада клеток печени и последующего их восстановления, что приводит к повышенному числу мутаций. На ранних стадиях принципиальных отличий от течения хронического гепатита нет, в запущенных случаях возникает стремительное ухудшение состояния, нарастание асцита, желтухи, неспецифических желудочно-кишечных симптомов, потери веса, анорексии.
У 10-15 % больных с хроническим вирусным гепатитом С возможно развитие аутоиммунных заболеваний, наиболее частыми из которых являются аутоиммунный гепатит (АИГ) и криоглобулинемия. АИГ — это иммуноопосредованное поражение печени. Внешне оно мало отличается от проявлений гепатитов другой этиологии, но зачастую имеет более агрессивное течение и поддаётся терапии только длительными курсами иммуносупрессивных препаратов. Криоглобулинемия — накопление в малых и средних кровеносных сосудах специфических белков, которые вызывают затруднение в них тока крови и приводят к специфическим проявлениям.
Также определена связь гепатита С с развитием сахарного диабета, неходжкинской лимфомы и кожной порфирии Тарда [2] [8] [9] [10] .
Диагностика гепатита С
Вариантов первичного выявления вируса и заболевания множество, однако чаще всего гепатит С выявляется в ходе планового обследования при сопутствующем заболевании (операции или госпитализации). Как правило, обнаруживают повышенный уровень АЛТ или антитела к гепатиту С (HCVAb). Это служит поводом для направления такого пациента к врачу-инфекционисту для углублённого обследования.
На приёме врач-инфекционист (гепатолог) осматривает пациента, в части случаев (в различных сочетаниях) выявляет характерное изменение цвета ладоней (печёночные ладони), увеличение размеров печени. В продвинутых случаях заболевания врач отмечает расширение вен области передней брюшной стенки («голова медузы»), отёчность (в том числе асцит как причина увеличения размеров живота), сосудистые звездочки и др.
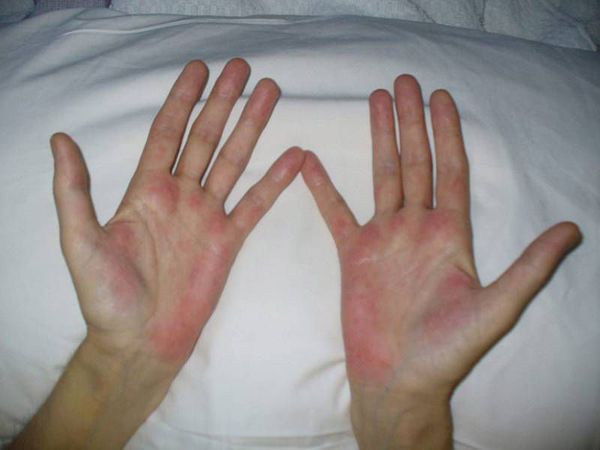
Прохождение тестирования на гепатит С
При лабораторном обследовании в первую очередь должно быть назначено исследование на АЛТ, РНК вируса методом ПЦР качественно с чувствительностью 15-60 МЕ и антитела к вирусу гепатита С суммарные. При отрицательном результате ПЦР и положительном анализе на антитела диагноз гепатита С не подтверждается. Согласно действующему в РФ законодательству, такой человек должен быть поставлен на учёт к инфекционисту на срок 2 года с обязательным обследованием методом ПЦР раз в 6 месяцев. При отрицательном результате наблюдение прекращается с диагнозом паст-инфекция гепатита С (выздоровление). При положительном результате ПЦР происходит подтверждение диагноза — острый или хронический вирусный гепатит С — и назначается дополнительное обследование в целях уточнения текущего состояния. Необходимо помнить, что выявление суммарных антител в иммуноферментном анализе (ИФА) говорит лишь о прошлой встрече с инфекцией и не даёт практически никакой информации о наличии заболевания в текущий момент. Антитела могут сохраняться пожизненно.
Обязательно должны быть назначены следующие исследования:
- Развернутый клинический анализ крови + СОЭ (скорость оседания эритроцитов). Для гепатита С характерны: лейкопения (снижение количества лейкоцитов), лимфо- и моноцитоз (увеличение числа лимфоцитов и моноцитов), уменьшение СОЭ, тромбоцитопения (снижение количества тромбоцитов);
- Биохимический анализ крови:
- аланинаминотрансферраза (АЛТ) — возможен нормальный уровень или периодическое повышение;
- аспартатаминотрансферраза (АСТ) — норма или повышение;
- гамма-глутамилтранспептидаза (ГГТ) — норма или повышение;
- щелочная фосфатаза (ЩФ) — повышение при ухудшении процесса;
- общий билирубин — норма или повышение;
- общий белок — снижение при нарушении функции печени;
- протеинограмма — повышение гамма-глобулинов;
- протромбиновый индекс (ПТИ) — снижение при прогрессировании процесса;
- креатинин, амилаза, сахар.
- Онкомаркеры. Альфафетопротеин — повышение при прогрессировании процесса и развитии рака печени.
- Общий анализ мочи — появление уробилина, белка.
- УЗИ органов брюшной полости — возможно увеличение размеров печени и селезёнки, изменение структуры печени, размера внутренних сосудов.
- ФГДС — исследование пищевода, желудка и двенадцатиперстной кишки. Выявляется расширение вен пищевода при развитии портальной гипертензии — осложнение цирроза печени.
- Фиброскан — метод оценки фиброза печени, который позволяет определить тяжесть заболевания без биопсии (F0 – отсутствие фиброза, F4 — цирроз).
- ПЦР на гепатите С — качественный и при необходимости количественный тест.
- Генотипирование — определение генотипа вируса гепатита С.
- Мутации лекарственной резистентности NS3, NS5A и NS5B регионов генома вируса гепатита С (при неудаче в лечении препаратами прямого действия или высоком риске такой неудачи до лечения).
- Анализы на маркеры сопутствующих вирусных гепатитов (HbsAg, HbcorAb total, anti-Hbs).
- Анализ на ВИЧ.
При необходимости список исследований может расширяться. Стоит подчеркнуть, что грамотное назначение обследования и его интерпретация возможны исключительно врачом-инфекционистом (гепатологом). Врач назначит лишь необходимое, тем самым поможет пациенту сэкономить деньги, даст грамотную оценку полученных данных, что чрезвычайно важно в планировании дальнейшего лечения и его исхода [2] [5] [6] [9] [12] .
Дифференциальная диагностика
- Вирусные и невирусные гепатиты другой этиологии. Связаны с путешествиями, любыми повреждениями кожи и слизистых, употреблением заражённых пищи и воды. Отличаются выраженностью симптоматики. Для уточнения диагноза проводятся специфические серологические тесты ИФА и ПЦР.
- Токсическое поражение печени. Связано с недавним значительным употреблением алкоголя или токсинов. Проводятся специфические серологические тесты ИФА и ПЦР, выявляется чрезмерное повышение ГГТ (фермент, маркер поражения печени).
- Паразитарные заболевания печени (например описторхоз, эхинококкоз). Связаны с проживанием в эндемичном регионе, употреблением плохо приготовленной рыбы, контактом с собаками. Характеризуются выраженной эозинофилией (увеличением уровня эозинофилов) периферической крови. Проводятся специфические серологические тесты, выявление яиц паразитов, инструментальные исследования.
- Первичный или метастатический рак печени. Изучаются данные анамнеза о сопутствующих заболеваниях, учитываются результаты инструментальной и лабораторной диагностики [2][4][10][11] .
Надо ли проверяться на гепатит С здоровому человеку
Регулярное обследование на гепатит С при отсутствии симптомов следует проводить медработникам, пациентам отделений гемодиализа, частым посетителям стоматолога, больным хроническими заболеваниями с частыми парентеральными вмешательствами (внутривенно, подкожно и внутримышечно) и лицам, часто меняющим половых партнёров.
Лечение гепатита С
Основу любого лечебного воздействия составляет правильно подобранная диета. В отношении вируса гепатита С этот метод как никогда актуален, однако он зачастую игнорируется как пациентами, так и самими врачами.
Диета при гепатите С
Самое главное условие — полный отказ от алкоголя. Ничто так не вредит печени, как алкоголь. Именно он может стать тем фактором, который запускает цепь патологических реакций и переводит гепатит из вялотекущего процесса в высокоактивный, ускоряя наступление цирротической стадии гепатита. В отношении других продуктов питания и напитков следует соблюдать золотую середину: питание должно быть разнообразным, всего должно быть в меру, без злоупотреблений «тяжёлой» пищей (ограничение жирного, жареного, солёного, копчёного) с учётом отсутствия или наличия сопутствующих заболеваний.
Большое значение имеет поддержание разумной физической активности и контроль веса (индекс массы тела не должен превышать 25 кг/м 2 ).
Какие врачи лечат гепатит С
Лечением гепатита С занимаются врачи-инфекционисты.
Медикаментозная терапия Гепатита С
Медикаментозное лечение гепатита С зависит от фазы развития заболевания, индивидуальных особенностей и возможностей организма. В остром периоде широко применяется инфузионная терапия (введение растворов) с привлечением различных дезинтоксикационных (очищение организма от вредных веществ) и питательных лечебных растворов.
Роль специфической противовирусной терапии острого гепатита С окончательно не решена и возможна лишь в индивидуальном порядке, например при угрозе хронизации или при фульминантном течении болезни (тяжёлом варианте воспалительно-некротического поражения печени). При невозможности радикального лечения гепатита С в хронической фазе вполне приемлема поддерживающая терапия так называемой группой гепатопротекторов (фосфолипиды, аминокислоты, антиоксиданты и др.). Данные средства не имеют чётко доказанной эффективности, однако широко применяются на практике и в некоторых случаях способны несколько задержать прогрессирование заболевания. Хороший эффект даёт нормализация функции ЖКТ и улучшение микрофлоры кишечника.
Попытки воздействия на вирус предпринимались с момента его открытия. Вначале это было изолированное применение препаратов интерферона короткого действия, затем комбинации интерферона короткого действия и рибавирина (препарата общевирусного действия). Их сменила комбинация интерферона пролонгированного действия и рибавирина.
К концу интерфероновой эпохи были достигнуты значительные успехи в процессе лечения и избавления человеческого организма от вируса гепатита С. Однако терапия была длительной, процент излечения достигал не более 70 % в среднем по генотипам, и курс лечения имел серьёзные побочные эффекты, иногда приводя к последствиям намного серьёзнее, чем сам гепатит С. Это обстоятельство дало толчок к разработке принципиально новых лекарственных средств, характеризующихся прямым противовирусным действием, сочетающих высокую эффективность (до 99 %), высокий профиль безопасности (минимальные побочные эффекты), простоту и удобство дозирования и небольшую длительность (2-3 месяца). В основу механизма действия легло подавление ключевых этапов размножения вируса, в первую очередь протеазы и полимеразы вируса гепатита С. Проведённые испытания препаратов показали высокие результаты, и, начиная с 2013 года, данная группа последних эффективных разработок с успехом применяется во всём мире. В некоторых странах одобрено лечение детей современными препаратами начиная с 3 лет (в зависимости от генотипа) с соответствующими взрослым показателями успеха.
Можно ли вылечить гепатит С полностью
В 2016 году Всемирная организация здравоохранения (ВОЗ) объявила гепатит С полностью излечимым заболеванием.
На 2020 год в мире доступны следующие виды и комбинации лекарственных препаратов прямого противовирусного действия для лечения гепатита С:
- Софосбувир.
- Даклатасвир.
- Элбасвир и Гразопревир.
- Глекапревир и Пибрентасвир.
- Ледипасвир и Софосбувир.
- Омбитасвир / Паритапревир / Ритонавир.
- Омбитасвир / Паритапревир / Питонавир / Дасабувир.
- Симепревир.
- Софосбувир и Велпатасвир.
- Софосбувир / Велпатасвир / Воксилапревир (комбинация не зарегистрирована в РФ).
Как лечить гепатит С в домашних условиях
Назначение противовирусной терапии должно осуществляться врачом, хорошо ориентирующимся в множестве применяемых для терапии гепатита С лекарств, после изучения всех составляющих процесса, возможных противопоказаний, взаимодействий с уже принимаемыми препаратами, особенностей диеты и образа жизни [1] [5] [8] [9] . Гепатит С — тяжёлое инфекционное заболевание, которое может привести к циррозу и раку печени, поэтому самолечение опасно для жизни.
Схемы лечения гепатита С в России
В России на сегодняшний день для лечения гепатита С используется преимущественно устаревшее лечение интерферонами (чаще бесплатно или со скидкой), в редких случаях — препаратами прямого противовирусного действия (чаще платно со скидкой).
Прогноз. Профилактика
Если лечение гепатита начать до того, как разовьётся цирроз печени, то прогноз будет благоприятным: как правило, наступает полное излечение. При запущенных стадиях (цирроз и рак печени) прогноз зависит от множества факторов, обычно при начальном циррозе больные при должном лечении могут жить дальше без каких-либо серьёзных проблем со здоровьем, при декомпенсированном процессе прогноз неблагоприятный.
Прогноз при отсутствии лечения гепатита С
В среднем без лечения при отсутствии пагубных привычек и здоровом образе жизни в течение 20 лет примерно у 10-20 % больных разовьются цирроз и рак печени, при регулярном злоупотреблении алкоголем, наркотиками и токсинами (в том числе лекарствами) доля таких тяжёлых осложнений составит до 30-40%.
Из-за повышенной мутационной способности вируса существует ряд технических сложностей в создании вакцины — на данный момент её не существует (ведутся разработки). Поэтому меры профилактики распространения вируса гепатита С направлены на разрывы механизмов и путей передачи вируса, санитарное информирование и обучение населения.
Первичная профилактика
- Предупреждение возможности заражения в медицинских учреждениях:
- гигиена и обработка рук, инструментария, использование перчаток;
- тестирование донорской крови, плазмы и компонентов;
- тестирование донорских органов;
- надлежащее проведение медицинских инъекций;
- обучение медицинского персонала;
- обследование доноров, беременных, госпитализированных.
- Предупреждение полового пути заражения
- обучение правильному и своевременному использованию презервативов;
- тестирование перед вступлением в брак.
- Выдача стерильного инструментария потребителям инъекционных наркотиков (не во всех странах).
Вторичная профилактика
- Проведение противовирусной терапии (в идеале при выявлении заболевания, т. к. это предупреждает дальнейшее распространение инфекции).
- Матерям с гепатитом С (если он не был пролечен до беременности) следует внимательно следить за состоянием целостности кожи сосков и рта ребёнка, при наличии повреждений необходимо прекращать грудное вскармливание на время до их заживления [2][7][9][12] .
Что делать, если член семьи болен гепатитом С
Самое важное, что следует сделать, чтобы предотвратить заражение вирусом — это избегать контакта с кровью инфицированного человека. Кровь может быть заразной, даже если она сухая. Надевайте перчатки, если вам нужно прикасаться к использованным бинтам. После контакта с кровью тщательно вымойте руки, даже если вы были в перчатках.
Некоторые предметы личной гигиены могут иногда содержать небольшое количество крови. Не следует совместно использовать зубную щётку, бритву или маникюрные ножницы.
Деятельность ВОЗ
В мае 2016 г. Всемирная ассамблея здравоохранения приняла первую «Глобальную стратегию сектора здравоохранения по вирусному гепатиту на 2016–2021 гг. Главной целью стратегии является снижение к 2030 г. числа новых случаев инфицирования вирусным гепатитом на 90 % и смертности от вирусного гепатита на 65 %. Для реализации этой стратегии ВОЗ занимается повышением осведомлённости о заболевании и его профилактике и расширяет охват услугами по скринингу, оказанию помощи и лечению гепатита С [13] .
Хронический вирусный гепатит С у взрослых
Хронический вирусный гепатит С (ХВГС) – хроническое воспалительное заболевание в течение более 6 месяцев с преимущественным поражением ткани печени вследствие инфицирования вирусом гепатита С (ВГС или HСV – hepatitis С virus), которое может привести к тяжелым последствиям – циррозу (ЦП), раку печени (гепатоцеллюлярной карциноме, ГЦК) и летальному исходу [1].
Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
Применявшийся ранее код Z22.5 для носителей вирусного гепатита был исключен из последнего пересмотра МКБ 10.

Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
— 800 RUB / 5500 KZT / 27 BYN — 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место — 800 RUB / 5500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
Заболевание классифицируют в зависимости от ГТ ВГС, а также наличия ЦП и внепеченочных проявлений.
4 – тяжелый фиброз.
Этиология и патогенез
Возбудителем ХВГС является ВГС, который представляет собой небольшой гепатотропный РНК-вирус из семейства Flaviviridae. Вирус состоит из нуклеокапсида, состоящего из сердцевинного (ядерного) белка (HCVcAg) и одноцепочечной (+) РНК, и белково-липидной оболочки, содержащей аполипопротеин Е (апоЕ) человека и вирусные белки Е1 и Е2. Вирусный геном кодирует 10 различных белков, среди которых 3 описанных выше структурных и 7 неструктурных (p7, NS2, NS3, NS4A, NS4B, NS5A и NS5B) [2].
Выделяют 8 генотипов (ГТ) [3], которые обозначаются арабскими цифрами от 1 до 8, и несколько десятков субтипов ВГС, которые обозначаются латинскими буквами. Наибольшее клиническое значение имеют субтипы ГТ 1: а и b. Генотипы и субтипы различаются в последовательностях приблизительно на 30% и 20% соответственно. Вариабельность генома вируса обусловливает изменения в строении антигенных детерминант, которые определяют выработку специфических антител. Это препятствует элиминации вируса из организма и созданию эффективной вакцины против ВГС [4,5].
Инфицирование ВГС в большей доле случаев (55-85%) приводит к хроническому течению заболевания и примерно у четверти больных приводит в течение последующих десятилетий к развитию ЦП, что, в свою очередь, может служить основой для формирования ГЦК [6]. Довольно часто ввиду преимущественного бессимптомного течения инфекции заболевание впервые проявляется осложнениями ЦП.
Ведущим патогенетическим механизмом при ХВГС является нарушение взаимодействия иммунных клеток с инфицированными ВГС гепатоцитами. Повреждение печеночной ткани в большей степени является результатом реализации иммунного ответа в очаге воспаления, а не цитопатического действия вируса [7]. В печени накапливаются иммунокомпетентные клетки, часть из которых (NK-клетки, цитотоксические T-лимфоциты) обладают высокой цитотоксичностью и способностью повреждать гепатоциты [8]. В результате контакта инфицированных гепатоцитов с CTL-лимфоцитами (компонента адаптивного иммунного ответа) происходит запуск апоптоза. Отмечается дефицит Т-системы, депрессия макрофагов, ослабление системы интерфероногенеза, отсутствие специфического антителогенеза в отношении антигенов вирусов, что в конечном итоге нарушает адекватное распознавание и элиминацию иммунной системой антигенов вирусов на поверхности гепатоцитов [8-11].
У больных с выраженным Т-клеточным ответом происходит полная элиминация ВГС после перенесенного острого гепатита С. Вследствие взаимодействия вируса и иммунной системы происходит угнетение активности CTL-лимфоцитов белками вируса. В результате этого при ХВГС формируется иммунологическая толерантность к вирусу [12].
Действие вируса при ХВГС и вызванные им иммунологические реакции обусловливают не только повреждение печени, но и других органов и тканей. Концепция системных поражений при ХВГС заключается в возможности репликации вируса вне печени, а именно в тканях лимфоидного и нелимфоидного происхождения [13]. Размножение вируса в иммунокомпетентных клетках (лимфоцитах) приводит к нарушению их иммунологической функции. Сохранение ВГС в моноцитах является основной причиной реинфекции после трансплантации печени у больных тяжелыми формами ХВГС [10].
Среди факторов хозяина, влияющих на исход и течение ХВГС, имеет значение возраст на момент инфицирования, злоупотребление алкоголем, коинфицирование гепатотропными вирусами, нарушения липидного обмена и др. [14,15].
Эпидемиология
По оценочным данным в мире у 1% населения (порядка 71 млн человек) выявляются антитела к ВГС (anti-HCV), среди которых 2/3 хронически инфицированы, и 1/3 выздоровели самостоятельно или вследствие излечения. Заболевание шире распространено в Африке и Азии (почти 3% населения), в то время как в Америке и Европе оно выявляется у 1,5-2,0% [17]. Достоверная распространённость ХВГС в РФ остаётся неизвестной, расчетное число пациентов может достигать 4,9 млн [16]. По данным Роспотребнадзора в субъектах РФ по состоянию на 01.01.2017 на диспансерном учёте состояло 591 830 пациентов с ХВГС [16].
В России самым распространенными являются ГТ 1 (52,6%, из них 3,7% приходятся на субтип 1а и 48,9% – на субтип 1b) и ГТ 3 (39,6%), гораздо реже встречается ГТ 2 (7,8%). Генотипы 4-6 встречаются менее чем в 0,01% случаев, ГТ 7 и 8 – крайне редко [16]. С появлением пангенотипных схем противовирусного лечения ХВГС клиническое значение ГТ ВГС постепенно утрачивается, однако остается еще ряд генотип-специфичных препаратов, перед применением которых необходимо уточнять ГТ ВГС.
Источником инфекции является больной человек. Наиболее значимым является парентеральный путь передачи (при употреблении внутривенных наркотических препаратов, медицинских манипуляциях, травмирующих косметических процедурах, включая маникюр и педикюр, нанесение татуировок и установку пирсинга), существенно реже – половой и вертикальный пути передачи [18].
Риск профессионального заражения медицинских работников при случайном уколе игрой, контаминированной инфицированной кровью, составляет около 1,8%. При попадании крови пациента на поврежденную кожу или неповрежденные слизистые медицинского работника риск инфицирования значительно меньше, а попадание ее на неповреждённую кожу безопасно. В связи с этим риск заражения для медицинского персонала мал. Риск инфицирования пациента от заражённого медицинского работника крайне мал [18]. Риск перинатальной передачи инфекции составляет 5-10% и мало зависит от способа родоразрешения, однако возрастает при наличии коинфекции ВИЧ у матери до 14-16% [18]. Низкая концентрация вируса в секретах половых желез и органах определяют низкий риск его передачи половым путем: около 0,5% в год при незащищенном половом контакте в моногамной гетеросексуальной паре, около 0,4-1,8% в год среди лиц, оказывающих сексуальные услуги [19], около 0,8% в год среди мужчин, практикующих секс с мужчинами с моноинфекцией ВГС (при коинфекции ВИЧ он выше в 4 раза) [20].
ВГС обладает сравнительно невысокой устойчивостью к воздействию факторов окружающей среды. Известно, что вирус устойчив к нагреванию до 50 0 С, полная его инактивация наступает через 30 минут при температуре 60 0 С и через 2 минуты при температуре 100С. Вирус чувствителен к ультрафиолетовому облучению и воздействию растворителей липидов [21].
Клиническая картина
Cимптомы, течение
У большинства пациентов заболевание протекает бессимптомно и выявляется при обследовании в рамках диспансеризации, догоспитальной подготовки, при посещении гастроэнтеролога по поводу диспепсических явлений (как правило, не связанных прямо с наличием ХВГС) и других специалистов (гинекологов, урологов, стоматологов и т.д.). От времени инфицирования до установления диагноза может пройти несколько лет. В ряде случаев первым проявлением заболевания являются В-клеточные лимфопролиферативные или иммунологически обусловленные внепеченочные заболевания (криоглобулинемический васкулит, в том числе с синдромом Рейно; интерстициальные заболевания легких; гломерулонефрит; синдром Шегрена; артрит и др.). У достаточного числа пациентов диагноз устанавливается только после манифестации осложнений ЦП: кровотечение из варикозно расширенных вен (ВРВ) пищевода и желудка и развития асцита [22,23].
Активность трансаминаз может быть как повышенной, так и в пределах референсных значений. В некоторых случаях отмечается периодическое повышение активности АЛТ. В крови обнаруживаются anti-HCV и РНК ВГС. Активность АЛТ в пределах нормальных значений не свидетельствует об отсутствии изменений в печени, и пациенты не могут рассматриваться как «здоровые носители». Было показано, что 30-50% случаев у таких больных может быть диагностирован ЦП [24,25]. Часто в начальной стадии компенсированного ЦП отмечаются лишь похудание, астенизация, снижение работоспособности. При осмотре выявляют увеличение печени с ее уплотнением и спленомегалию. Однако у 20% больных в начальной стадии ЦП протекает бессимптомно, и его обнаруживают, как правило, случайно во время профилактического осмотра или обследования по поводу другого заболевания.
Цирроз печени развивается, как правило, в 25-35% случаев ХВГС. Вероятность его развития составляет 7,3% в год (5,1-9,5%). У многих пациентов ЦП в исходе ХВГС впервые диагностируется по данным гистологического исследования биоптата печени. Темпы декомпенсации ЦП составляют 5,5% в год. Вероятность развития в течение года синдрома портальной гипертензии у больных с компенсированным ЦП составляет 3,6%, печеночной энцефалопатии – 0,4%, ГЦК – 1,5% [24,26,27].
Диагностика
Диагностика заболевания или состояния (группы заболеваний или состояний, медицинские показания и противопоказания к применению методов диагностики
Диагноз ХВГС устанавливается на основании наличия антител к вирусу гепатита С (Определение суммарных антител классов M и G (anti-HCV IgG и anti-HCV IgM) к вирусу гепатита C (Hepatitis C virus) в крови, далее везде в тексте – anti-HCV) и РНК вируса гепатита С (Определение РНК вируса гепатита C (Hepatitis C virus) в крови методом ПЦР, качественное исследование, далее везде в тексте – РНК ВГС) или ядерного антигена ВГС (Определение Core-антигена вируса гепатита C (Hepatitis C virus) в крови, далее везде в тексте – HCVcAg) на протяжении более 6 месяцев [1].
Специфических жалоб, характерных для ХВГС, нет. Заболевание, как правило, протекает бессимптомно, и довольно часто манифестирует осложнениями ЦП (асцит, кровотечение из ВРВ пищевода и желудка, печеночная энцефалопатия) [28]. В ряде случаев первыми проявлениями заболевания выступают иммунологически обусловленные внепеченочные проявления [23].
При физикальном осмотре, как правило, никаких изменений не выявляется. Возможно наличие признаков ЦП (асцит, «печеночные ладони», ВРВ брюшной стенки, отеки, спленомегалия). При развитии иммунологически обусловленных внепеченочных проявлений имеют место соответствующие изменения [23].
Скрининг на наличие ХВГС основан на выявлении anti-HCV. Если обнаружены anti-HCV, следует обязательно провести анализ на РНК ВГС. В случае если анализ на РНК ВГС недоступен, допустимо провести тест на HCVcAg. Этот антиген в сыворотке или плазме крови также является маркером репликации ВГС. Анализ HCVcAg менее чувствителен, чем РНК ВГС (нижний предел обнаружения эквивалентен приблизительно 500-3000 МЕ/мл РНК ВГС, в зависимости от ГТ ВГС [28,29]). В редких случаях HCVcAg не обнаруживается при определяемой РНК ВГС [30].
- Рекомендуется обследование anti-HCV у лиц из группы повышенного риска для выявления потенциально инфицированных [1].
Комментарии: отношение к группе повышенного риска устанавливается, как правило, на основании слов пациента (место работы, реципиент в анамнезе, введение инъекционных наркотиков, половые партнеры, семейный анамнез и т.д.).
— Пациенты центров и отделений гемодиализа, пересадки почки, сердечно-сосудистой и лёгочной хирургии, гематологии;
— Пациенты с иммунодефицитом (пациенты с онкологическими заболеваниями, пациенты на гемодиализе, пациенты на лечении иммунодепрессантами и др.);
— Пациенты с заболеваниями печени неясной этиологии (в процессе первичного клинико-лабораторного обследования).
- Всем пациентам с выявленными anti-HCV рекомендуется провести анализ РНК ВГС или HCVcAg (в случае недоступности первого) для подтверждения наличия текущей инфекции [1].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
- Всем пациентам с выявленными anti-HCV и отрицательной РНК ВГС (или HCVcAg) в случае недоступности первого) рекомендуется провести повторный анализ РНК ВГС через 12 и 24 недели, с тем чтобы подтвердить или опровергнуть наличие ХВГС [1].
Комментарии: наличие anti-HCV в сочетании с РНК ВГС (или HCVcAg) характерно как для пациентов с ХВГС, так и пациентов с острым гепатитом С. Концентрация РНК ВГС (или HCVcAg) у больных с острым гепатитом С может значительно колебаться, вплоть до неопределяемого уровня. Таким образом, пациентам с неопределяемой РНК ВГС (или HCVcAg), необходимо повторно провести анализ РНК ВГС (или HCVcAg) через 12 и 24 недели после отрицательного результата, с тем чтобы убедиться в клиренсе ВГС (самостоятельное выздоровление от острого гепатита С) или подтвердить формирование ХВГС.
- Определение генотипа вируса гепатита С (Определение генотипа вируса гепатита C (Hepatitis C virus), далее везде в тексте – ГТ ВГС) рекомендуется только пациентам с ХВГС для планирования генотип-специфичной схемы противовирусной терапии (ПВТ) [1].
Комментарии: ГТ ВГС имеет значение только при планировании генотип-специфичных противовирусных препаратов. При доступности пангенотипных препаратов это обследование не требуется.
- Всем пациентам с ХВГС с исходом в ЦП и/или признаками внепеченочных проявлений (лимфопролиферативные заболевания) рекомендуется проведение общего (клинического) анализа крови развернутого [23,36-38].
Комментарии: течение ХВГС может влиять на клеточный состав крови, однако убедительных доказательств таких изменений в отсутствии ЦП и лимфопролиферативных заболеваний, индуцированных ВГС, нет. В случае формирования ЦП чаще всего наблюдается тромбоцитопения различной степени выраженности, реже другие варианты цитопений.
- Всем пациентам с ХВГС рекомендуется проведение анализа крови биохимического общетерапевтического для определения активности трансаминаз (аланинаминотрансфераза, аспартатаминотрансфераза), тяжести повреждения гепатоцитов, оценки функции печени и почек [39-41].
Комментарии: в отсутствии признаков ЦП клиническое значение активности трансаминаз и других показателей функции печени (билирубин, альбумин) невелико. Оно приобретает большее значение, если имеет место сочетанная патология печени. У пациентов с ЦП в исходе ХВГС тяжесть поражения гепатоцитов и признаки декомпенсации имеют решающее значение в выборе тактики ведения пациента, препаратов ПВТ, прогнозе течения заболевания [39]. Кроме того, АЛТ и АСТ могут использоваться для самостоятельной оценки выраженности фиброза печени (например, индексы APRI, FIB-4) в отсутствии возможности выполнить инструментальное обследование [42] (см. Приложение Г). Оценка функции почек (креатинин) необходима при планировании схем ПВТ, содержащих софосбувир** [40,41].
- Всем пациентам с ХВГС с исходом в ЦП рекомендуется определение протромбинового (тромбопластинового) времени в крови или в плазме для оценки функции печени [46].
- Рекомендуется исследование уровня альфа-фетопротеина (АФП) в сыворотке крови пациентам с ХВГС с выраженным и тяжелым фиброзом печени (F3-F4 по METAVIR) для своевременной диагностики ГЦК [44,45].
Комментарии: риск развития ГЦК на стадии ЦП составляет приблизительно 1-5% в год. Вероятность летального исхода в течение первого года после постановки диагноза у пациентов с ГЦК составляет 33%.
- Лабораторный мониторинг не рекомендуется пациентам с ХВГС без ЦП во время ПВТ без применения рибавирина** [205,206].
Комментарий: препараты современной ПВТ обладают высокой безопасностью и эффективностью, в связи с чем необходимости в лабораторном мониторинге во время ПВТ без применения рибавирина** нет.
- При применении РБВ** рекомендуется раз в 2-4 недели исследовать общий (клинический) анализ крови развернутый, с тем чтобы исключить вероятность частого побочного эффекта препарата – анемии [117].
- Не рекомендуется определение РНК во время ПВТ для оценки ее эффективности [46-48] (см. Приложение Б).
Комментарий: закономерности между скоростью элиминации ВГС во время ПВТ и вероятностью УВО нет, в связи с чем необходимости в контроле РНК ВГС во время лечения нет [48].
- Не рекомендуется использовать анализ anti-HCV пациентам, выздоровевшим от ХВГС вследствие ПВТ, для контроля реинфицирования ВГС [49-51].
Комментарий: после успешной ПВТ anti-HCV сохраняются длительно в подавляющем большинстве случаев, поэтому этот анализ не может использоваться для определения реинфицирования у пациентов с опытом элиминации ВГС. Доля пациентов, у которых anti-HCV постепенно исчезают, очень мала, и срок этого исчезновения неизвестен.
- Всем пациентам, получившим курс ПВТ ХВГС, рекомендуется определение РНК ВГС через 12 недель после окончания ПВТ для оценки ее эффективности (УВО12) [46-48] (см. Приложение Б).
Комментарий: отсутствие РНК ВГС через 12 недель после завершения ПВТ соответствует излечению от ХВГС, так как поздний рецидив возникает менее чем в 0,2% случаев [48].
- Рекомендуется определение уровня АФП пациентам с выраженным фиброзом печени (F3 по METAVIR) и с ЦП 1 раз в полгода для диагностики ГЦК [44,45].
Комментарий: риск развития ГЦК на стадии ЦП составляет около 1-5% в год. Вероятность летального исхода в течение первого года после постановки диагноза у пациентов с ГЦК составляет 33%.
- Всем пациентам с ХВГС рекомендуется выполнить УЗИ органов брюшной полости (комплексное) и забрюшинного пространства для выявления признаков ЦП и ГЦК [52,53].
Комментарии: УЗИ органов брюшной полости и забрюшинного пространства проводится для диагностики ГЦК, признаков портальной гипертензии (увеличения селезенки, расширения вен портальной системы), асцита, исключения сопутствующей патологии желудочно-кишечного тракта, что в некоторых случаях может иметь решающее значение в определении стадии заболевания и тактики лечения. ЦП и ГЦК в исходе ХВГС могут протекать бессимптомно и выявляться только по данным УЗИ. При обнаружении в печени образования, подозрительного на ГЦК, следует продолжить исследования согласно клиническим рекомендациям по диагностике и лечению ГЦК.
- Всем пациентам с ХВГС рекомендуется выполнение неинвазивной диагностики фиброза, с тем чтобы определить тактику ПВТ и дальнейшее ведение пациента (в случае ЦП) [54-58].
Комментарии: неинвазивная диагностика позволяет с высокой точностью определить стадию фиброза. Она может быть выполнена с помощью эластометрии печени (должна быть выполнена на валидизированном аппарате), либо с помощью сывороточных тестов. При недоступности эластометрии могут использоваться некоммерческие расчетные показатели, основанные на результатах лабораторного обследования (например, расчет индексов APRI, FIB-4, см. Приложения Г2, Г3).
- При получении противоречивых данных неинвазивной диагностики рекомендуется рассмотреть вопрос о проведении чрескожной биопсии печени, с тем чтобы определить тактику ПВТ и дальнейшее ведение пациента (в случае ЦП) [1].
Комментарии: Биопсия печени является инвазивной процедурой с риском развития осложнений, поэтому ее следует проводить только в случае, если не удается получить результат с помощью применения неинвазивных методов [1].
- Рекомендовано выполнение эзофагогастродуоденоскопии (ЭГДС) пациентам с ХВГС с исходом в ЦП для оценки наличия и степени ВРВ пищевода и желудка [59-61].
Комментарии: Эндоскопический осмотр выполняется для диагностики степени ВРВ пищевода и желудка, а также при наложении клипс и лигатур при кровотечении или его профилактики из вен пищевода у пациентов с ЦП. Возможно проведение процедуры в условиях седации, что требует предварительной консультации и сопровождения анестезиолога.
- Компьютерная томография органов брюшной полости с внутривенным болюсным контрастированием или магнитно-резонансная томография органов брюшной полости с внутривенным контрастированием рекомендуется провести пациентам с ХВГС при обнаружении в печени образования по результатам УЗИ брюшной полости (комплексное) для уточнения его природы [62-65].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
- Рекомендуется выполнение неинвазивной диагностики стадии фиброза печени (эластометрия печени, при ее недоступности – сывороточные расчетные некоммерческие тесты APRI, FIB-4) пациентам с ХВГС 1 раз в год для динамического наблюдения [54,55,57,66].
- Рекомендуется выполнение ЭГДС пациентам с ХВГС с исходом в ЦП для динамического наблюдения 1 раз в год [59-61,67].
- После излечения от ХВГС пациентам с ЦП или выраженным фиброзом печени (F3 по METAVIR) рекомендуется пожизненно проводить скрининговое обследование для раннего выявления ГЦК (УЗИ брюшной полости комплексное каждые 6 месяцев) [53].
Комментарии: у данных пациентов сохраняется риск развития ГЦК, несмотря на элиминацию вируса из организма, поэтому им рекомендовано проведение профилактического обследования для ее раннего выявления.
Лечение
Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
Цель лечения ХВГС – элиминация ВГС для профилактики осложнений ХВГС (включая ЦП, ГЦК, смерть), улучшение качества жизни и предотвращение дальнейшей передачи ВГС в популяции. Вирус гепатита С не образует высокостабильных внутриклеточных форм генетического материала, поэтому может быть элиминирован из организма полностью [1]. Показателем элиминации вируса из организма является стойкое достижение неопределяемого уровня РНК вируса в крови, которое оценивают через 12 недель после окончания терапии (УВО12) [29,30].
- стадия фиброза печени, наличие ЦП и его класс;
- ГТ ВГС;
- наличие некоторых сопутствующих заболеваний;
- опыт предыдущей ПВТ (если есть);
- прием лекарственных средств по поводу сопутствующей патологии.
- Противовирусное лечение рекомендуется проводить всем пациентам с ХВГС, независимо от наличия ЦП, с целью излечения от инфекции (эрадикации ВГС) [1,69] (см. также Приложение А3).
Комментарии: лечение ХВГС показано всем больным, так как в настоящее время применяются высокоэффективные и безопасные препараты, которые позволяют добиться УВО в подавляющем большинстве случаев.
Для лечения ХВГС применяются противовирусные препараты прямого действия (ПППД). Те из них, которые входят в список ЖНЛВП, отмечаются знаком **. ПППД представляют собой ингибиторы различных неструктурных белков вируса. Второй корень названия ПППД указывает на то, какой конкретно белок он ингибирует: «-превир» – NS3/NS4A, «-асвир» – NS5А, «-бувир» – NS5B. Выбор препаратов для лечения и длительность лечения зависят от стадии фиброза, наличия и класса ЦП, ГТ вируса, опыта предшествующей терапии ХВГС, наличия сопутствующих заболеваний (в частности, хронической болезни почек (ХБП)), некоторых препаратов сопутствующей терапии. В зависимости от эффективности при различных ГТ выделяют пангенотипные схемы (эффективны при всех ГТ вируса) и генотип-специфические (эффективны только при определенных ГТ ВГС). В табл. 1 представлены лекарственные средства и их компоненты, применяющиеся в РФ.

Табл. 1. Компоненты, входящие в состав лекарственных средств прямого противовирусного действия, и лекарственные средства прямого противовирусного действия, одобренные для применения в РФ (представлены в алфавитном порядке).
- Велпатасвир + софосбувир** (ВЕЛ+СОФ**)
- Глекапревир + пибрентасвир** (ГЛЕ+ПИБ**)
- Гразопревир + элбасвир** (ГРА+ЭЛБ**)
- Дасабувир; омбитасвир + паритапревир + ритонавирб** (ДСВ; ОБВ+ПТВ/р**)
- Ледипасвир + софосбувир (ЛЕД+СОФ)
б — ритонавир** (РТВ**) – фармакокинетический бустер, не обладает противовирусной активностью, используется с НРВ** и ПТВ для увеличения их концентрации в крови.
- Безотлагательно терапию рекомендуется рассмотреть в первую очередь у пациентов:
— с риском быстрого развития заболевания печени по причине сопутствующих заболеваний (хронический вирусный гепатит В, ВИЧ-инфекция, сахарный диабет и
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
- Перед применением ПППД рекомендуется проверить сочетаемость назначенной схемы с уже принимаемыми пациентом препаратами, используя любой специальный ресурс (например, https://www.hep-druginteractions.org). При выявлении значимого взаимодействия рекомендуется заменить схему или препарат, который пациент принимает при лечении сопутствующего заболевания. Если это невозможно, решение следует принимать в индивидуальном порядке, оценивая соотношение пользы и риска от данной комбинации и возможных последствий от ее применения [70].
Комментарии: Большинство ПППД безопасно, но особенности их фармакокинетики могут приводить к значимому взаимодействию с другими препаратами, принимаемыми пациентом.
- Пациенты без опыта ПВТ и без ЦП;
- Пациенты без опыта ПВТ с компенсированным ЦП;
- Пациенты, не ответившие на предшествующую ПВТ (ПегИФН** + РБВ** ± СОФ** или СОФ** + РБВ**) без ЦП;
- Пациенты, не ответившие на предшествующую ПВТ (ПегИФН** + РБВ** ± СОФ** или СОФ** + РБВ**) с компенсированным ЦП.
Лечение пациентов с декомпенсированным ЦП рассматриваются отдельно в разделе «Трансплантация печени» и в Приложении А3.
Принципы перелечивания после неуспешного курса ПППД (ингибиторующими NS3/4А и/или ингибиторующими NS5A) рассматриваются в разделе Перелечивание.
- Лечение пациентов с ХВГС без ЦП, без опыта ПВТ и без трансплантации печени в анамнезе рекомендуется проводить по одной из альтернативных схем согласно табл. 2:
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Табл. 2. Схемы ПВТ ХВГС для пациентов без предшествующего опыта ПВТ и без цирроза печени в зависимости от генотипа (лекарственные средства представлены в алфавитном порядке).

ДАК** + НРВ**/р** – даклатасвир** 60 мг 1р/д + нарлапревир** 200 мг 1 р/д (2 таб. одновременно, по 100 мг каждая) + ритонавир** 100 мг 1р/д;
ДСВ; ОБВ+ПТВ/р** – дасабувир (1 таб. по 250 мг 2 р/д); омбитасвир + паритапревир + ритонавир** (2 таб. одновременно 1р/д, по 12,5/75/50 мг каждая);
НРВ**/р** + СОФ** – нарлапревир** 200 мг 1 р/д (2 таб. одновременно, по 100 мг каждая) + ритонавир** 100 мг 1р/д + софосбувир** 400 мг 1 таб. 1р/д;
а — при ВН не более 800 000 МЕ/мл срок лечения 12 недель; 16-недельный курс совместно с РБВ** следует рассмотреть при ВН ВГС >800 000 ME/мл и/или при наличии полиморфизмов NS5A;
б — у пациентов со слабовыраженным фиброзом (F0-2) 8 недель, с фиброзом F3-F4 по METAVIR – 12 недель.
в — у пациентов со слабовыраженным фиброзом (F0-2) и ВН менее 1 000 000 МЕ/мл можно рассмотреть длительность 8 недель по решению врачебной комиссии.
- Лечение пациентов с ХВГС с компенсированным ЦП без опыта ПВТ рекомендуется проводить по одной из альтернативных схем согласно табл. 3:

Табл. 3. Схемы ПВТ ХВГС для пациентов с компенсированным циррозом печени без предшествующего опыта ПВТ в зависимости от генотипа (лекарственные средства представлены в алфавитном порядке).
ДСВ; ОБВ+ПТВ/р** – дасабувир (1 таб. по 250 мг 2 р/д); омбитасвир + паритапревир + ритонавир** (2 таб. одновременно 1р/д, по 12,5/75/50 мг каждая);
а — при ВН не более 800 000 МЕ/мл срок лечения 12 недель; 16-недельный курс совместно с РБВ** следует рассмотреть при ВН ВГС >800 000 ME/мл и/или при наличии полиморфизмов NS5A;
- Лечение пациентов с ХВГС, не ответивших на предшествующую терапию ПегИФН** + РБВ** ± СОФ** или СОФ** + РБВ**, без ЦП рекомендуется проводить по одной из альтернативных схем согласно табл. 4:
Табл. 4. Схемы ПВТ ХВГС для пациентов, не ответивших на предшествующую терапию ПегИФН** + РБВ** ± СОФ** или СОФ** + РБВ**, без цирроза печени в зависимости от генотипа (лекарственные средства представлены в алфавитном порядке).


ДСВ; ОБВ+ПТВ/р** – дасабувир (1 таб. по 250 мг 2 р/д); омбитасвир + паритапревир + ритонавир** (2 таб. одновременно 1р/д, по 12,5/75/50 мг каждая);
а – при ВН не более 800 000 МЕ/мл срок лечения 12 недель; 16-недельный курс совместно с РБВ** следует рассмотреть при ВН ВГС >800 000 ME/мл и/или при наличии полиморфизмов NS5A.
- Лечение пациентов с ХВГС, не ответивших на предшествующую терапию ПегИФН** + РБВ** ± СОФ** или СОФ** + РБВ**, с компенсированным ЦП рекомендуется проводить по одной из альтернативных схем согласно табл. 5:

Табл. 5. Схемы ПВТ ХВГС для пациентов, не ответивших на предшествующую терапию, ПегИФН** + РБВ** ± СОФ** или СОФ** + РБВ**, с компенсированным циррозом печени в зависимости от генотипа (лекарственные средства представлены в алфавитном порядке).
ДСВ; ОБВ+ПТВ/р** – дасабувир (1 таб. по 250 мг 2 р/д); омбитасвир + паритапревир + ритонавир** (2 таб. одновременно 1р/д, по 12,5/75/50 мг каждая);
а — при ВН не более 800 000 МЕ/мл срок лечения 12 недель; 16-недельный курс совместно с РБВ** следует рассмотреть при ВН ВГС >800 000 ME/мл и/или при наличии полиморфизмов NS5A;
в — в случае недоступности иных схем лечения.
Все схемы ПВТ для лечения пациентов с ХВГС (всех ГТ ВГС) с ЦП (в т.ч. декомпенсированным) или без него, с опытом предшествующей ПВТ или без него, суммированы также в Приложении А3.
- Всем пациентам, получившим ПВТ ХВГС, рекомендуется провести качественное определение РНК ВГС через 12 недель после окончания лечения, с тем чтобы оценить эффективность проведенной ПВТ. Рекомендуется использовать методы с высокой чувствительностью (≤15 МЕ/мл) [46-48,111]. Отсутствие РНК ВГС через 12 недель после окончания ПВТ означает излечение от ХВГС. Напротив, положительный результат РНК ВГС в эти сроки указывает на неудачу проведенного лечения.
- При применении РБВ** рекомендуется раз в 2-4 недели исследовать общий развернутый (клинический) анализ крови, и при снижении гемоглобина на 10 г/л от исходного и более уменьшить дозу препарата на 200 мг/сут, а при концентрации гемоглобина менее 85 г/л отменить терапию РБВ** [112-117].
Комментарии: Большинство современных препаратов ПВТ ХВГС хорошо переносятся, однако в ряде случаев необходимо добавлять РБВ** (для некоторых схем, особенно для пациентов с ЦП) – препарат, одним из основных побочных эффектов которого является не иммунный гемолиз. При применении РБВ** следует контролировать общий развернутый (клинический) анализ крови и при необходимости проводить коррекцию терапии.
- По решению лечащего врача, независимо от условий оказания медицинской помощи, для контроля ПВТ (в т.ч. оценки эффективности и безопасности) взрослых пациентов с ХВГС рекомендуется рассмотреть применение телемедицинских технологий [228,230].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3)
В большинстве случаев (95-100%) применение ПППД приводит к УВО, однако в редких случаях достичь УВО не удается.
- При неэффективности терапии ПППД рекомендуется использовать схему с другими препаратами, а также комбинацию из трех препаратов различного механизма действия (препаратом, ингибирующим NS3/NS4A + препаратом, ингибирующим NS5A + препаратом, ингибирующим NS5B) без РБВ** или с добавлением его. Если доступно исследование мутаций резистентности ВГС к различным ПППД, рекомендуется выполнить его для рационального подбора новой схемы [71-76,167,212].
— Пациентам с ХВГС (ГТ 1-6) без ЦП или с компенсированным ЦП после неэффективной ПВТ препаратами, ингибирующими NS3/4А+/-NS5В: для перелечивания рекомендуется пангенотипная схема велпатасвир + софосбувир** 100/400 мг в течение 12 недель;
— Пациентам с ХВГС (ГТ 1-6) с декомпенсированным ЦП после неэффективной ПВТ препаратами, ингибирующими NS3/4А+/-NS5В: для перелечивания рекомендуется пангенотипная схема велпатасвир + софосбувир** 100/400 мг в комбинации с РБВ** (600 – 1200 мг/сут) в течение 12 недель;
— Пациентам с ХВГС (ГТ 1-6) без ЦП или с ЦП (компенсированным и декомпенсированным) после неэффективной ПВТ препаратами, ингибирующими NS5А: для перелечивания рекомендуется пангенотипная схема велпатасвир + софосбувир** 100/400 мг в комбинации с РБВ** (600 – 1200 мг/сут) в течение 24 недель;
— Пациентам с ХВГС (ГТ 1) без ЦП или с компенсированным ЦП после неэффективной ПВТ препаратами, ингибирующими NS3/4А без препаратамов, ингибирующих NS5A: для перелечивания рекомендуется схема глекапревир + пибрентасвир** (300/120 мг) в течение 12 недель;
ПВТ препаратами, ингибирующими NS5A, без препаратов, ингибирующих NS3/4А: для перелечивания рекомендуется схема глекапревир + пибрентасвир** (300/120 мг) в течение 16 недель;
— Пациентам с ХВГС (ГТ 1-6) без ЦП или с компенсированным ЦП после неэффективной ПВТ препаратами, ингибирующими NS3/4А и NS5А: по решению врачебной комиссии для перелечивания можно рассмотреть #глекапревир + пибрентасвир** (300/120 мг 1р/д) в сочетании с софосбувиром** (400 мг 1 р/д) внутрь и/или РБВ** (1000-1200 мг/сут) в течение 12-24 недель. Длительность курса определяется индивидуально и зависит, в том числе, от стадии фиброза печени и наличия резистентных к ПППД вариантов ВГС.
Патогенетической терапии для пациентов с ХВГС нет.
Симптоматической терапии для пациентов с ХВГС нет.
- Рекомендуется проведение трансплантации печени при наличии стойких признаков декомпенсации функции печени пациентам с ЦП для сохранения жизни [118-120].
Комментарий: дообследование проводится в соответствии с протоколом ведения пациентов из листа ожидания в трансплантологическом центре.
- Пациентам с ЦП рекомендуется выполнение эндоскопического лигирования или склерозирования ВРВ пищевода и желудка для профилактики кровотечения или его купирования [121-125].
- Рекомендуется выполнение лапароцентеза пациентам с ЦП при наличии рефрактерного асцита для его купирования [126].
- Рекомендуется выполнение трансъюгулярного внутрипеченочного порто-системного шунтирования пациентам при наличии выраженной портальной гипертензии [126].
- Пациентам с внепеченочными иммунологически обусловленными проявлениями ХВГС рекомендуется назначить ПППД по описанным выше схемам [23,127-129].
Комментарии: ХВГС может проявиться внепеченочными иммунологически обусловленными состояниями (криоглобулинемический васкулит, в том числе с синдромом Рейно, интерстициальные заболевания легких, гломерулонефрит, синдром Шегрена, артрит и другие), а также неходжкинскими В-клеточными лимфомами. Во всех случаях следует назначить ПППД по описанным выше схемам. Раннее начало ПВТ значительно снижает риск развития внепеченочных проявлений.
Пациенты с ХВГС и коинфекцией ВИЧ относятся к группе, требующей безотлагательной ПВТ ХВГС [1,69]. Течение ХВГС у ВИЧ-инфицированных зависит от степени выраженности иммунодефицита, обусловленного ВИЧ. Вероятность развития тяжелого поражения печени особенно высока при снижении CD4 лимфоцитов менее 200/мкл. Прогрессирование, связанное с поражением печени, обусловлено повышением концентрации вируса в крови (в 2-8 раз) на фоне выраженного иммунодефицита. Коинфекция ВИЧ и ВГС приводит к увеличению частоты развития осложнений, а также связанной с этими заболеваниями смертности.
Антиретровирусная терапия коинфицированных ВГС/ВИЧ больных ассоциирована с возможным риском нарушения функций печени вследствие ее гепатотоксичности [130,131].
- Для лечения ХВГС у больных, коинфицированных ВИЧ, рекомендуется использовать те же схемы ПВТ, что и для лечения моноинфекции ВГС, с целью эрадикации ВГС [132-137].
Комментарии: все схемы ПВТ на основе ПППД требуют учета межлекарственных взаимодействий. Одним из удобных способов оценки межлекарственных взаимодействий является использование Ливерпульской таблицы лекарственных взаимодействий в Интернет ресурсе (http://www.hep-druginteractions.org).
Пациенты с ХВГС и коинфекцией вирусом гепатита В (ВГВ) относятся к группе, требующей безотлагательной ПВТ ХВГС [1,69]. Коинфекция ВГС/ВГВ ускоряет прогрессирование заболевания и увеличивает риск развития ГЦК [138,139].
- Всем больным ХВГС рекомендуется провести тестирование на наличие перенесенной или текущей инфекции, вызванной ВГВ (HBsAg, anti-HBs, anti-HBc суммарные) [140-143].
- Пациентам с коинфекцией ВГС/ВГВ рекомендуется назначить ПВТ нуклеозидами и нуклеотидами, кроме ингибиторов обратной транскриптазы, для профилактики реактивации инфекции, вызванной ВГВ. ПВТ нуклеозидами и нуклеотидами, кроме ингибиторов обратной транскриптазы, рекомендуется назначить на весь срок терапии ХВГС, а также на 12 недель после ее успешного завершения [142].
Комментарии: поскольку ВГС, как правило, подавляет репликацию ВГВ, устранение первого вируса может привести к реактивации второго. Поэтому при лечении ХВГС следует тщательно контролировать маркеры активности ВГВ, и при их увеличении назначить ПВТ инфекции, вызванной ВГВ. Эту терапию также можно назначить с профилактической целью на срок лечение ХВГС и далее в течение 12 недель после ее успешного завершения.
- Пациентам с ХВГС и anti-HBc (в отсутствии HBsAg и anti-HBs) во время ПВТ ХВГС рекомендуется ежемесячный контроль АЛТ для исключения реактивации ВГВ [142].
- При коинфекции ВГС/ВГВ для лечения ХВГС рекомендуется использовать стандартные схемы, описанные выше [1,138,142-145].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2)
Комментарии: на сегодня накоплено достаточно клинического опыта применения софосбувира** у пациентов с тяжелой ХБП [153-155], что позволяет рекомендовать софосбувир**-содержащие схемы ПВТ всем таким пациентам без коррекции доз ПППД.
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
11.1 Противовирусная терапия ХВГС у больных с декомпенсированным циррозом печени, находящихся в Листе ожидания трансплантации печени
Целями ПВТ ХВГС у больных с декомпенсированным ЦП, находящихся в Листе ожидания ортотопической трансплантации печени (ОТП), являются:
- Предотвращение инфицирования трансплантата печени;
- Улучшение функции печени перед трансплантацией;
- Выведение пациента из Листа ожидания ОТП.
Улучшение функции печени оценивается по клиническим показателям, а также по шкалам Child-Pugh (см. Приложение Г) и MELD (для подсчета этого индекса можно использовать любой интернет-ресурс, например, https://www.mdcalc.com/meldna-meld-na-scoreliver-cirrhosis). Улучшение оценки MELD наблюдается у 60% больных с декомпенсированным ЦП, завершивших курс ПВТ. Это улучшение тем более вероятно и тем сильнее выражено, чем ниже оценка MELD до начала терапии.
До 25-30% больных с декомпенсированным ЦП могут иметь стойкое улучшение (компенсацию) ЦП, что позволяет вывести их из Листа ожидания ОТП. Выживаемость таких пациентов на протяжении 3-х лет не ниже, чем в группе реципиентов печени, которым была проведена ОТП, сопоставимых по исходной MELD [118,119,158-162].
- Больным с декомпенсированным циррозом в исходе ХВГС (Child-Pugh В или С) без ГЦК, ожидающим ОТП, рекомендуется назначать ПВТ, если MELD
Комментарии: для ПВТ пациентов с декомпенсированным ЦП строго противопоказано использование препаратов, ингибирующих NS3/4.
- Больным с декомпенсированным ЦП в исходе ХВГС (Child-Pugh В или С) без ГЦК, ожидающим трансплантацию печени, с MELD ≥20 рекомендуется провести ОТП, не назначая ПВТ. ПВТ ХВГС рекомендуется провести после трансплантации [165,166].
- Больным с декомпенсированным ЦП в исходе ХВГС (Child-Pugh В или С) без ГЦК, ожидающие ОТП, с MELD ≥20 могут начать лечение до ОТП, если предполагаемое время ожидания органа превышает 6 месяцев [165,166].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1)
- ПВТ инфекции трансплантата, вызванной ВГС, рекомендуется проводить всем реципиентам, у которых выявляется РНК ВГС в крови, насколько это возможно по состоянию пациента [176,177].
Комментарии: частота УВО у реципиентов печени с компенсированной болезнью трансплантата, получивших запланированный курс ПВТ, составляет более 95%. УВО ассоциируется с замедлением прогрессирования фиброза и улучшением выживаемости трансплантата и реципиентов.
Беременность, по-видимому, не оказывает негативного влияния на течение ХВГС. Активность АЛТ в сыворотке крови снижается в течение I и III триместров беременности и повышаются после родов. Уровень РНК ВГС повышается в течение I и III триместров, достигая пика в течение III триместра, и снижается после родоразрешения. Эти события, вероятно, обусловлены иммуносупрессивными эффектами беременности и увеличением объема материнской плазмы [191,192]. Передача ВГС от матери ребенку встречается с общей частотой от 5% до 15% [193,194]. Убедительных данных о негативном влиянии ВГС на развитие плода и исход беременности нет. Есть отдельные сообщения о влиянии ЦП на течение беременности и ее исход. Так, беременные женщины с ЦП подвергаются повышенному риску неблагоприятных исходов для матери (например, преэклампсия, геморрагические осложнения и смерть) и для плода (например, преждевременные роды, низкая масса тела при рождении и неонатальная смерть). Женщины с ЦП в исходе ХВГС должны быть проинформированы об этих возможных осложнениях [195,196].
- Женщинам репродуктивного возраста рекомендуется ПВТ ХВГС до планирования беременности, с тем чтобы снизить риск передачи ВГС будущему ребенку [197].
- Для выявления ХВГС рекомендуется проводить обследование беременных на anti-HCV крови (Определение суммарных антител классов M и G (anti-HCV IgG и anti-HCV IgM) к вирусу гепатита C (Hepatitis C virus) в крови) в I (при постановке на учет по беременности) и в III триместрах беременности [198].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
- Не рекомендуется проводить ПВТ ПППД во время беременности из-за отсутствия в настоящее время достаточных данных о безопасности и эффективности ПППД [199, 200].
Комментарии: на сегодня не существует крупномасштабных клинических испытаний, оценивающих безопасность ПППД при беременности. Специальные исследования ПВТ СОФ** и ЛЕД+СОФ во время беременности продемонстрировали хорошую безопасность для плода. Данных об использовании пангенотипных схем во время беременности в настоящее время нет.
- Женщинам детородного возраста, получающим ПВТ ХВГС с РБВ**, не рекомендуется беременность во время приема ПВТ и в течение не менее 6 месяцев после прекращения ПВТ [201,202].
- Мужчинам, получающим ПВТ ХВГС с РБВ**, не рекомендуется беременность их половых партнерш во время приема ПВТ и в течение не менее 6 месяцев после прекращения ПВТ [201,202].
Комментарии: РБВ** обладает тератогенным свойством, то есть может вызвать аномалии развития и гибель плода. Его не следует назначать беременным женщинам или женщинам детородного возраста, которые могут забеременеть во время лечения РБВ** или в течение 6 месяцев после прекращения РБВ**. Кроме того, следует помнить, что РБВ** аналогичным образом может вызывать врожденные дефекты у плода, в случае если мужчина получал РБВ**, когда женщина забеременела от него. Таким образом, для избегания беременности во время лечения РБВ** и в течение не менее 6 месяцев после этого лицам с детородным потенциалом крайне важно использовать по крайней мере 2 формы эффективной контрацепции. Консультирующему врачу необходимо задокументировать обсуждение потенциальных тератогенных эффектов РБВ** в медицинской карте пациента.
- Женщинам с ХВГС не рекомендуется отмена грудного вскармливания, за исключением случаев повреждения сосков и кровотечения из этих повреждений [203,204].
Комментарии: грудное вскармливание не представляет риска для передачи ВГС от матери ребенку, поскольку частота инфицирования детей по результатам исследований сопоставима в группах на грудном вскармливании и на искусственном вскармливании. Однако в случае повреждения сосков и кровотечения из этих повреждений возникает риск инфицирования ребенка от матери с ХВГС вследствие передачи ВГС через кровь.
Вирусный гепатит С
Вирусный гепатит С – антропонозное заболевание, вызываемое вирусом и парентеральным повреждением. Наиболее часто протекает в форме острого или хронического (что наиболее часто) воспаления печени. Многие называют эту болезнь «ласковой», так как обычно симптомы ее очень похожи на другие заболевания. По статистическим данным предположительно в мире насчитывается 500 миллионов человек болеющих или являющимися переносчиками вируса гепатита С.
Природа гепатита С является многофакторной. Есть гепатиты первичные — вирусной природы, и гепатиты вторичные, которые возникают на фоне других заболеваний. Как неинфекционных (таких как заболевания органов пищеварения, различные заболевания крови, а также токсикозы беременных), так и инфекционных (мононуклеоз инфекционный, сепсис, инфекции кишечника, аденовирусная инфекция) болезней.
Существует еще такой вид болезни, как острый гепатит С. Он возникает в результате токсического взаимодействия разных лекарств, ядовитых отходов от промышленности, поражение радиацией, яд бледной поганки.
Статистические данные и наблюдения врачей говорят о том, что в ближайшие года вирусный гепатит С, к сожалению, станет главной задачей для здравоохранительных структур. Большая часть человечества подвержена этому заболеванию, и его распространение набирает быстрый темп в росте количества заболевших людей.
Из всех заболеваний, которые поражают именно печень, гепатит С является самой основной угрозой человечества. Как уже было сказано, возбудителем такого заболевания, как гепатит С, является вирус, и у него есть своя этиология. Относится он к семейству Flaviviridae, имеет свою собственную оболочку и в диаметре составляет 60-70 нм. При микроскопической диагностике на поверхности оболочки вируса очень хорошо видны бугорки и выступы высотой в 6-7 нм. Очень неустойчив возбудитель болезни к воздействию внешней среды.
Основным способом заражения является парентеральный путь, то есть биоматериал инфицированного человека, в данном случае кровь, попадает в кровяное русло другого, неинфицированного. В этом случае возможно заражение. С потоком крови вирус попадает в печень и начинает размножаться. Заболевание происходит не только из-за продуктов жизнедеятельности вируса, а и сама иммунная система, лимфоцитами, уничтожает зараженные печеночные клетки. Заражение возможно при парентеральных манипуляциях (инъекциях, накожных пробах на препараты, при стоматологических услугах), также в ряде других случаев, например, при нанесении на кожу татуировки, пирсинге, оказании парикмахерских услуг. Очень мало случаев заражения, таким заболеванием как гепатит С, половым путем. Инфицирование именно этим путем равно 15%. В основном при половом контакте передается также вирус гепатита, но только другой группы – гепатита В.
Очень часто, после заражения вирусом абсолютно ничего не происходит, то есть, нет начала болезни и клинических симптомов. Инфицированный человек становится переносчиком вируса, но самого гепатита С у него не наблюдается. Переносчики инфекции, в свою очередь, узнают о том, что они инфицированы, при проведении анализа крови на вирус гепатита С. Некоторые так и не знают о своем инфицировании. Бывает так, что переносчики болезни живут и по 50-60 лет, пребывая в абсолютном неведении.
Симптомы вирусного гепатита С

От момента заражения и до проявления первых клинических симптомов может пройти от 3 до 27 недель. Первые клинические симптомы проявляются в виде острых суставных болей, расстройством пищеварения, слабостью и недомоганием. Эти симптомы вирусного гепатита С характерны лишь для начального периода, который длится около 2-9 недель. Как правило острый гепатит С не отличается появлением желтухи, потому ни в начальном периоде заболевания ни позже ее проявления не заметны. Также не характерна для этой формы гепатита и гипертермия. Повышение температуры бывает при гепатите В. На ранних стадиях болезни, если вовремя не поставить диагноз и начать срочное лечение — очень велик риск перехода заболевания в хроническую стадию, которая чревата циррозом, а в худшем случае и раком печени. При подозрении на хронический гепатит С, основными симптомами, как правило являются повышенная усталость и психическая депрессия. Они вызываются воздействием продуктов жизнедеятельности вируса гепатита С на нервную систему организма.
Диагностика вирусного гепатита С
При принятии решения и определения диагноза о том, что человек болен таким заболеванием как вирусный гепатит С, намного упрощается тогда, когда врач имеет полную и правдивую информацию о всех предыдущих заболеваниях и обследованиях человека.
Как практика показывает, люди, в основном, узнают, что они больны гепатитом С, при сдачи донорской крови или в процессе того, когда проходят обычное обследование.
Обязательно нужно пройти все тесты и сдать все анализы на выявление в вашем организме гепатита С если:
- если анализ крови плохой, то есть какие-то симптомы о не очень здоровом состояние печени. Возможно использовали донорские услуги, и получили донорскую кровь от человека, который болен гепатитом С;
- использовали шприцы нестерильные, не важно, когда это было, даже если это было много лет назад;
- если вы работаете в учреждениях, куда обращаются люди с таким заболеванием и вы контактируете с кровью этих людей, или с шприцами, которыми кололи их, или есть контакт с другими жидкостями больных на гепатит С людей;
- если ваш сексуальный партнер входит в список людей больных на гепатит С;
- если ваши почки давали сбой в нормальной работе, и они проходили процесс фильтрации через аппарат, так называемый гемодиализ.
Диагностика вирусного гепатита С включает ряд исследований, медицинские работники берут кровь на анализ, так называемые «печеночные пробы». В лаборатории микроскопическим и бактериоскопическим методом наблюдают за активностью «печеночных» ферментов. Также проводятся исследования на наличие маркеров инфицирования вирусом гепатита С. В дополнение ко всем вышеперечисленным методам можно добавить еще и конфирмационные тесты. Они позволяют различить ложнопозитивные образцы от образцов крови действительно содержащих антитела, выработанные к вирусу гепатита С. В этих тестах используется принцип имунноблота, например тест RIBA или Lia TEK HCV.
Перед утверждением что пациент действительно заболел именно гепатитом С, а не любой другой его формой также берется во внимание и настоящий анамнез заболевшего. Еще, обязательно, проводится ультразвуковое обследование печени и селезенки на предмет их увеличения.
Лечение вирусного гепатита С
На данный момент абсолютного 100% лечения от гепатита С не существует. Хотя еще несколько лет назад статистика показывала, что положительные результаты в лечении этого заболевания составляло только 30-40% среди заболевших. На данный момент эта же статистика имела изменения в лучшую сторону и сейчас специалисты этой отрасли могут с уверенность сказать, что это число выросло до 50-80%. А при правильном и хорошо спланированном лечении число вылеченных людей от этой недуги может достичь и все 60-90%.
Если по результатам анализов выявлено изменения в печени, то есть обнаружили заболевание, то лечение вирусного гепатита С не стоит откладывать.
Максимально эффективные результаты может дать использование комбинированной антивирусной терапии. В состав препаратов этой самой терапии входят интерферон и рибавирин. По отдельности эти два препарата менее эффективны. Но бывают случаи, когда назначение одного из препаратов противопоказано, тогда может назначаться лечение одним препаратом, так называемая монотерапия.
Следует помнить что вирус гепатита С очень быстро мутирует и приспосабливается под иммунную систему человека, поэтому препараты которые были успешны в борьбе сегодня – завтра уже могут быть не так эффективны.
Еще практикуется симптоматическая терапия, то есть лечение направлено на то, что бы купировать симптомы вирусного гепатита С. Это и снятие психических расстройств, и понижение уровня утомляемости методом приема амфетамина, хлорофиллина и др., а также повышения сопротивляемости иммунной системы. Для этой цели вполне пригодны иммуномодулирующие препараты, такие как фоспренил, неотим, неоферон, риботан и др. Также обязательна поддержка страдающей печени гепатопротекторами: Гепабене, Эссенциале-Форте, Фосфоглив, Галстена. Но такие препараты только поддерживают и улучшают функции печени, у них нет противовирусного эффекта.
В наше время реклама очень влияет на подсознание человека. И, к сожалению, очень много рекламы лекарственных препаратов, в том числе и для лечения гепатита. Но не забывайте, что реклама не всегда является правдивой. Вреда может эти препараты и не принесут, но пользы так точно не будет. Поэтому, не занимайтесь самолечением, а обратитесь к специалистам, которые не откажут вам в помощи, и точно пропишу, то лечение вирусного гепатита С, которое вам поможет.
Труднее всего лечению поддается острый и хронический гепатит С у людей старше 40 лет, а особенно у мужчин. Также довольно сложно добиться положительных результатов в лечение этой болезни при длительном течении ее в организме человека.
Бывают случаи, когда после лечения положительного результата достигнуть не удалось, или он оказался неполным. Для таких случаев существуют специальные схемы и курсы повторной терапии. Появляются новые препараты для борьбы с гепатитом С и намного эффективнее предыдущих, поэтому есть шансы, что новые медикаменты помогут и дадут положительный результат.
Продолжительность лечения от гепатита С у каждого больного индивидуальна и зависит от ряда различных причин, а особенно от стадии гепатита С и характера его протекания у больного. Лечение вирусного гепатита С может длиться и около 12 месяцев.
При лечении гепатита могут возникать некоторые побочные эффекты. Как показывает статистика, то легко переносят лечение в основном молодые люди. К побочным эффектам можно отнести такие как: в анализе крови отмечают легкую гемолитическую анемию, то есть разрушение эритроцитов; также бывает легкая диспепсия; в крови повышенный уровень мочевой кислоты; бывает головная боль; в редких случаях непереносимость медицинских препаратов. При лечении интерферонами, побочные эффекты гарантированы, но они прогнозируются. В начальной стадии лечения организм привыкает к препаратам в виде повышения температуры, боли в суставах и в мышцах, бывает озноб, а также слабость организма. Это привыкание происходит на протяжении нескольких дней. После, организм привыкает, но усталость и слабость остается. Бывают редкие случаи, что при лечение интерферонами наблюдается снижение настроения, может быть выпадение волос, потери веса, состояние депрессии, сухость кожи. Поэтому во время лечения, обязательно необходимое наблюдения врача.
К сожалению, есть категории людей, которым комбинированное лечение вирусного гепатита С противопоказано. К таким категориям относятся:
Источник https://probolezny.ru/gepatit-c/
Источник https://diseases.medelement.com/disease/%D1%85%D1%80%D0%BE%D0%BD%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D0%B9-%D0%B2%D0%B8%D1%80%D1%83%D1%81%D0%BD%D1%8B%D0%B9-%D0%B3%D0%B5%D0%BF%D0%B0%D1%82%D0%B8%D1%82-%D1%81-%D1%83-%D0%B2%D0%B7%D1%80%D0%BE%D1%81%D0%BB%D1%8B%D1%85-%D0%BA%D1%80-%D1%80%D1%84-2021/17070
Источник https://medside.ru/virusnyiy-gepatit-c